Биосинтез глицерофосфолипидов.
3.3.1.Как известно (1.4.2), глицерофосфолипиды являются производными фосфатидной кислоты и одного из аминоспиртов (например, этаноламина, холина или серина). Реакции образования фосфатидной кислоты обсуждались в предыдущем параграфе (см. 3.2.2, рисунок 3.5).
Подобно другим предшественникам в биосинтезе липидов, аминоспирты, участвующие в синтезе фосфолипидов, вступают в реакцию в активной форме – в виде соединения с цитидиндифосфатом (ЦДФ). В качестве примера на рисунке 3.7 приводятся реакции активации этаноламина. Обратите внимание, что в реакциях активации аминоспиртов принимают участие два нуклеозидтрифосфата – АТФ и ЦТФ.
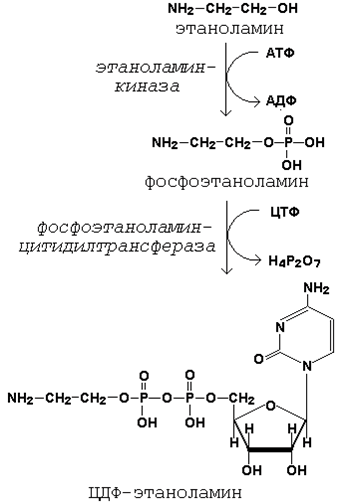
Рисунок 3.7.Реакции образования активной формы этаноламина.
Далее остаток фосфоэтаноламина с ЦДФ-этаноламина переносится на 1,2-диацилглицерол, образующийся в результате дефосфорилирования фосфатидной кислоты (рисунок 3.8, реакции 1 и 2). Продуктом реакции является фосфатидилэтаноламин.
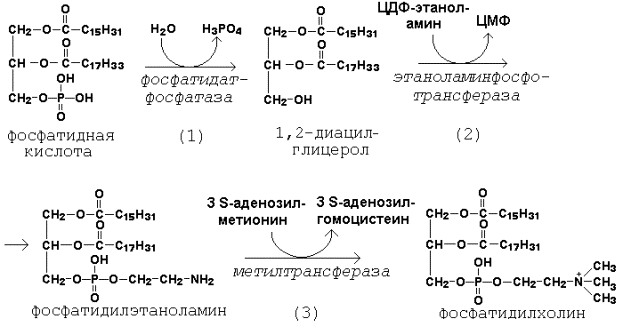
Рисунок 3.8.Реакции синтеза фосфатидилхолина.
Синтез фосфатидилхолина происходит путём трёхкратного метилирования фосфатидидэтаноламина. Донором метильных групп служит S-аденозилметионин (рисунок 3.8, реакция 3). Фосфатидилхолин может образоваться также путём активации холина, подобно этаноламину.
Фосфатидилсерин образуется в реакции прямого взаимодействия фосфатидилэтаноламина и серина:
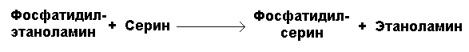
3.3.2. Липотропные факторы – вещества, способствующие синтезу фосфолипидов и препятствующие отложению триацилглицеролов в тканях.
Липотропный эффект этих соединений связан с тем, что общим предшественником триацилглицеролов и фосфолипидов является фосфатидная кислота. При недостатке липотропных факторов фосфатидная кислота используется преимущественно для синтеза триацилглицеролов. Они нерастворимы в воде и накапливаются в клетках, способствуя их жировому перерождению. Запомните, какие липотропные факторы можно использовать в качестве препаратов для его предупреждения:
1) холин – самое распространённое азотистое основание фосфолипидов;
2) метионин – незаменимая аминокислота, предшественник S-аденозилметионина, универсального донора метильных групп;
3) фолиевая кислота и витамин В12 – предшественники коферментов, участвующих в реакциях переноса СН3-групп.
При введении липотропных факторов снижается синтез триацилглицеролов и усиливается выведение жира из клеток при участии липопротеиновых комплексов (см.3.5.2).
Биосинтез холестерола.
3.4.1.Исходным соединением для синтеза холестерола является ацетил-КоА (см. 2.2.3, рисунок 2.6). Ферменты, катализирующие реакции синтеза, содержатся в цитоплазме и эндоплазматическом ретикулуме многих клеток. Наиболее активно этот процесс происходит в печени. В организме человека в сутки синтезируется около одного грамма холестерола.
3.4.2.Биосинтез холестерола включает три основные стадии (рисунок 3.9).
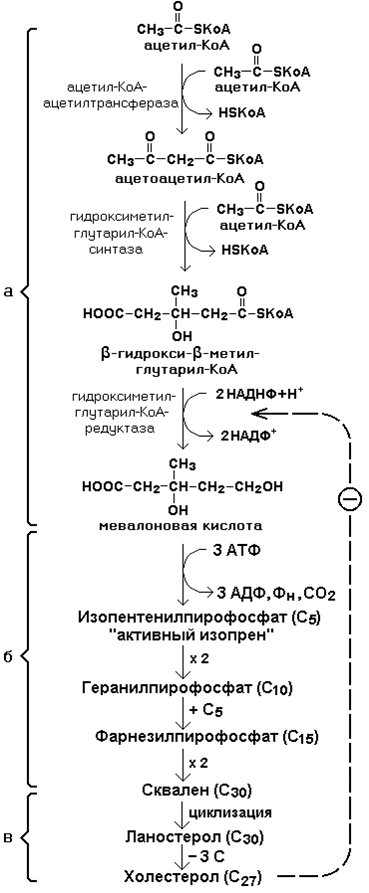
Рисунок 3.9. Синтез холестерола.
На первой стадии образуется мевалоновая кислота (рисунок 3.9, а).
На второй стадии мевалоновая кислота превращается в изопентенилпирофосфат («активный изопрен»), 6 молекул которого конденсируются в сквален (рисунок 3.9, б).
На третьей стадии сквален превращается в холестерол (рисунок 3.9, в).
Всего для синтеза 1 молекулы холестерола используется 18 молекул ацетил-КоА: для образования «активного изопрена» требуется 3 молекулы; в последующих реакциях конденсации участвуют 6 молекул «активного изопрена»; 3 × 6 = 18.
3.4.3.Скорость синтеза холестерола в организме регулируется по механизму отрицательной обратной связи (рисунок 3.8, пунктирная стрелка). Фермент β-гидрокси-β-метилглутарил-КоА-редуктаза катализирует лимитирующую реакцию биосинтеза холестерола. Холестерол является корепрессором синтеза данного ферментного белка, что приводит к снижению скорости катализируемой реакции. Поэтому при поступлении избытка холестерола с пищей синтез эндогенного холестерола прекращается.
Холестерол является компонентом биологических мембран, из него в организме образуются стероидные гормоны, витамин D3, желчные кислоты (см. 1.1.2). Избыток холестерола превращается в печени в желчные кислоты (см. 2.1.3, рисунок 2.3), а также выделяется с желчью в кишечник и выводится с калом.
3.4.4.Нормальное содержание холестерола в сыворотке крови человека составляет 3,9 – 6,3 ммоль/л. Транспортной формой холестерола в крови являются липопротеины (см. далее 3.5.2). Если нарушается соотношение между поступлением холестерола в организм и его выведением, то содержание холестерола в тканях и крови изменяется. Повышение концентрации холестерола в крови (гиперхолестеролемия) может приводить к развитию атеросклероза и желчно-каменной болезни.
Липопротеины.
3.5.1. Липиды нерастворимы в воде и поэтому транспортируются кровью в форме надмолекулярных комплексов – липопротеинов. Гидрофобное ядро липопротеинов содержит неполярные липиды (ТАГ, эфиры холестерола), оболочка состоит из амфифильных липидов (фосфолипиды, холестерол) и белков-апопротеинов (см. 2.2.2). Липопротеины различаются по химическому составу, свойствам и функциям. Основными классами липопротеинов являются: 1) хиломикроны, 2) липопротеины очень низкой плотности (ЛПОНП), 3) липопротеины низкой плотности (ЛПНП), 4) липопротеины высокой плотности (ЛПВП).
3.5.2.Особенности обмена и биологическая роль различных классов липопротеинов представлены на рисунке 3.10.
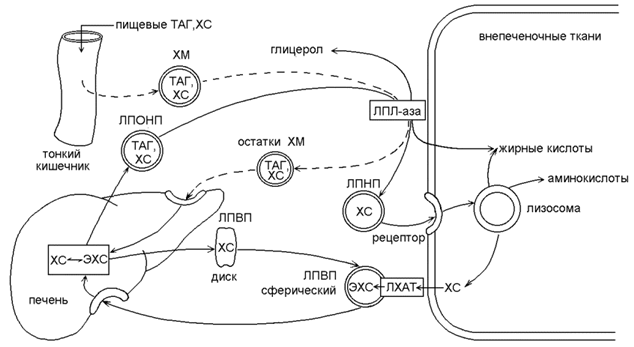
Рисунок 3.10.Обмен липопротеинов. ЛПВП - липопротеин высокой плотности; ЛПНП - липопротеин низкой плотности; ЛПОНП - липопротеин очень низкой плотности; ХМ - хиломикрон; ТГ - триацилглицерол; ХС -холестерол; ЭХС - эфир холестерола; ЛПЛ-аза - липопротеинлипаза; ЛХАТ - лецитин: холестерол-ацилтрансфераза.
Хиломикроны (см. также 2.2.2) образуются в стенке кишечника, содержат до 80% ТАГ пищевого происхождения, которые транспортируются кровью в периферические ткани. В кровеносных капиллярах ТАГ подвергаются гидролизу липопротеинлипазой; образующиеся жирные кислоты поступают в ткани, а «остатки» хиломикронов поглощаются клетками печени (рисунок 3.10, пунктирная линия).
ЛПОНП - образуются в печени, являются транспортной формой эндогенных ТАГ. Как и хиломикроны, являются субстратами липопротеинлипазы эндотелия капилляров. После гидролиза ТАГ, ЛПОНП превращаются в ЛПНП.
ЛПНП - образуются в крови из ЛПОНП под действием липопротеинлипазы. Богаты холестеролом, транспортируют его во внепечёночные ткани. В результате взаимодействия ЛПНП с рецепторами на поверхности мембран холестерол из ЛПНП проникает внутрь клеток, где участвует в образовании клеточных структур и реакциях биосинтеза веществ (см.1.4.1).
ЛПВП – образуются в печени, первоначально состоят преимущественно из белков и фосфолипидов и имеют форму дисков. При помощи фермента ЛХАТ липопротеины этого класса извлекают избыток холестерола из внепечёночных клеток и в форме эфиров доставляют его в печень.
Увеличение содержания в крови ЛПНП и ЛПОНП и уменьшение содержания ЛПВП способствует развитию атеросклероза. Следовательно, ЛПОНП и ЛПНП –атерогенные липопротеины, ЛПВП –антиатерогенные липопротеины.
