Константа равновесия ОВР, использование ОВР в аналитической химии и фармац. анализе. Связь константы равновесия с электродными потенциалами
Способность одного вещества отдавать электроны другому веществу можно оценить также с помощью константы равновесия окислительно-восстановительной реакции. Эта константа связана с ЭДС реакции следующим образом. Пусть реакция между окислителем
Ox1 и восстановителем Red2 состоит из двух полуреакций:
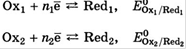

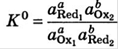
В состоянии равновесия 
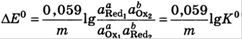
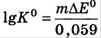
ОВР применяются для обнаружения неорг и орг в-в, маскировки мешающих ионов, при выделении неорг в-в из орг матриц, в титриметрических методах (иодо-, хлориодо-, иодато-, бромато-, нитрито-, перманганато-, дихромато-, цери-), во многих электрохим и кинетических методах анализа.
Расчет рН смеси сильных кислот, слабых кислот, смеси слабой и сильной кислоты.
2 кислоты:
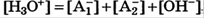
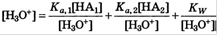
если кислота не очень слабая и не в очень маленькой конц, то автопротолизом пренебрегаем.
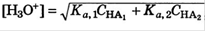
Если К*С сильно различаются, одним можно пренебречь. (сильная+слабая)
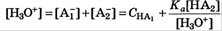
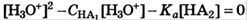
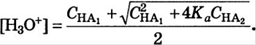
Слабые кислоты (считаем протоны одной+второй, логарифмируем)
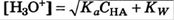 очень слабая или маленькая конц
очень слабая или маленькая конц
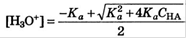 не соблюдается равенство
не соблюдается равенство 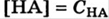
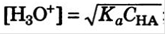

36+38. Отбор проб. Генеральная, лабораторная и анализируемая пробы. Арбитражная проба. Разложение пробы. «Мокрые» способы разложения пробы. Виды проб (представительная, генеральная, лабораторная, анализируемая). Отбор проб газов, жидкостей, твердых в-в, усреднение. Причины погрешностей.
Пробойназывается отобранная для анализа часть объекта исследования (анализируемого образца).
Средняя(представительная) проба- небольшая часть анализируемого объекта, средний состав и свойства которой считаются идентичными среднему составу и свойствам анализируемого объекта.
Генеральная проба- Величина пробы и способ отбора зависят от агрегатногосостояния образца, степени его однородности, размера частиц, допустимойнеопределённости результата анализа. Генеральная проба отбирается из объекта.
Лабораторная проба- получают из генеральной пробы путем ее измельчения и усреднения.
Анализируемая проба-часть лабораторной пробы, которая идет на качественный и
Количественный анализ.
Отбор пробы газов
Генеральная проба газообразных веществ небольшая. Используют вакуумные мерные колбы или бюретки с соответствующей запорной жидкостью, а также специальные
контейнеры. При отборе пробы газов в замкнутом пространстве (например, в
цеху, лаборатории) пробу отбирают в разных точках, а затем смешивают либо анализируют каждую из них отдельно.
Отбор пробы жидкостей
Отбор пробы гомогенной жидкости (например, глазные капли или раствор для инъекций) проводят обычно по объёму, используя для этой цели пипетки или бюретки. Предварительно жидкость тщательно перемешивают. Если анализируемую жидкость сложно или невозможно перемешать ,то отбор пробы проводят на разной глубине ёмкости.
Гетерогенные жидкости перед взятием пробы тщательно гомогенизируют путём перемешивания либо вибрации. Пробы таких жидкостей часто отбирают не только по объёму, но и по массе. Если анализируют жидкость из потока, то для получения достоверной информации пробы отбирают из различных мест по течению водотоков.
