Общие методы получения каротиноидов
Из растительного сырья
В литературе описано несколько способов извлечения каротиноидов из растительного сырья. Испанские авторы предлагают проводить извлечение суммы каротиноидов после-довательной экстракцией разнополярными растворителями. Для этого измельченные плоды растения (100 г) обрабатывают в гомогенизаторе 100 мл ацетона. Процесс экстракции повторяют до получения бесцветных экстрактов. Экстракты объединяют, обрабатывают в делительной воронке 100 мл диэтилового эфира, интенсивно встряхивают, оставляют смесь до полного расслоения. После чего, для перевода каротиноидов в эфирный слой в делительную воронку добавляют 30 мл 10% раствора натрия хлорида и интенсивно встряхивают в течение 10 мин. После расслоения фаз эфирный слой сушат трехкратной обработкой безводным натрия сульфатом. Для удаления жирных кислот, перешедших в эфирную фракцию, проводят омыление раствора действием 100 мл 10% раствора калия гидроксида в спирте метиловом при периодическом встряхивании в течение 3 часов. После этого каротиноиды переводят в эфирный слой, действием воды очищенной. Органическую фазу промывают водой очищенной до удаления следов щелочи, сушат фильтрованием через слой безводного натрия сульфата и концентрируют в мягких условиях на роторном испарителе [88].
Достаточно селективным может также считаться выделение суммы каротиноидов по методу [97]: измельченное растительное сырье трижды (по 10 мл) экстрагируют тетрагидрофураном, содержащим 0.1% бензилбутилового эфира в присутствии безводного натрия сульфата (20% от веса растения). Полученный экстракт подвергают ультразвуковому воздействию в течение 30 мин каждый раз, при температуре 5-100С. Объединенные извлечения концентрируют досуха на роторном испарителе в мягких условиях (вакуум водоструйного насоса, температура не выше 400С). Концентрат растворяют в 4 мл дихлорметана и фильтруют через 0.45-мкм поливинилиден фторидный (или подобный) мембранный фильтр. Растворитель удаляют продуванием тока азота, сумму каротиноидов растворяют в гексане и анализируют методом ВЭЖХ.
КСАНТОНЫ
Ксантоны – это конденсированная система бензольных колец и гетерокольца. С другой стороны их можно рассматривать как производные хромона.
В растениях это пигменты желтого цвета, чаще a– и b-оксипроизводные и димерные структуры, которые обладают антимикробным и инсектицидным действием.
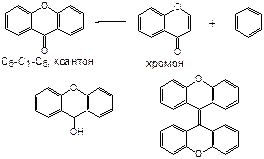 |
Все производные ксантонов растворимы в спирте при нагревании, в эфире, бензоле и хлороформе.
Выделение:
Около 1 г измельченного растительного сырья заливают 15-20 мл этилацетата, спирта этилового 70-80% или спирта метилового 50-80% и экстрагируют в течение 30-40 мин в колбе при нагревании на водяной бане, фильтруют.
Для качественных реакций используют 2-3 мл раствора.
Качественный анализ [7,10-12]:
Ксантоны дают реакции фенолов с оттенками, в зависимости от расположения ОН-групп. Можно обнаружить их в УФ-свете.
q Наносят несколько капель анализируемого раствора на фильтровальную или хроматографическую бумагу, появляется бледно-желтое окрашивание, которое в УФ-свете имеет абрикосовый цвет.
q Прибавляют 2-3 мл спиртового раствора алюминия хлорида, встряхивают, появляется зелено-голубое окрашивание.
Другие реакции являются общими для полифенолов.
Хроматографический анализ:
Разделению, анализу со стандартными образцами и препаративному выделению растительных ксантонов в тонком слое сорбента посвящено большое количество публикаций. Основными ТСХ хроматографическими системами в исследовании ксантонов являются:
- Хлороформ-метанол (9:1)
- Хлороформ-петролейный эфир (9:1)
- Гексан-этилацетат (98:2)
- Толуол-ацетон (19:1)
- Толуол-уксусная кислота (20:3)
- н-бутанол-уксусная кислота-вода (12:3:5 и 20:5:8)
- Хлороформ-ацетон-муравьиная кислота (70:30:0.5, 80:20:1 и 90:10:0.5)
- Толуол-этилацетат-муравьиная кислота (65:35:1)
- Петролейный эфир-этилацетат-муравьиная кислота (70:30:1)
В виду того, что ксантоны в растительных объектах редко присутствуют в виде многокомпонентных смесей, а также относительной легкости их выделения, методы ВЭЖХ не получили сколько-нибудь широкого распространения в исследовании ксантонов и их производных. Однако анализ имеющихся методик позволяет сделать вывод о том, что наиболее подходящей неподвижной фазой в условиях обращенно-фазного распределения при анализе ксантон-содержащих экстрактов являются mBondapak RP-C18 и mBondasphere C18 100-AE сорбенты. Подвижной фазой служит, как правило, система метанол-вода состава (1:1, 2:3, 7:13 и 9:1) в условиях изократического элюирования с фотодиодным или УФ детектором (237 нм) [98-100].
Количественное определение:
Около 2 г (точная навеска) измельченного сырья помещают в круглодонную колбу вместимостью 100 мл, прибавляют 30 мл 50% водного ацетона, 5 мл кислоты хлороводородной, нагревают на кипящей водяной бане с обратным холодильником в течение 1 часа. Гидролизат охлаждают, фильтруют, концентрируют до объема 2-3 мл и хроматографируют на пластинках силикагеля или целлюлозы в присутствии СО мангиферина, используя в качестве подвижной фазы 15% раствор кислоты уксусной.
Пятна, соответствующие мангиферину (Rf=0.38-0.42) и другим ксантоновым соединениям (ярко-оранжевые в УФ свете) соскабливают с пластинки и элюируют в колбе 15 мл 50% водного ацетона настаиванием в течение 15-17 часов. Экстракт фильтруют и определяют оптическую плотность при длине волны 372 нм в кювете с толщиной слоя 10 мм.
Содержание ксантонов в абсолютно сухом сырье, в пересчете на мангиферин в процентах (Х), вычисляют по формуле:
|
D1 . V1 . m . (100 - W)
где D - оптическая плотность испытуемого раствора при длине волны 372 нм;
D1– оптическая плотность раствора СО при длине волны 372 нм;
m – масса навески сырья, в граммах;
m1 – масса навески СО, в граммах;
V1 – объем раствора СО, в миллилитрах, нанесенного на хроматограмму;
V2 – объем испытуемого раствора в миллилитрах, нанесен-ного на хроматограмму;
W – потеря в массе при высушивании сырья в процентах.
