Функции белков. Аминокислоты
Белки выполняют в организме очень важные функции. К ним в первую очередь следует отнести: структурную, каталитическую, сократительную, транспортную, регуляторную, защитную, а также энергетическую. На долю белков в среднем приходится 1/6 часть от массы тела человека.
По строению белки - это высокомолекулярные азотсодержащие соединения, состоящие из аминокислот.В состав белковых молекул могут входить десятки, сотни и тысячи остатков аминокислот. Однако все белки, независимо от происхождения, содержат лишь 20 видов аминокислот Строение 20 разновидностей аминокислот, входящих во все белки, можно отразить следующей формулой:
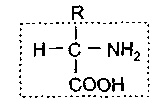 |
У всех аминокислот можно выделить общую, одинаковую часть молекулы, содержащую амино- и карбоксильную группы. Другая же часть молекулы, обозначенная как радикал, у каждой из 20 аминокислот имеет специфическое строение, и аминокислоты отличаются друг от друга только радикалами. Аминокислоты, соединяясь друг с другом пептидной связью, образуют длинные неразветвленные цепи - полипептиды. Пептидная связь возникает при взаимодействии карбоксильной группы одной аминокислоты и аминогруппы другой аминокислоты с выделением воды. Пептидные связи обладают высокой прочностью, их образуют все аминокислоты. В состав белковой молекулы входит один или несколько полипептидов.
Кроме пептидных, в белках обнаруживаются еще дисульфидные, водородные, ионные и другие связи. Эти химические связи могут возникать между остатками аминокислот, которые входят в разные участки одного и того же полипептида или же находятся в разных полипептидах, но обязательно пространственно сближены. В первом случае благодаря таким связям полипептидная цепь принимает определенную пространственную форму. Во втором случае с помощью непептидных связей полипептиды объединяются в белковую молекулу. В итоге молекула белка является объемным, трехмерным образованием, имеющим определенную пространственную форму.
Структура белков
Первый уровень пространственной организации белковой молекулы называется первичной структуройи представляет собой последовательность расположения аминокислот в полипептидных цепях. Фиксируется эта структура прочными пептидными связями. Другими словами, первичная структура характеризует химическое строение полипептидов, образующих белковую молекулу. Каждый индивидуальный белок имеет уникальную первичную структуру.
Второй уровень пространственной организации - вторичная структура- описывает пространственную форму полипептидных цепей. Например, у многих белков полипептидные цепи имеют форму спирали. Фиксируется вторичная структура дисульфидными и различными нековалентными связями.
Третий уровень пространственной организации - третичная структура- отражает пространственную форму вторичной структуры. Например, вторичная структура в форме спирали, в свою очередь, может укладываться в пространстве в виде глобулы, т. е. имеет шаровидную или яйцевидную форму. Стабилизируется третичная структура слабыми нековалентными связами, а также дисульфидными связями и поэтому является самой неустойчивой структурой.
Пространственная форма всей белковой молекулы получила название конформация.Поскольку в молекуле белка наряду с прочными ковалентными связями имеются еще менее прочные (нековалентные) связи, то его конформация характеризуется нестабильностью и может легко изменяться. Изменение пространственной формы белка влияет на его биологические функции. Конформация, находясь в которой белок обладает биологической активностью, называется нативной.Любые воздействия на белок, приводящие к нарушению этой конформации, сопровождаются частичной или полной утратой белком его биологических свойств. Изменение конформации в небольших пределах обратимо и является одним из механизмов регуляции биологических функций белков в организме.
Четвертичной структуройобладают только некоторые белки. Четвертичная структура - это сложное надмолекулярное образование, состоящее из нескольких белков, имеющих свою собственную первичную, вторичную и третичную структуры. Каждый белок, входящий в состав четвертичной структуры, называется субъединицей. Ассоциация субъединиц в четвертичную структуру приводит к возникновению нового биологического свойства, отсутствующего у свободных субъединиц. Например, формирование четвертичной структуры в ряде случаев сопровождается появлением каталитической активности, которой нет у отдельных субъединиц.
Нуклеиновые кислоты
По своему строению нуклеиновые кислоты являются полинуклеотидами,состоящими из очень большого количества мононуклеотидов (нуклеотидов).Любой нуклеотид обязательно включает в себя азотистое основание(циклическое соединение, содержащее атомы азота и обладающее щелочными свойствами), углеводи фосфорную кислоту.
Азотистые основания бывают двух типов: пуриновыеи пиримидиновые.
 |
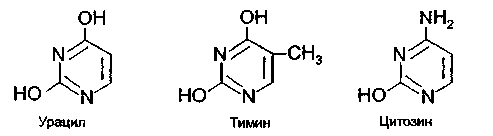
| Пиримидиновыми основаниями являются урацил, тимин и цитозин: |
 |
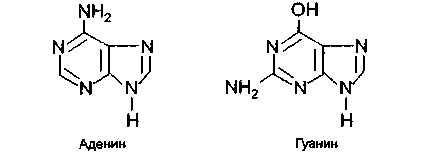
К пуриновым основаниям относятся аденини гуанин,имеющие следующее строение
Углеводом, входящим в состав нуклеотидов, может быть рибозаили дезоксирибоза,находящиеся в циклической форме
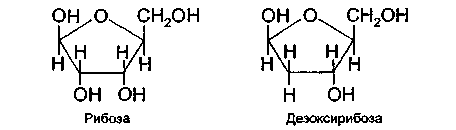
Азотистые основания присоединяются к первому углеродному атому. Азотистое основание, связанное с углеводом, называется нуклеозидом. Нуклеозиды, содержащие аденин и гуанин, называются соответственно аденозини гуанозин,а нуклеозиды с пиримидиновыми основаниями получили названия: уридин, тимидини цитидин. Нуклеотиды, входящие в состав нуклеиновых кислот, имеют один остаток фосфорной кислоты, а свободные нуклеотиды могут содержать от одного до трех фосфатных остатков Нуклеотиды, входящие в нуклеиновые кислоты, соединяются друг с другом в длинные полинуклеотидные цепи эфирными связями, идущими от углевода одного нуклеотида к фосфорной кислоте соседнего. В результате такого связывания образуется длинная цепь, состоящая из чередующихся остатков углевода и фосфорной кислоты. Азотистые основания непосредственно в эту цепь не входят; они как боковые веточки присоединяются к углеводам. Отличаются полинуклеотиды друг от друга длиной (т. е. количеством нуклеотидов) и последовательностью расположения азотистых оснований.
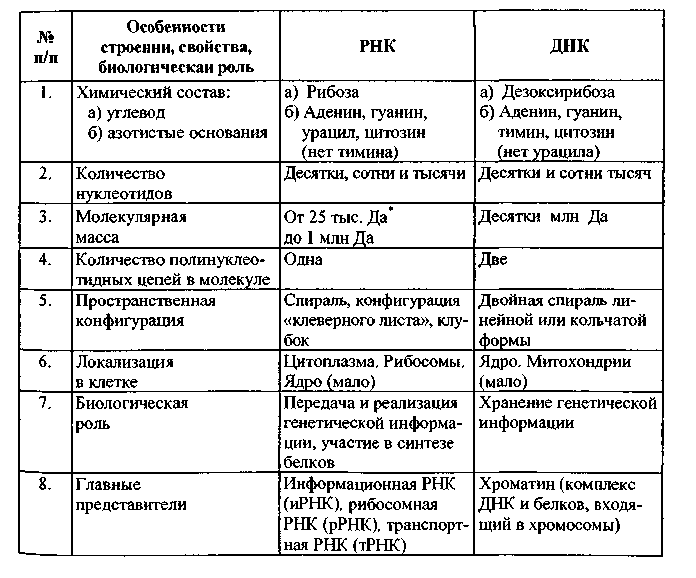
Все нуклеиновые кислоты делятся на два типа: рибонуклеиновые- РНК(содержат рибозу) и дезоксирибонуклеиновые- ДНК(содержат дезоксирибозу). Азотистые основания обеих цепей находятся внутри двойной спирали и соединены друг с другом водородными связями. Связывание (спаривание) азотистых оснований осуществляется строго определенным образом. Аденин всегда соединяется с тимином, а гуанин - с ци-тозином, причем все без исключения основания одной цепи спарены с основаниями второй. Вследствие этого обе нук-леотидные цепи, образующие молекулу ДНК, имеют одинаковую длину и пространственно соответствуют друг другу. Если в каком-то месте одной цепи находится аденин, то обязательно напротив него в другой цепи присутствует тимин, а напротив гуанина всегда располагается цитозин.
Такое пространственное соответствие двух полинуклеотидных цепей ДНК получило название комплементарность.
Принцип комплементарности лежит в основе таких важнейших процессов, как репликация(удвоение молекулы ДНК в процессе клеточного деления), транскрипция(передача генетической информации с молекулы ДНК информационной РНК в процессе синтеза белков) и трансляция(сборка из аминокислот белковой молекулы на рибосомах).
Углеводы
Углеводы - это альдегидоспирты или кетоспирты и их производные. В природе углеводы содержатся главным образом в растениях. В организме человека углеводов около 1%.
Основным природным углеводом является глюкоза, которая может находиться как в свободном виде (моносахарид), так и в составе олигосахаридов (сахароза, лактоза и др.) и полисахаридов (клетчатка, крахмал, гликоген).
Эмпирическая формула глюкозы СбН1206. Однако, как известно, глюкоза может иметь различные пространственные формы (ациклическую и циклические). В организме человека почти вся глюкоза (свободная и входящая в олиго- и полисахариды) находится в циклической а-пиранозной форме:
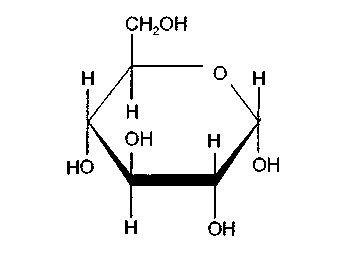
Свободная глюкоза в организме человека в основном находится в крови, где ее содержание довольно постоянно и колеблется в узком диапазоне от 3,9 до 6,1 ммоль/л (70-110 мг%).
Другим углеводом, типичным для человека и высших животных, является гликоген.Состоит гликоген из сильно разветвленных молекул большого размера, содержащих десятки тысяч остатков глюкозы. Эмпирическая формула гликогена - (С6Н10О5)„ (С6Н10О5 - остаток глюкозы).
Гликоген является запасной, резервной формой глюкозы. Основные запасы гликогена сосредоточены в печени (до 5-6% от массы печени) и в мышцах (до 2-3% от их массы). Глюкоза и гликоген в организме выполняют энергетическую функцию, являясь главными источниками энергии для всех клеток организма.
