Классификация и характеристика отдельных классов ферментов
По мере открытия новых ферментов, изучения их свойств возникала необходимость в классификации ферментов. В зависимости от типа катализируемой реакции все ферменты делятся на 6 классов:
1) оксидоредуктазы;
2) трансферазы;
3) гидролазы;
4) лиазы;
5) изомеразы;
6) лигазы (синтетазы).
Классы ферментов делятся на подклассы, а те в свою очередь на подподклассы. Подкласс уточняет действие фермента, так как указывает в общих чертах на природу химической группы субстрата, атакуемой ферментом. Подподкласс еще более конкретизирует действие фермента, уточняя природу атакуемой связи субстрата или природу акцептора, который участвует в реакции.
Ферменты класса оксидоредуктаз катализируют окислительно-восстановительные реакции.
К этому классу относятся ферменты дегидрогеназы, участвующие в переносе атомов водорода. Они подразделяются на анаэробные:
H H
/ /
схема реакции: S1 + S2 ¾¾¾® S1 + S2
\ \
H H
перенос атомов Н2 на любой S кроме О2
и аэробные:
H
/
S + O2 ¾¾¾®S + H2O2 акцептором Н2 служит О2
\
H
К классу оксидоредуктаз также относятся цитохромы. Эти ферменты участвуют в переносе электронов. Например, цитохромы a, b, c. Цитохромоксидаза (цитохром a3) переносит электроны на О2.
Ферменты каталаза и пероксидаза, относящиеся к классу оксидоредуктаз, участвуют в переносе атомов водорода на акцептор, которым является пероксид водорода:
каталаза
Н2О2 + Н2О2 ¾¾¾®2 Н2О+О2
Н
/ пероксидаза
S + Н2О2 ¾¾¾¾® S + 2Н2О
\
Н
Трансферазы катализируют реакции межмолекулярного переноса различных групп и остатков.
В зависимости от типа переносимой группировки различают:
- метилтрансферазы (перенос групп -СН3);
- ацилтрансферазы (перенос ацильных групп R-C=O);
\
- гликозилтрансферазы (перенос остатков углеводов, например, фермент гликогенфосфорилаза переносит остаток глюкозы с гликогена на фосфорную кислоту с образованием глюкозо-1-фосфата в процессе расщепления гликогена);
- аминотрансферазы (перенос аминогрупп -NH2 с аминокислоты на кетокислоту в процессе синтеза заменимых аминокислот):
СООН СООН аланин- СООН СООН
½ ½ аминотран- ½ ½
СНNH2 C=O сфераза C=O + CHNH2
½ ½ <=========> ½ ½
CH3 СH2 CH3 CH2
I I
CH2 CH2
½ ½
COOH COOH
a-аланин a- кетоглутаровая пировиноградная глутамино-
кислота кислота вая кислота
- фосфотрансферазы (перенос фосфатных групп). Перенос фосфатных групп с АТФ на субстрат или с субстрата на АДФ осуществляют ферменты киназы (например, гексокиназа переносит фосфатную группу с АТФ на глюкозу с образованием глюкозо-6-фосфата в процессе гликолиза).
Гидролазы участвуют в расщеплении внутримолекулярных связей (кроме -С-С-) в органических веществах гидролитическим путем, т.е. с участием воды. Важное место среди ферментов этого класса занимают пищеварительные ферменты, участвующие в переваривании липидов(липазы), белков (пептидазы) и углеводов (гликозодазы).
Липазы, относящиеся к подклассу эстераз, осуществляют гидролиз сложноэфирных связей осуществляют в молекулах триглицеридов:
O
II
СН2 - О - С - R1 СН2 - О - H R1 - COOH
½ O + 3 Н2О ½
½ II липаза ½
СН - О - С - R2 ¾¾® СН - О - H + R2 - COOH
½ O ½
½ II ½
СН2 - О - С - R3 СН2 - О - H R3 - COOH
триглицерид глицерин жирные кислоты
В данном случае расщепляются сложноэфирные связи, образованные спиртом и карбоновыми кислотами - такой гидролиз осуществляют карбоксиэстеразы.
К классу гидролаз относятся гликозидазы. Они расщепляют гликозидные связи в молекулах ди - и полисахаридов. Примеры: Сахараза расщепляет сахарозу на a- Д-глюкозу и b - Д-фруктозу, амилаза расщепляет крахмал до мальтозы.
Ферменты пептидазы осуществляют гидролиз пептидных связей в молекулах белков и пептидов:
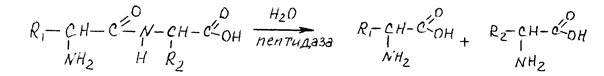
дипептид аминокислоты
Эндопептидазы расщепляют пептидные связи внутри молекул (например, пепсин). Экзопептидазы делятся на карбоксипептидазы (расщепляют пептидные связи с С-конца цепи) и аминопептидазы (расщепляют пептидные связи с N-конца цепи).
Лиазы расщепляют внутримолекулярные связи в органических веществах (включая - С-С-) не гидролитическим путем, а также катализируют реакции присоединения группировок по месту разрыва двойных связей.
Примеры:
O
II
С - ОН
I пируват- O
C= O декарбоксилаза II
I ¾¾¾¾¾® C- H
CH3 - CO2 I
СH3
пировиноградная кислота уксусный альдегид
CООH СООH
I + Н2О I
C - H фумаратгидратаза HO - C - H
II ¾¾¾¾® I
H- C CH2
I I
CОOH СООН
фумаровая L - яблочная
кислота кислота
Изомеразы катализируют реакции взаимопревращения изомеров.
Пример:
O
II
C - H триозофосфатизомераза СH2 - OH
I ¾¾¾¾¾® I
H - C - OH OH C=O OH
I I I I
CH2 - O - P=O CH2 - O - P = O
I I
OH OH
глицеральдегид-3-фосфат дигидроксиацетонфосфат
Ферменты класса лигаз катализируют реакции присоединения 2-х молекул друг к другу сопряженное с разрывом пирофосфатной связи в молекуле АТФ или ее аналогов, т.е. они осуществляют синтез сложного вещества из более простых с использованием энергии АТФ или ее аналогов.
Пример:
АТФ, СО2
CОOH пируваткарбоксилаза CОOH
I ¾¾¾¾¾® I
C=O - АДФ C=O
I Н3РО4 I
CH3 СH2
пировиноградная I
кислота CОOH
щавелево-уксусная кислота
Строение ферментов
