Гравиметрический метод анализа
Гравиметрический метод анализа основан на точном измерении массы вещества, выделенного в виде соединения известного состава или в элементарном виде. Метод базируется на законе сохранения массы вещества в химических реакциях. Для определения веществ методом гравиметрии используют осаждение или отгонку. При отгонке определяемое вещество отгоняют в виде летучего соединения.
При анализе вещества по методу осаждения определяемый компонент выделяют в осадок, который затем отфильтровывают, промывают, высушивают, иногда прокаливают до постоянной массы и взвешивают на аналитических весах.
Количество осадка обычно эквивалентно количеству вещества, вступившего в реакцию, поэтому по количеству осадка можно рассчитать количество исходного вещества.
Например, ионы Ca2+ в солях можно определить методом осаждения, используя в качестве реактива оксалат аммония:
CaCl2 + (NH4)2C2O4 = CaC2O4 + 2NH4Cl.
Осадок CaC2O4 промывают, высушивают и прокаливают. При этом оксалат кальция переходит в оксид кальция:
CaC2O4 = CaO +CO2↑ + CO↑ (t > 200 °C).
Образовавшийся оксид кальция взвешивают и по его количеству рассчитывают содержание кальция в анализируемом веществе.
В связи с тем, что многие осадки при последующем прокаливании изменяют свой состав, различают осаждаемую и весовую форму осадка. В примере с определением кальция сначала была получена осаждаемая форма осадка CaC2O4. А при прокаливании осаждаемая форма перешла в весовую - CaO.
В ряде случаев, например, при осаждении Ba2+ серной кислотой, состав осаждаемой и весовой форм совпадает.
Ba2+ + SO42- = BaSO4.
13.Осаждаемая форма осадка (форма осаждения) - соединение, которое осаждается из раствора при взаимодействии определяемого компонента с соответствующим реагентом (или соединение, в виде которого осаждают анализируемое вещество).
Гравиметрическая (весовая) форма - соединение, которое взвешивают для получения окончательного результата анализа (или соединение, в виде которого взвешивают определяемый компонент).
Наиболее часто составы осаждаемой и гравиметрической форм не совпадают. Реже их состав одинаков. Например, хлорид- и Ag+-ионы определяют г.а., осаждая их в виде AgCl.
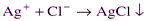
Осаждаемая и гравиметрическая формы в этом случае имеют одинаковый состав AgCl.
3.4. Требования к осаждаемой и гравиметрической формам осадка
Для получения точных результатов в гравиметрических методах осаждаемая и гравиметрическая формы осадка должны соответствовать определенным требованиям.
Требования к осаждаемой форме:
1. Осадок должен быть практически нерастворим.
Это означает, что в растворе после осаждения и промывания осадка, определяемого компонента должно оставаться меньше, чем можно взвесить на аналитических весах. Опыт показывает, что для бинарных электролитов (т.е. соединений, каждая молекула которых образует при диссоциации два иона, например, AgI, PbSO4 и т.д.) практически полное осаждение может быть достигнуто лишь тогда, когда ПР осадка имеет значение, не превышающее 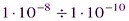 . (Если же соединение тринарное, тетрарное и более сложного состава, то ПР будет другим, но всегда растворимость осадка не должна превышать 10-6 г/л).
. (Если же соединение тринарное, тетрарное и более сложного состава, то ПР будет другим, но всегда растворимость осадка не должна превышать 10-6 г/л).
2.Желательно, чтобы структура осадка давала возможность с достаточной скоростью выполнить операции фильтрования и промывания осадка.
В этом отношении очень удобны крупнокристаллические осадки, т.к.они почти не забивают поры фильтра, мало загрязняются посторонними примесями из анализируемого раствора и легко отмываются от них.
Аморфные осадки типа Al(OH)3 и Fe(OH)3, имея сильно развитую поверхность, являясь рыхлыми и объемными, значительно адсорбируют примеси из анализируемого раствора, трудно отмываются от них, а также медленно фильтруются. Однако, если соединений, обладающих более подходящими для анализа свойствами, не известно, то работают и с такими осадками. Стремятся только обеспечить все условия, способствующие наибольшему устранению или уменьшению недостатков аморфных осадков (эти условия представлены в разделе 3.5.5).
3. Необходимо, чтобы осаждаемая форма достаточно легко и полностью превращалась в гравиметрическую форму.
Требования к гравиметрической форме:
1. Состав гравиметрической формы должен соответствовать определенной химической формуле.
На практике многие осадки не удовлетворяют этому требованию. Например, осадок гидроксида железа не соответствует формуле Fe(OH)3, более правильно принято писать 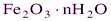 . Количество воды в этом соединении непостоянно и зависит от условий осаждения. Но после прокаливания гидроксид железа переходит в стабильную гравиметрическую форму, строго соответствующую формуле Fe2O3.
. Количество воды в этом соединении непостоянно и зависит от условий осаждения. Но после прокаливания гидроксид железа переходит в стабильную гравиметрическую форму, строго соответствующую формуле Fe2O3.
2.Гравиметрическая форма должна обладать достаточной химической устойчивостью.
Иначе нарушится соответствие ее состава определенной химической формуле. Если установлено, что гравиметрическая форма может легко изменять свой состав вследствие, например, поглощения водяных паров или СО2 из воздуха, окисления (восстановления), разложения или других подобных реакций, то ее превращают в более удобную форму, обрабатывая соответствующими ре-агентами. Например, осадок СаО, легко поглощающий Н2О и СО2из воздуха (что затрудняет его точное взвешивание), иногда превращают в CaSO4, обработав серной кислотой.
3. Гравиметрическая форма, получаемая путем прокаливания, должна обладать устойчивостью при высоких температурах (термоустойчивостью).
Некоторые гравиметрические формы могут разлагаться при высоких (порядка 1200-1300 оС и выше) температурах.
Например,
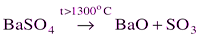 ;
;
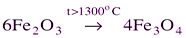 ,
,
поэтому осадки прокаливают при температуре не выше 1100 оС.
14. Осаждение. Оптимальные условия осаждения кристаллических и аморфных осадков
В зависимости от индивидуальных свойств анализируемых веществ и условий осаждения процесс образования осадка может идти двумя путями, которые приводят к образованию либо кристаллического, либо аморфного осадка. В разделе 3.4 было отмечено, что в гравиметрии отдают предпочтение крупнокристаллическим осадкам. Прежде, чем указать условия, при которых они получаются, необходимо хотя бы в общих чертах рассмотреть, как протекает процесс образования осадка (твердой фазы) в растворе.
Оптимальные условия получения кристаллических осадков. Если относительное пересыщение мало (значение Q мало, а S велико), то меньшее число первичных кристаллов будет возникать, и крупнее они будут. Следовательно, для получения крупнокристаллических осадков необходимо в процессе осаждения повышать растворимость осадка и понижать концентрации осаждаемого и осаждающих ионов.
Для повышения растворимости (S) осадков в процессе осаждения:
а) обычно повышают температуру: ведут осаждение из горячего анализируемого раствора, иногда нагревают и раствор осадителя; но осадок отфильтровывают только после охлаждения раствора;
б) добавляют в раствор вещества, повышающие растворимость осадков.
Заметим, что после того, как осадок сформируется, растворимость понижают, иначе осаждение будет неполным. Например, при осаждении сульфата бария прибавляют HCl, которая повышает его растворимость вследствие образования  -ионов. К концу осаждения эту повышенную растворимость BaSO4 снова понижают, прибавляя небольшой избыток осадителя.
-ионов. К концу осаждения эту повышенную растворимость BaSO4 снова понижают, прибавляя небольшой избыток осадителя.
^ Для понижения концентрации реагирующих ионов при формировании осадка: а) ведут осаждение из разбавленного анализируемого раствора разбавленным раствором осадителя; б) раствор с осадком непрерывно перемешивают;
Перемешивание способствует снижению высоких местных (локальных) концентраций осадителя и увеличению скорости растворения первичного осадка. Число зародышевых кристаллов при этом уменьшается, и создаются условия для роста крупных кристаллов.
в) осадитель добавляют очень медленно, по каплям (особенно в начале осаждения);
При медленном осаждении (наряду с одновременным тщательным перемешиванием анализируемого раствора) обеспечивается равномерное распределение и малая концентрация осадителя во всем объеме раствора. Вследствие этого степень пересыщения невелика и первичных центров кристаллизации появляется сравнительно немного. Образующиеся первичные кристаллы успевают правильно ориентироваться по отношению друг к другу (ориентация- расположение частиц осадка в процессе агрегации в строго определенном порядке). Дальнейшее прибавление новых порций осадителя приводит не столько к возникновению новых центров кристаллизации, сколько к увеличению размеров уже образовавшихся центров и к получению крупнокристаллических осадков. Чем больше скорость образования осадка, тем быстрее нарушается правильная ориентация при кристаллизации. При быстром осаждении сразу появляется много зародышевых, а затем мелких кристаллов.
г) иногда связывают осаждаемый ион в комплексное соединение средней прочности;
Достаточно низкая концентрация осаждаемого иона в растворе создается за счет частичной диссоциации комплексного соединения. При добавлении оса-дителя концентрация осаждаемого иона понижается из-за образования осадка, а, следовательно, будет смещаться равновесие ионизации комплекса. В раствор переходят новые ионы о.в., но их концентрация все время будет оставаться низкой.
д) применяют возникающие реагенты.
В раствор добавляют не осадитель, а вещество, которое, вступая в какую-либо реакцию, образует этот осадитель. Необходимым условием является медленное протекание такой реакции, в результате чего ион осадителя постепенно, очень маленькими порциями «возникает» (образуется) в исследуемом растворе. Его концентрация всегда остается низкой, что способствует понижению относительного пересыщения раствора. Например, существуют реагенты, которые претерпевают в растворе медленный гидролиз с выделением собственно осадителя. К таким реагентам относятся некоторые сложные эфиры: триэтилфосфат, диметилфосфат, метилоксалат, этилоксалат и т.д. Один из них, диметилсульфат, применяют для гравиметрического определения ионов Ва2+. Ионы Ва2+осаждаются H2SO4, образующейся в результате медленного гидролиза диметилсульфата.
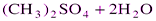

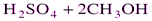
Такой метод называется методом возникающих реагентов. Процесс осаждения с помощью возникающих реагентов называют также процессом осаждения из гомогенного раствора.
Оптимальные условия получения аморфных осадков. Из формулы (43) видно, что если вещество малорастворимо (величина S мала) и выделяется из сравнительно концентрированных растворов (Q велико), то относительное пересыщение велико. Это будет способствовать быстрому образованию в раст-воре огромного количества зародышевых кристаллов, их быстрой агрегации и выделению аморфного осадка, поэтому первым условием при получении аморфных осадков является следующее: их необходимо осаждать из концентрированных растворов концентрированным раствором осадителя. Таким способом, они получаются гораздо более плотными, с меньшей поверхностью, быстрее оседают и легче отмываются от примесей.
Другие условия получения аморфных осадков обусловлены особенностями их образования. Ранее уже было отмечено, что в результате соединения первичных кристаллов в более крупные агрегаты происходит коагуляция коллоидного раствора, выпадает аморфный осадок. Очевидно, что при получении такого осадка наиболее важно создать условия, способствующие быстрому про-теканию именно этого процесса. Они определяются необходимостью устранить влияние двух основных факторов, препятствующих коагуляции коллоидных частиц и укрупнению частиц коллоидных осадков.
Первым фактором, мешающим сцеплению коллоидных частиц друг с другом, является наличие у них одноименных электрических зарядов, между которыми действуют силы электростатического отталкивания (эти заряды возникают в результате адсорбции коллоидными частицами ионов из раствора) (см. раздел 3.5.7). Для того, чтобы устранить его негативное влияние, осаждение аморфных осадков ведут в присутствии подходящего электролита-коагу-лянта. Заряд иона этого электролита всегда противоположен знаку заряда частиц, поэтому ионы электролита-коагулянта, адсорбируясь на поверхности коллоидных частиц, нейтрализуют их заряд и дают им возможность соединяться в агрегаты. В качестве электролитов-коагулянтов в гравиметрии обычно применяют различные соли аммония или кислоты.
Другим фактором, препятствующим сцеплению коллоидных частиц, является адсорбция ими молекул растворителя - сольватация коллоидных частиц (если растворителем является вода, то говорят о гидратации коллоидных частиц). Сольватные оболочки мешают коллоидным частицам достаточно близко подойти друг к другу и объединиться в более крупные агрегаты.
Загрязнение осадков
Основной причиной, вызывающей загрязнение осадков, является соосаждение. Соосаждением называют одновременное осаждение растворимого компонента с макрокомпонентом (осадком) из одного и того же раствора путем адсорбции, окклюзии, образования смешанных кристаллов или механического захвата частиц других фаз. Осадки при этом загрязнены веществами, произведение растворимости для которых не достигается.
Адсорбция — увеличение поверхностной концентрации растворенных веществ на границе раздела фаз. В соответствии с правилом адсорбции на поверхности осадка в первую очередь адсорбируются ионы, входящие в состав кристаллической решетки осадка и находящиеся в избытке (первичная адсорбция). При этом поверхность осадка приобретает положительный или отрицательный заряд, в зависимости от того, какие ионы в растворе находятся в избытке. Под действием заряда к поверхности осадка притягиваются противоионы, которые удерживаются слабее первично адсорбированных ионов. При осаждении, например, сульфат-ионов действием избытка раствора хлорида бария первично адсорбированными на поверхности BaSOi ионами после полного осаждения осадка являются ионы бария, противоионами — хлорид-ионы.
Адсорбируемость ионов на поверхности осадка зависит также от концентрации ионов, находящихся в растворе, от заряда ионов (многозарядные адсорбируются легче однозарядных) и от их размера (при прочих равных условиях в первую очередь адсорбируются ионы, имеющие примерно тот же размер, что и ионы, входящие в состав кристаллической решетки осадка). Количество адсорбированных на поверхности осадка ионов тем больше, чем больше его поверхность, поэтому к адсорбции более склонны осадки с развитой поверхностью, т. е. аморфные. Для предотвращения явления адсорбции осаждение как аморфных, так и кристаллических осадков проводят в условиях, позволяющих получить осадки с наименьшей поверхностью повышение температуры также способствует уменьшению адсорбции, так как адсорбция — экзотермический процесс. Количество адсорбированных примесей можно уменьшить при промывании осадков на фильтре водой или промывной жидкостью, а также в случае кристаллических осадков в процессе их старения.
15.
Способы выражения концентрации растворов Концентрацию веществ в растворах можно выразить разными способами. На этой страничке вы с ними познакомитесь. Наиболее часто используют массовую долю растворённого вещества, молярную и нормальную концентрацию. Массовая доля растворённого вещества w(B) - это безразмерная величина, равная отношению массы растворённого вещества к общей массе раствора m : w(B)= m(B) / m Массовую долю растворённого вещества w(B) обычно выражают в долях единицы или в процентах. Например, массовая доля растворённого вещества – CaCl2 в воде равна 0,06 или 6%. Это означает,что в растворе хлорида кальция массой 100 г содержится хлорид кальция массой 6 г и вода массой 94 г. Молярная концентрация C(B) показывает, сколько моль растворённого вещества содержится в 1 литре раствора. C(B) = n(B) / V = m(B) / (M(B) · V), где М(B) - молярная масса растворенного вещества г/моль. Молярная концентрация измеряется в моль/л и обозначается "M". Например, 2 M NaOH - двухмолярный раствор гидроксида натрия. Один литр такого раствора содержит 2 моль вещества или 80 г (M(NaOH) = 40 г/моль). Концентрацию раствора можно выразить количеством молей растворённого вещества в 1000 г растворителя. Такое выражение концентрации называют моляльностью раствора. Нормальность раствора обозначает число грамм-эквивалентов данного вещества в одном литре раствора или число миллиграмм-эквивалентов в одном миллилитре раствора. Грамм - эквивалентом вещества называется количество граммов вещества, численно равное его эквиваленту. Для сложных веществ - это количество вещества, соответствующее прямо или косвенно при химических превращениях 1 грамму водорода или 8 граммам кислорода. Эоснования = Моснования / число замещаемых в реакции гидроксильных групп Экислоты = Мкислоты / число замещаемых в реакции атомов водорода Эсоли = Мсоли / произведение числа катионов на его заряд Величины нормальности обозначают буквой "Н". Например, децинормальный раствор серной кислоты обозначают "0,1 Н раствор H2SO4". Так как нормальность может быть определена только для данной реакции, то в разных реакциях величина нормальности одного и того же раствора может оказаться неодинаковой. Так, одномолярный раствор H2SO4 будет однонормальным, когда он предназначается для реакции со щёлочью с образованием гидросульфата NaHSO4, и двухнормальным в реакции с образованием Na2SO4. Пересчет концентраций растворов из одних единиц в другие При пересчете процентной концентрации в молярную и наоборот, необходимо помнить, что процентная концентрация рассчитывается на определенную массу раствора, а молярная и нормальная - на объем, поэтому для пересчета необходимо знать плотность раствора. Если мы обозначим: с - процентная концентрация; M - молярная концентрация; N - нормальная концентрация; э - эквивалентная масса, r - плотность раствора; m - мольная масса, то формулы для пересчета из процентной концентрации будут следующими: M = (c · p · 10) / m N = (c · p · 10) / э Этими же формулами можно воспользоваться, если нужно пересчитать нормальную или молярную концентрацию на процентную. Пример Какова молярная и нормальная концентрация 12%-ного раствора серной кислоты, плотность которого р = 1,08 г/см3? Решение Мольная масса серной кислоты равна 98. Следовательно, m(H2SO4) = 98 и э(H2SO4) = 98 : 2 = 49. Подставляя необходимые значения в формулы, получим: а) Молярная концентрация 12% раствора серной кислоты равна M = (12 · 1,08 · 10) / 98 = 1,32 M б) Нормальная концентрация 12% раствора серной кислоты равна N = (12 ·1,08 ·10) / 49 = 2,64 H. Иногда в лабораторной практике приходится пересчитывать молярную концентрацию в нормальную и наоборот. Если эквивалентная масса вещества равна мольной массе (Например, для HCl, KCl, KOH), то нормальная концентрация равна молярной концентрации. Так, 1 н. раствор соляной кислоты будет одновременно 1 M раствором. Однако для большинства соединений эквивалентная масса не равна мольной и, следовательно, нормальная концентрация растворов этих веществ не равна молярной концентрации. Для пересчета из одной концентрации в другую можно использовать формулы: M = (N · Э) / m N = (M · m) / Э Пример Нормальная концентрация 1 М раствора серной кислоты N = (1 · 98) / 49 = 2 H. Пример Молярная концентрация 0,5 н. Na2CO3 M = (0,5· 53) / 106 = 0,25 M. Упаривание, разбавление, концентрирование, смешивание растворов Имеется mг исходного раствора с массовой долей растворенного вещества w1 и плотностью ρ1. Упаривание раствора В результате упаривания исходного раствора его масса уменьшилась на Dm г. Определить массовую долю раствора после упаривания w2 Решение Исходя из определения массовой доли, получим выражения для w1 и w2 (w2 > w1): w1 = m1 / m (где m1 – масса растворенного вещества в исходном растворе) m1 = w1·m w1 = m1 / (m – Dm) = (w1· m) / (m – Dm) Пример Упарили 60 г 5%-ного раствора сульфата меди до 50 г. Определите массовую долю соли в полученном растворе. m = 60 г; Dm = 60 – 50 = 10 г; w1 = 5% (или 0,05) w2 = (0,05 · 60) / (60 – 10) = 3 / 50 = 0,06 (или 6%-ный) Концентрирование раствора Какую массу вещества (X г) надо дополнительно растворить в исходном растворе, чтобы приготовить раствор с массовой долей растворенного вещества w2? Решение Исходя из определения массовой доли, составим выражение для w1 и w2: w1 = m1 / m2, (где m1 – масса вещества в исходном растворе). m1 = w1 · m w2 = (m1+x) / (m + x) = (w1 · m + x) / (m+x) Решая полученное уравнение относительно х получаем: w2 · m + w2 · x = w1 · m + x w2 · m – w1 · m = x – w2 · x (w2– w1 ) · m = (1 – w2 ) · x x = ((w2 – w1) · m) / (1 – w2 ) Пример Сколько граммов хлористого калия надо растворить в 90 г 8%-ного раствора этой соли, чтобы полученный раствор стал 10%-ным? m = 90 г w1 = 8% (или 0,08), w2 = 10% (или 0,1) x = ((0,1 – 0,08) ·90) / (1 – 0,1) = (0,02 · 90) / 0,9 = 2 г Смешивание растворов с разными концентрациями Смешали m1 граммов раствора №1 c массовой долей вещества w1 и m2 граммов раствора №2 c массовой долей вещества w2 . Образовался раствор (№3) с массовой долей растворенного вещества w3 . Как относятся друг к другу массы исходных растворов? Решение Пусть w1 > w2 , тогда w1 > w3 > w2 . Масса растворенного вещества в растворе №1 составляет w1 · m1, в растворе №2 – w2 · m2. Масса образовавшегося раствора (№3) – (m1 – m2). Сумма масс растворенного вещества в растворах №1 и №2 равна массе этого вещества в образовавшемся растворе (№3): w 1 · m1 + w 2 · m2 = w3· (m1 + m2) w1 · m1 + w 2 · m2 = w3 · m1 + w3 · m2 w 1 · m1 – w3 · m1 = w3 · m2 – w2 · m2 (w1– w3) · m1 = (w3– w2) · m2 m1 / m2 = (w3– w2 ) / (w1– w3) Таким образом, массы смешиваемых растворов m1 и m2 обратно пропорциональны разностям массовых долей w1 и w2 смешиваемых растворов и массовой доли смеси w3. (Правило смешивания). Для облегчения использования правила смешивания применяют правило креста : 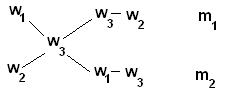 m1 / m2 = (w3 – w2) / (w1 – w3) Для этого по диагонали из большего значения концентрации вычитают меньшую, получают (w1 – w3), w1 > w3 и (w3 – w2), w3 > w2. Затем составляют отношение масс исходных растворов m1 / m2 и вычисляют. Пример Определите массы исходных растворов с массовыми долями гидроксида натрия 5% и 40%, если при их смешивании образовался раствор массой 210 г с массовой долей гидроксида натрия 10%. m1 / m2 = (w3 – w2) / (w1 – w3) Для этого по диагонали из большего значения концентрации вычитают меньшую, получают (w1 – w3), w1 > w3 и (w3 – w2), w3 > w2. Затем составляют отношение масс исходных растворов m1 / m2 и вычисляют. Пример Определите массы исходных растворов с массовыми долями гидроксида натрия 5% и 40%, если при их смешивании образовался раствор массой 210 г с массовой долей гидроксида натрия 10%. 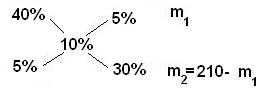 5 / 30 = m1 / (210 - m1) 1/6 = m1 / (210 – m1) 210 – m1 = 6m1 7m1 = 210 m1 =30 г; m2 = 210 – m1 = 210 – 30 = 180 г Разбавление раствора Исходя из определения массовой доли, получим выражения для значений массовых долей растворенного вещества в исходном растворе №1 (w1) и полученном растворе №2 (w2): w1 = m1 / (ρ1 · V1) откуда V1= m1 /( w1 ·ρ1) w2 = m2 / (ρ2 · V2) m2 = w2 ·ρ2 · V2 Раствор №2 получают, разбавляя раствор №1, поэтому m1 = m2. В формулу для V1 следует подставить выражение для m2. Тогда V1= (w2 ·ρ2 · V2) / (w1 · r1) m2 = w2 ·ρ2 · V2 или 5 / 30 = m1 / (210 - m1) 1/6 = m1 / (210 – m1) 210 – m1 = 6m1 7m1 = 210 m1 =30 г; m2 = 210 – m1 = 210 – 30 = 180 г Разбавление раствора Исходя из определения массовой доли, получим выражения для значений массовых долей растворенного вещества в исходном растворе №1 (w1) и полученном растворе №2 (w2): w1 = m1 / (ρ1 · V1) откуда V1= m1 /( w1 ·ρ1) w2 = m2 / (ρ2 · V2) m2 = w2 ·ρ2 · V2 Раствор №2 получают, разбавляя раствор №1, поэтому m1 = m2. В формулу для V1 следует подставить выражение для m2. Тогда V1= (w2 ·ρ2 · V2) / (w1 · r1) m2 = w2 ·ρ2 · V2 или
m1(раствор) / m2(раствор) = w2 / w1 При одном и том же количестве растворенного вещества массы растворов и их массовые доли обратно пропорциональны друг другу. Пример m1(раствор) / m2(раствор) = w2/ w1 |
