Реакции солей диазония с выделением азота
Соли диазония неустойчивы и способны распадаться гетеролитически в растворителях с высокой диэлектрической проницаемостью:
Ar - N+ºN X-  Ar+ + N2 + X-
Ar+ + N2 + X-
или гомолитически (как правило, под действием катализаторов):
Ar - N+ºN X-  Ar. + N2 + X.
Ar. + N2 + X.
Направление распада зависит от аниона соли диазония и растворителя. Гомолизу способствуют в основном анионы слабых кислот, но в неводных растворах таким образом распадаются даже хлориды. Растворители с высокой диэлектрической проницаемостью способствуют гетеролитическому распаду (общая закономерность).
Диазосоединения широко используются для замены диазогруппы в аренах на различные функциональные группы. Иногда это единственный метод получения нужного продукта.
Ниже приведены наиболее часто применяемые в лаборатории синтезы с применением диазосоединений. Около каждой реакции указывается, если это достоверно известно, по какому механизму она протекает: ГТЛ (гетеролитически) или ГМЛ (гомолитически).
Замещение диазониевой группы гидроксилом:
Ar-N+ºN + H2O 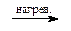 Ar-OH + N2 + H+ Ar-OH + N2 + H+ | (ГТЛ) |
2. Замещение диазогруппы на Cl, Br, CN и CNS (реакция Зандмейера). Осуществляется путем разложения соли диазония в присутствии соответствующих координационных соединений меди(I) ([CuCl4]3-, [CuBr4]3-, [Cu(CN)4]-, [Cu(CNS)4]3-):
Ar-N+ºN + X- 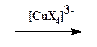 Ar-X + N2 Ar-X + N2 | (ГМЛ) |
Доказано, что этот процесс идет через промежуточное образование арильного радикала. Поставщиком электрона, необходимого для гомолитического разрыва связи С-N, является ион меди в степени окисления +1 (схематично):
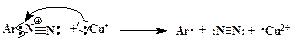
Далее ион Cu2+ вновь превращается в Сu+, забирая электрон у галогена, и радикал Х· образует ковалентную химическую связь с Ar·:
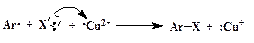
Таким образом, медь в реакции Зандмейера служит переносчиком электрона.
Образованием в промежуточной стадии арильных радикалов объясняется прохождение ряда побочных процессов при реакциях Зандмейера:
а) Образование диарилов:
Ar. + Ar.  Ar-Ar
Ar-Ar
б) Образование производных азобензола:
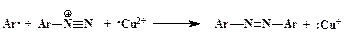
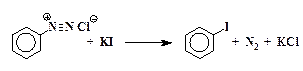
3. Замещение диазогруппы на иод непосредственно действием йодистого калия на водный раствор соли диазония без катализатора:
Ar-N+ºN + I-  Ar-I + N2
Ar-I + N2
В случае реакции с йодид-анионом катализатор не нужен, т.к. роль переносчика электрона способен выполнить сам иодид-ион.
4. Разложение сухого тетрафторбората диазония с образованием фторзамещенных:
[Ar-N+ºN] [BF4]-  Ar-F + BF3 + N2 Ar-F + BF3 + N2 | (ГТЛ) |
5. В ряде случаев диазогруппа может быть замещена на сульфохлоридную группу и нитрогруппу:
Ar-N+ºN Cl- + SO2 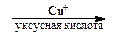 Ar-SO2Cl + N2
Ar-SO2Cl + N2
Ar-N+ºN SO4H- + NaNO2  Ar-NO2 + N2 + NaHSO4
Ar-NO2 + N2 + NaHSO4
6. Взаимодействие диазониев с полисульфидами щелочных металлов:
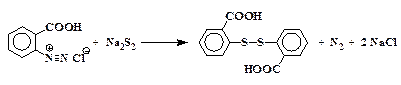
Запрещается применять эту реакцию к диазониям, не содержащим групп, сообщающих растворимость в щелочной среде (-ОН, -СООН, -SО3Н), так как в этом случае наблюдаются сильные взрывы.
Если при диазотировании ароматических аминов образуется нерастворимая в воде соль диазония (например, при диазотировании сульфаниловой кислоты), ее необходимо перерабатывать только во влажном виде из-за чрезвычайной взрывчатости высушенных диазосоединений. Воронку и фильтр, на которых производилось отсасывание диазония, следует немедленно обмыть водой.
Йодбензол
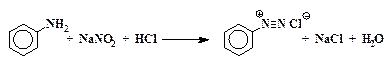
Диазотирование анилина. В стакане емкостью 100 мл смешивают 8,3 мл 38,3 % соляной кислоты с 10 мл воды и к раствору прибавляют 3,1 г свежеперегнанного анилина. Раствор охлаждают в бане со льдом до 1 – 2 °С и из капельной воронки при непрерывном перемешивании постепенно прибавляют раствор 2,3 г нитрита натрия в 6,5 мл воды. Температура реакционной смеси не должна превышать 5 °С. Для этого в реакционную смесь бросают кусочки льда. Окончание реакции диазотирования контролируют по йодкрахмальной бумажке. Избыток азотистой кислоты разрушают добавлением нескольких крупинок карбамида (мочевины) до прекращения выделения пузырьков газа.
Замещение диазогруппы на йод.Полученный раствор соли диазония медленно при перемешивании приливают к предварительно охлажденному в ледяной воде раствору 6,7 г иодида калия в 10 мл воды, находящемуся в колбе емкостью 500 мл. Смесь оставляют на 2 часа при комнатной температуре. Затем к колбе присоединяют воздушный холодильник и нагревают на кипящей водяной бане до прекращения выделения азота. Раствор охлаждают и приливают к нему концентрированный (30 %) раствор NаОН до сильнощелочной реакции. Отгоняют йодбензол с водяным паром. Перегонку ведут до прекращения выделения маслянистых капель йодбензола.
Йодбензол отделяют от воды с помощью делительной воронки и обезвоживают прокаленным хлористым кальцием. Перегоняют из маленькой колбы, собирая фракцию, кипящую при 185 – 189 °С. Выход 90 %. Ткип 188 °С, показатель преломления йодбензола nD20 = 1,6213.
Таким же способом можно получить из орто-толуидина орто-йодтолуол (Ткип 204 °С, nD20 = 1,609).
Пояснения к синтезу
Из-за низкой активности йода и обратимости процесса прямое йодирование бензола проходит медленно и дает низкий выход иодбензола:
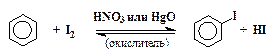
Окислитель выводит йодистый водород из сферы реакции и тем самым сдвигает равновесие вправо. Способ синтеза йодбензола с использованием соли диазония намного более удобен.
Необходимое для работы количество анилина следует перегнать непосредственно перед диазотированием на установке для микроперегонки (рис. 21, стр. 102). Для этого нужно взять 4 мл неочищенного анилина, а в перегонную колбочку вместе с анилином поместить небольшое количество цинковой пыли.
Разложение соли фенилдиазония в водном растворе йодистого калия проводят при очень медленном повышении температуры для того, чтобы замедлить побочную реакцию соли диазония с водой. Образующийся в качестве побочного продукта фенол связывают в неперегоняющийся фенолят натрия путем добавления в реакционную смесь щелочи:
Йодбензол и о-йодтолуол представляют собой очень тяжелые по сравнению с водой (плотность йодбензола 1,835) бесцветные жидкости с высокими показателями преломления. Это – характерные свойства галоген- и особенно йодпроизводных.
Контрольные вопросы по работе см. на стр. 147.
2.4.3. п-Йоднитробензол
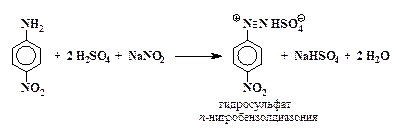
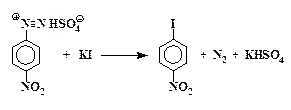
Диазотирование п-нитроанилина. В конической колбе при нагревании растворяют 2,5 г п-нитроанилина в смеси 3 мл концентрированной серной кислоты с 30 мл воды. Смесь быстро охлаждают до
5 – 10° С и к ней постепенно при постоянном перемешивании в течение 30 мин прибавляют раствор 1,5 г нитрита натрия в 7,5 мл воды. Температура реакционной массы при этом не должна превышать 10 °С. Конец реакции диазотирования определяют пробой с иодокрахмальной бумажкой.
Холодную реакционную смесь фильтруют через складчатый фильтр. К фильтрату прибавляют небольшое количество карбамида (мочевины) до прекращения выделения пузырьков газа. Добавка карбамида требуется для разложения некоторого избытка азотистой кислоты. Фильтрату не дают при этом нагреваться выше 10 °С.
Разложение соли диазония. Холодный фильтрат, представляющий собой раствор гидросульфата п-нитробензолдиазония, постепенно при размешивании прибавляют к охлажденному раствору 5 г йодистого калия в 30 мл воды, находящемуся в стакане или конической колбе емкостью не менее 500 мл. Происходит бурное выделение азота, смесь при этом сильно пенится. Выпавший осадок отфильтровывают на воронке Бюхнера, промывают водой и высушивают. Выход 90 %.
Берут 1/5 часть сухого осадка (по весу) и перекристаллизовывают ено из спирта. Определяют температуру плавления перекристаллизованного продукта. Тпл 174° С. Рассчитывают выход неочищенного продукта и долю потерь при его перекристаллизации (в %).
Пояснения к синтезу
При низкой температуре растворимость и скорость растворения п-нитроанилина в 15 % серной кислоте мала, поэтому растворение проводят при нагревании. Затем раствор резко охлаждают, и в осадок выпадает мелкокристаллическая соль амина. В растворе при этом находится равновесная смесь свободного амина и его соли. Диазотированию подвергается только свободный амин, реагирующий относительно быстро. По мере расходования амина его содержание пополняется за счет разложения растворенной соли. Таким образом, скорость суммарного процесса диазотирования определяется скоростью растворения гидросульфата п-нитроанилиния. А она тем выше, чем меньше размеры кристаллов. Тем не менее, раствор нитрита к реакционной смеси следует добавлять медленно (7,5 мл за 30 мин).
Гидросульфат п-нитробензолдиазония, как и большинство других солей диазония, хорошо растворим в воде и разбавленных растворах кислот. Поэтому при правильном проведении процесса реакционная смесь к окончанию диазотирования будет однородным раствором желтоватого цвета. Если смесь в конце реакции представляет собой не раствор, а суспензию, это означает, что нитрит добавляли слишком быстро. Часть п-нитроанилина, не успев продиазотироваться, выпала в осадок из-за разбавления кислоты водой, добавленной вместе с нитритом. (С уменьшением концентрации кислоты растворимость амина падает). В этом случае раствор соли диазония нужно быстро отфильтровать, а лишь затем разлагать в присутствии иодистого калия. Избыток азотистой кислоты в растворе следует убрать, добавив к нему небольшое количество мочевины до прекращения выделения пузырьков газа. Иначе азотистая кислота окислит йодистый калий с выделением свободного йода, что приведет к загрязнению продукта.
Следует соблюдать осторожность при разложении соли n-нитрофенилдиазония в присутствии йодистого калия. Раствор КI перед прибавлением к нему соли диазония обязательно должен быть охлажден в ледяной воде.
Контрольные вопросы по работе см. на стр. 147.
