Названия и формулы некоторых кислот и кислотных остатков
| Формула кислоты | Название кислоты | Кислотный остаток | Название кислотного остатка |
| Бескислородные кислоты | |||
| HF | фтороводородная | F– | фторид-ион |
| HCl | хлороводородная (соляная) | Cl– | хлорид - ион |
| HBr | бромоводородная | Br– | бромид-ион |
| HI | йодоводородная | I– | йодид-ион |
| НСN | циановодородная | СN– | цианид-ион |
| H2S | сероводородная | S2– | сульфид-ион |
| HS– | гидросульфид-ион | ||
| Кислородсодержащие кислоты | |||
| HClO | хлорноватистая | ClO– | гипохлорит-ион |
| HClO2 | хлористая | СlO2− | хлорит-ион |
| HClO3 | хлорноватая | СlO3− | хлорат-ион |
| HClO4 | хлорная | СlO4− | перхлорат-ион |
| H2SO3 | сернистая | HSO3− | гидросульфит-ион |
| SO32− | сульфит-ион | ||
| H2SO4 | серная | HSO4− | гидросульфат-ион |
| SO42− | сульфат-ион | ||
| HNO2 | азотистая | NO2− | нитрит-ион |
| HNO3 | азотная | NO3− | нитрат-ион |
| H3PO4 | ортофосфорная | H2PO3− | дигидрофосфат-ион |
| HPO32− | гидрофосфат-ион | ||
| PO43− | ортофосфат-ион | ||
| H2CO3 | угольная | HCO3− | гидрокарбонат-ион |
| CO32− | карбонат-ион | ||
| H2SiO3 | метакремниевая | SiO32− | силикат-ион |
| H3BO3 | борная (ортоборная) | BO33− | борат-ион |
| H2CrO4 | хромовая | CrO42− | хромат-ион |
| H2Cr2O7 | дихромовая | Cr2O72− | дихромат-ион |
| HMnO4 | марганцовая | MnO4– | перманганат-ион |
| H2MnO4 | марганцовистая | MnO42– | манганат-ион |
Al(OH)3, Fe(OH)3, Sn(OH)4 и др.
Важнейшие химические свойства гидроксидов (оснований, кислот и амфолитов) представлены в таблице 11.
Соли
Соли – это сложные вещества, молекулы которых состоят из катионов металла (или аммония NH4+) и кислотного остатка. Их можно рассматривать как продукты частичного или полного замещения атомов водорода в кислоте на металл (или NH4+) или гидроксильных групп в основании на кислотные остатки. Различают средние, кислые основные соли (схема 3).
Средние (нормальные) соли – продукты полного замещения атомов водорода в кислотах на катион металла (или NH4+) или гидроксильных групп в основаниях на кислотный остаток. Например, Na2CO3, K2SO4, Ca3(PO4)2. Средние соли образуют все кислоты: как одно-, так и многоосновные. Уравнения диссоциации средних солей можно записать:
K3PO4 ® 3K+ + PO43-
NH4Cl ® NH4+ + Cl-
Таблица 11
Важнейшие химические свойства гидроксидов
| Основные гидроксиды | Кислотные гидроксиды |
1.Отношение к нагреванию: Основание 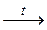 Основный оксид + Н2О Ba(OH)2 Основный оксид + Н2О Ba(OH)2 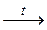 BaO + H2O 2.Основание + Кислотный оксид → Соль + H2O: Ba(OH)2 + СО2 → BaСО3 + Н2О NaOH(разб.) + SO2 → NaHSO3 3.Щёлочь + растворимая соль → малодиссоциируемое соединение: 3NaOH(разб.) + AlCl3 → Al(OH)3↓ + 3NaCl 2KOH(разб.) + 2AgNO3 → Ag2O↓ + H2O + 2KNO3 4.Основание + неметалл → Соль 2Ca(OH)2(хол.) + 2Cl2 → Ca(ClO)2 + CaCl2 + 2H2O суспензия 3КОН + 4Р + 3H2O BaO + H2O 2.Основание + Кислотный оксид → Соль + H2O: Ba(OH)2 + СО2 → BaСО3 + Н2О NaOH(разб.) + SO2 → NaHSO3 3.Щёлочь + растворимая соль → малодиссоциируемое соединение: 3NaOH(разб.) + AlCl3 → Al(OH)3↓ + 3NaCl 2KOH(разб.) + 2AgNO3 → Ag2O↓ + H2O + 2KNO3 4.Основание + неметалл → Соль 2Ca(OH)2(хол.) + 2Cl2 → Ca(ClO)2 + CaCl2 + 2H2O суспензия 3КОН + 4Р + 3H2O 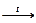 РН3↑ + 3КН2РО2 5.Щёлочь + Амфотерный металл +Н2О → Соль + Н2↑ 3NaOH(разб.) + Zn + 2Н2О → Na2[Zn(OH)4] + Н2↑ 6.Водный раствор щелочи изменяет окраску индикатора: лакмуса – в синий фенолфталеина – в малиновый метилоранжа – в жёлтый РН3↑ + 3КН2РО2 5.Щёлочь + Амфотерный металл +Н2О → Соль + Н2↑ 3NaOH(разб.) + Zn + 2Н2О → Na2[Zn(OH)4] + Н2↑ 6.Водный раствор щелочи изменяет окраску индикатора: лакмуса – в синий фенолфталеина – в малиновый метилоранжа – в жёлтый | 1.Термически неустойчивые кислоты разлагаются при комнатной температуре или при лёгком нагревании: Н2СО3 → СО2↑ + Н2О Н2SО3 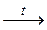 SО2↑ + Н2О↑ 2.Кислота + Осн. (амф.) оксид → Соль + Н2О: 2H3PO4(разб.) + 3СаО → Са3(РО4)2↓ + 3Н2О 2HNO3 + ZnO → Zn(NO3)2 + Н2О 3.а)Кислота-окислитель + соль, содержащая анион, проявляющий восстановительные свойства: 8NaI + 5H2SO4(конц.)→ 4I2↓ + H2S↑ +4Na2SO4 +4H2O б) Кислота + Соль → Соль + Кислота Na2SO3 + H2SO4 → Na2SO4 + SO2↑ + H2O BaCl2 + H2SO4 → BaSO4↓ + 2HCl 4.Кислота + неметалл: С + 2H2SO4(конц.) SО2↑ + Н2О↑ 2.Кислота + Осн. (амф.) оксид → Соль + Н2О: 2H3PO4(разб.) + 3СаО → Са3(РО4)2↓ + 3Н2О 2HNO3 + ZnO → Zn(NO3)2 + Н2О 3.а)Кислота-окислитель + соль, содержащая анион, проявляющий восстановительные свойства: 8NaI + 5H2SO4(конц.)→ 4I2↓ + H2S↑ +4Na2SO4 +4H2O б) Кислота + Соль → Соль + Кислота Na2SO3 + H2SO4 → Na2SO4 + SO2↑ + H2O BaCl2 + H2SO4 → BaSO4↓ + 2HCl 4.Кислота + неметалл: С + 2H2SO4(конц.) 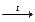 СО2↑ + 2SO2↑ + 2H2O S + 2HNO3(конц.) СО2↑ + 2SO2↑ + 2H2O S + 2HNO3(конц.) 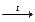 H2SO4 + 2NO↑ 5.Кислота (не сильный окислитель) + металл (стоящий в электрохимическом ряду напряжений до водорода)→ Cоль + Н2↑: H2SO4(разб.) + Zn → ZnSO4 + H2↑ 2HCl + Mg → MgCl2 + H2↑ 6.Водный раствор кислоты изменяет окраску индикатора: лакмуса – в красный фенолфталеина – бесцветный метилоранжа – в красный H2SO4 + 2NO↑ 5.Кислота (не сильный окислитель) + металл (стоящий в электрохимическом ряду напряжений до водорода)→ Cоль + Н2↑: H2SO4(разб.) + Zn → ZnSO4 + H2↑ 2HCl + Mg → MgCl2 + H2↑ 6.Водный раствор кислоты изменяет окраску индикатора: лакмуса – в красный фенолфталеина – бесцветный метилоранжа – в красный |
| 3.Основание + Кислота → Соль + Н2О 2NaOH + H2SO4 → Na2SO4 + 2H2O NaOH(разб.) + Н2СО3 → NaНСО3 + Н2О | |
| Окончание таблицы 11 | |
Амфотерные гидроксиды 1.Отношение к нагреванию: Амфотерный гидроксид 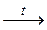 Амфотерный оксид + Н2О Pb(OH)2 Амфотерный оксид + Н2О Pb(OH)2 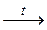 PbO + H2O PbO + H2O | |
| 1.Амф. гидроксид + Кисл. оксид → Соль + Н2О 2Be(OH)2 + 2CO2 → Be2CO3(OH)2↓ + H2O 2.Амф. гидроксид + Кислота → Соль + Н2О Zn(OH)2 + 2HCl → ZnCl2 + H2O | 1.Амф. гидроксид + Осн. оксид → Соль + Н2О Al2O3 + 2NaOH(конц.,гор.) + 3H2O → 2Na[Al(OH)4] 2.Амф. гидроксид + Основание → Соль + Н2О Ga(OH)3 + NaOH 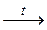 NaGaO2 + 2H2O Ga(OH)3 + NaOH(конц.,гор.) → Na[Ga(OH)4] NaGaO2 + 2H2O Ga(OH)3 + NaOH(конц.,гор.) → Na[Ga(OH)4] |
Кислые соли (гидросоли) – продукты неполного замещения атомов водорода в молекулах многоосновных кислот ионами металлов. Их образуют только многоосновные кислоты. Например, NaHCO3, Ca(H2PO4)2, KHSO3. Диссоциацию кислой соли можно выразить уравнениями:
NaHCO3 ® Na+ + HCO3-
HCO3- « H+ + CO32-
Основные соли (гидроксосоли) – продукты неполного замещения гидроксогрупп в основаниях на кислотные остатки. Основные соли образуются только многокислотными основаниями. Например, (СuOH)2CO3, AlOH(NO3)2, FeOHCl. Диссоциация основной соли выражается уравнениями:
МgOHCl ® МgOH+ +Cl-
МgOH+ « Мg2+ + OH-
Формула соли строится с учетом валентностей металла и кислотного остатка. Практически все соли – ионные соединения, поэтому можно говорить, что в солях связанных между собой ионы металла и ионы кислотных остатков:
Na+Cl– – хлорид натрия
Ca2+SO42– – сульфат кальция
Названия солей составляются из названия кислотного остатка и названия металла. Главным в названии является кислотный остаток. Названия солей в зависимости от кислотного остатка показаны в таблице 12.
Таблица 12
Построение названий солей
| Кислота | Кислотный остаток | Валентность остатка | Название солей | Примеры |
| Азотная, HNO3 | NO3– | I | нитраты | Ca(NO3)2 нитрат кальция |
| Кремниевая, H2SiO3 | SiO32– | II | силикаты | Na2SiO3 силикат натрия |
| Серная, H2SO4 | SO42– | II | сульфаты | PbSO4 сульфат свинца |
| Угольная, H2CO3 | CO32– | II | карбонаты | Na2CO3 карбонат натрия |
| Фосфорная, H3PO4 | PO43– | III | фосфаты | AlPO4 фосфат алюминия |
| Бромоводородная, HBr | Br – | I | бромиды | NaBr бромид натрия |
| Иодоводородная, HI | I – | I | иодиды | KI иодид калия |
| Сероводородная, H2S | S2– | II | сульфиды | FeS сульфид железа (II) |
| Хлороводородная, HCl | Cl – | I | хлориды | NH4Cl хлорид аммония |
| Фтороводородная, HF | F – | I | фториды | CaF2 фторид кальция |
В таблице 13 приведены международные названия солей. Однако полезно знать также русские названия и некоторые исторически сложившиеся, традиционные названия солей, имеющих практическое значение.
Важнейшие химические свойства солей
1.Соли взаимодействуют с кислотами и щелочами (см. выше).
2.При взаимодействии двух растворимых в воде солей образуются две новые соли, одна из которых должна выпадать в осадок:
Ba(NO3)2 + K2SO4®2KNO3 + BaSO4¯
3.Реакция металла с солью менее активного металла приводит к образованию соли и металла:
Fe + CuSO4 ® FeSO4 + Cu
реакции в виде осадка (иногда – в виде газа), то при смешивании растворов образуется только смесь ионов, на которые при растворении распадаются исходная соль и реагент.
Таблица 13
