Иницирование химической реакции. Катализ. Сущность гомогенного и гетерогенного катализа.
Изменение скорости реакции под действием катализаторов - катализ. Положительный (просто катализ) и антикатализ. При катализе скорость реакции увеличивается, при антикатализе - уменьшается. В-ва., увеличивающие скорость реакции - катализаторы, уменьшающие - ингибиторы. Как правило катализатор при реакции не расходуется, ингибитор расходуется. Автокатализ - в роли катализатора - продукты реакции. Прим. FeO+H2=Fe+H2O
Использование катализатора не отражается на величине изменения свободной энергии системы. Нельзя увеичить выход продуктов реакции. К сожалению, катализаторам присуща определенная избирательность. Катализатор ищут методом подбора. Этанол с разными катализаторами:
А) порошок 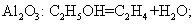
Б) порошок Cu или Ag: 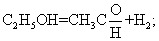
В) 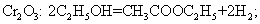
Г) 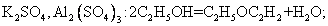
Д) оксидный катализатор С.В.Лебедева: 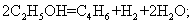
Различают гомогенный и гетерогенный катализ. А(г)+В(г)+Кат(г) - гомогенный - 1 фаза.
Ускорительное действие катализатора пропорционально его общему количеству.
Гетерогенный катализ. А(г)+В(г)+Кат(т) в различных фазах (часто газ и тв. в-во)
Ускорение катализа определяется состоянием поверхности катализатора.
Гомогенный катализ. Действие катализатора пропорционально его общему количеству. А+В=АВ (в газовой фазе), Е, не большая скорость. 1) А+Кат=АКат, Е1 ; 2) АКат+В=АВ+Кат, Е2; Е1<<Е, Е2<<Е Уменьшение энергии активации. Снижение потенциального барьера. ; NH3=1/2*N2+3/2*H2 E~=300кДж/моль
W E'~=160 кДж/моль 2so2+o2=2so3, NO (Суммарная реакция + еще две)
Катализатор не расходуется, происходит только чисто механический унос.
Гетерогенный катализ. При Г. катализе реагирующие в-ва и катализатор находятся в разных фазах. А(г)+В(г)+Кат(т) При Г. кат. нужно учитывать адсорбционную способность катализатора, поверхность, наличие активных центров, их геометрический рисунок, расстояние между активными центрами, соотношение между активными молекулами и многое другое. Иногда порошкообразный гетерогенный кат. вызывает мгновенное ускорение реакции. (пример: реакция разложения h2o2 на воду и кислород с катализатором MnO2) .Электронно-химическая теория Рогинского. АВ+CD=AC+BD
Молекулы адсорбируются на поверхности кат. Ослабевают внутримолекулярные связи, т.е. молекула перешла в возбужденное состояние. Теория мультиплетов (Баландин) Доказано, что работает не вся поверхность кат., а только ее активные центры. Каталитические яды - As,P, C2H2, O2, цианиды... Небольшое количество кат. ядов отравляет огромные поверхности катализатора. Согласно теории мультиплетов, катализируемая молекула должна расположиться определенным образом на поверхности кат. вблизи активных центров. (см. рисунки+ формулы) В некоторых случаях требуется определенное расположение молекул(ы) между 4-6 центрами. СУТЬ КАТАЛИЗА - снижение энергии активации.
Антикатализ (торможение коррозии) (вып. ингибиторами) Механизм действия: ингибитор нейтрализует действие (+)кат., если реакция протекает по цепной реакции, то разрывает цепи. Ингибитор может адсобрироваться на поверхности, препятствуя взаимодействию веществ.
