Электролиз и поляризация. Поляризация. Перенапряжение
ПОЛЯРИЗАЦИЯ в электрохимии, отклонение значения электродного потенциала от равновесного при пропускании электрич. тока. Величина поляризации зависит от плотности тока i, т.е. силы тока, отнесенной к единице пов-сти электрода, и обычно тем больше, чем больше i. При одном и том же значении i поляризация зависит от природы электрода и типа протекающей на его пов-сти р-ции, состава р-ра, т-ры и др. факторов и может колебаться от долей мВ до неск. В. Знак поляризации зависит от направления протекания тока и при изменении направления меняется на обратный.
Причиной поляризации служит малая скорость одной или нескольких стадий суммарного электродного процесса. Если лимитирующей стадией является подвод реагирующего в-ва к пов-сти электрода, поляризация обусловлена тем, что из-за протекания тока концентрация cs в-ва у пов-сти отличается от объемной концентрации сu (концентрационная поляризация). В простейшем случае разряда ионов металла на электроде из того жеметалла или анодного растворения металла концентрационная поляризация |DE| = [RT/nF]ln(cs/сu), где n-число электронов, участвующих вэлектродном процессе, T-т-ра, F- постоянная Фарадея, R - газовая постоянная. При катодном осаждении металла DЕ < 0, при анодном растворении металла DЕ > С. Связь между величинами DЕ и i может быть выражена в виде:
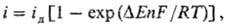
где iд - предельный диффузионный ток, отвечающий условию cs = 0. Из этого ур-ния следует, что при |DЕ| 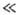 RT/nF зависимость между i и DЕ линейна. При больших отрицат. DЕ примерно i = iд, а при больших положит. DЕ (анодное растворение металла) i экспоненциально возрастает с ростом DЕ.
RT/nF зависимость между i и DЕ линейна. При больших отрицат. DЕ примерно i = iд, а при больших положит. DЕ (анодное растворение металла) i экспоненциально возрастает с ростом DЕ.
Перенапряжение электрохимическое, отклонение электродного потенциала от его равновесного (по отношению к приэлектродному составураствора) термодинамического значения при поляризации электрода внешним током. При заметном удалении от равновесия перенапряжение (h) и плотность поляризующего тока (i) обычно связаны соотношением h = а + b lg i (уравнение Тафеля), где а и b — эмпирические постоянные. Перенапряжение зависит от температуры, природы электродного материала и состава раствора. Перенапряжение необходимо для ускорения нужной электродной реакции. Если скорость электродной реакции в целом определяется скоростью собственно электрохимической стадии, связанной с переносом заряда, то перенапряжение усиливает электрическое поле, действующее на разряжающиеся частицы, благодаря чему снижается энергия активации разряда. Поскольку электрическое поле в значительной степени обусловлено строением двойного электрического слоя, перенапряжение оказывается зависящим от концентрации постороннего электролита и адсорбирующихся веществ, влияющих на распределение потенциала в двойном слое. На повышении перенапряжения основано действие многих ингибиторов коррозии металлов (см.Ингибиторы химические), что является одной из положительных сторон перенапряжения. В то же время перенапряжение в промышленномэлектролизе, неизбежно связанное с дополнительным расходом энергии, приводит к увеличению себестоимости продукции.
