В группах главных подгрупп металлические свойства элементов увеличиваются, а неметаллические свойства уменьшаются с возрастанием порядкового номера элемента.
Энергия ионизации. Наиболее характерным химическим свойством металлов является способность их атомов легко отдавать валентные электроны и превращаться в положительно заряженные ионы. Количественно эта способность может быть оценена энергией ионизации атома(J).
Энергия ионизации − это энергия, которую нужно затратить для отрыва электрона от невозбужденного атома (Эо) для превращения его в положительно заряженный ион (Э+):
Эо+J=Э++ 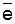
Энергию ионизации выражают либо в килоджоулях на моль (кДж/моль), либо в электронвольтах (эВ).
Для моноэлектронных атомов энергия ионизации J1, J2, J3, ... Jn соответствует отрыву 1−го, 2−го и т.д. электронов. При этом J1<J2<J3...<Jn, так как увеличение числа оторванных электронов приводит к возрастанию положительного заряда образующегося иона.
В группах энергия ионизации уменьшается по мере возрастания расстояния электрона от ядра и увеличения размера атомов, т.е. сверху вниз металлические свойства усиливаются.
В периодах слева направо энергия ионизации увеличивается с увеличением заряда ядра атома и с уменьшением их радиусов, т.е. металлические свойства в периоде слева направо ослабевают. У d - элементов энергия ионизации сравнительно мало изменяется при переходе от одного элемента к другому
Сродство к электрону. Неметаллы характеризуются способностью присоединять электроны с образованием отрицательных ионов, выделяющаяся при этом энергия называется сродством к электрону (F):
Эо+ 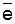 =Э−+F.
=Э−+F.
У неметаллов тем больше энергия сродства к электрону, чем ближе элемент находится к концу периода, т.е. неметаллические свойства в периоде слева направо усиливаются.
В группах сверху вниз энергия сродства к электрону уменьшается и неметаллические свойства соответственно ослабевают.
Электроотрицательность. Так как атомы многих элементов могут и отдавать, и принимать электроны, то их химические свойства определяются полусуммой энергии сродства к электрону и энергии ионизации. Эта величина называется электроотрицательностью (ЭО):
ЭО=½ (J + F).
Электроотрицательность увеличивается в периодах слева направо и уменьшается в группах сверху вниз.
Таким образом, самыми электроотрицательными элементами в ПС являются типичные неметаллы (элементы VII A подгруппы). Часто для удобства пользуются величиной относительной электроотрицательности (ОЭО). Значения ОЭО элементов главных подгрупп периодической системы приведены в табл. 1.2.
Таблица 1.2
Относительная электроотрицательность атомов
| Н | ||||||
| 2,1 | ||||||
| Li | Be | В | С | N | О | F |
| 0,98 | 1,5 | 2,0 | 2,5 | 3,07 | 3,5 | 4,0 |
| Na | Mg | Al | Si | P | S | CI |
| 0,93 | 1,2 | 1,6 | 1,9 | 2,2 | 2,6 | 3,0 |
| К | Ca | Ga | Ge | As 2,1 | Se | Br |
| 0,91 | 1,04 | 1,8 | 2,0 | 2,5 | 2,8 | |
| Rb | Sr | In | Sn | Sb | Те | J |
| 0,89 | 0,99 | 1,5 | 1,7 | 1,8 | 2,1 | 2,6 |
