Влияние концентрации реагирующих веществ на смещение химического равновесия
| № пробирки | Добавляемый реагент | Наблюдаемые визуальные изменения | Характер смещения химического равновесия |
?Напишите математическое выражение константы равновесия для реакции взаимодействия хлорида железа и роданида калия:
Кравнов = ________________________________________________
? Сформулируйте вывод о смещении химического равновесия при изменении концентрации реагирующих веществ с позиций принципа Ле-Шателье. Предложите иные способы смещения химического равновесия.
__________________________________________________________
__________________________________________________________
__________________________________________________________
__________________________________________________________
__________________________________________________________
__________________________________________________________
__________________________________________________________
Вопросы для подготовки к блиц-опросу
1. Как математически выразить скорость химической реакции?
2. В чем сущность закона действия масс?
3. Как математически записать закон действия масс для гомогенной и гетерогенной реакции? (Приведите примеры)
4. Какие факторы влияют на скорость реакции?
5. В чем сущность правила Вант-Гоффа?
6. Как математически записать правило Вант-Гоффа?
7. Что такое энергия активации?
8. В чем сущность принципа Ле-Шателье?
9. Какие факторы и каким образом влияют на смещение химического равновесия?
10. Что такое константа равновесия? (Приведите пример)
Таблица 4.4
Результаты оценивания лабораторной работы
| № п/п | Критерий оценивания | Кол-во баллов | |
| максимальное | фактическое | ||
| Правильно проведенный ход работы | 0,5 | ||
| Правильное написание уравнений реакций | 0,5 | ||
| Правильно выполненные расчеты | 0,5 | ||
| Правильно сделанный вывод по работе | 0,5 | ||
| Правильные ответы на вопросы по работе | |||
| ИТОГО |
_____________________ ________________
(подпись преподавателя) (дата)
_____________________ ________________
(подпись студента) (дата)
ЛАБОРАТОРНАЯ РАБОТА № 5
Тема: Приготовление растворов
Amp;Тезаурус темы
Дисперсные системы – это гетерогенные системы, в которых одно вещество в виде очень мелких частиц равномерно распределено в объеме другого.
Растворы –это многокомпонентные гомогенные системы переменного состава (размер частиц менее 10-7 см).
Кристаллогидраты –это вещества, содержащие в своей структуре воду.
Массовая доля (ω) –это масса растворенного вещества (mраст.в-ва), деленная на массу раствора (mр-ра):

Мольная доля (χ) –это количество моль растворенного вещества (νраст.в-ва), деленное на количество моль раствора (νр-ра):

Объемная доля (φ) –это объем растворенного вещества (Vраст.в-ва), деленный на объем раствора (Vр-ра):

Молярность (с) –это количество моль вещества (νраст.в-ва) в 1 литре раствора (Vр-ра):

Моляльность (m)– это количество моль вещества (νраст.в-ва) в 1 кг (1000 г) растворителя (mр-ля):

Нормальность (N) – это количество моль эквивалентов вещества (νэкв(раст.в-ва)) в 1 литре раствора (Vр-ра):
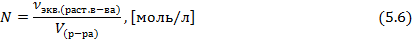
Титр (Т) –это масса вещества (mраст.в-ва) в объеме раствора (Vр-ра):

MЭкспериментальная часть
ОПЫТ № 1. Приготовление раствора заданной процентной концентрации
Реактивы
Хлорид натрия (кристаллический), сульфат натрия (кристаллический), нитрат натрия (кристаллический), сульфат аммония (кристаллический), хлорид аммония (кристаллический), хлорид калия (кристаллический).
Оборудование
Весы электронные, химический стакан, мерный цилиндр, ареометр.
Ход работы
? Произвести расчет массы вещества и воды для приготовления раствора одной из указанных солей заданной процентной концентрации, которую укажет преподаватель:
______________________________________________________________
______________________________________________________________
______________________________________________________________
______________________________________________________________
______________________________________________________________
______________________________________________________________
______________________________________________________________
______________________________________________________________
______________________________________________________________
______________________________________________________________
______________________________________________________________
1. Взвесить рассчитанную навеску вещества, раствор которого требуется приготовить, перенести ее в стакан. Мерным цилиндром отмерить расчетное количество воды и перелить ее в стакан с навеской вещества. Раствор перемешать до полного растворения соли.
2. Точность концентрации приготовленного раствора проверить по плотности, измерив ее с помощью ареометра. Для этого перелить приготовленный раствор в цилиндр и погрузить в него ареометр.
3. По измеренной фактической плотности в справочнике (спросить у преподавателя) найти фактическую процентную концентрацию раствора.
? Заполните табл. 5.1.
Таблица 5.1
