Задания для самостоятельной работы. Определение кинетических характеристик реакции окисления иодид-ионов пероксидом водорода
3.67: 3.70; 3.83; 3.91; 3.97; 3.111
Дата _______
Лабораторная работа 4.1
Определение кинетических характеристик реакции окисления иодид-ионов пероксидом водорода. Влияние катализатора на скорость реакции.
Цель работы. Изучить влияние катализатора и температуры на скорость реакции окисления иодид-ионов пероксидом водорода в кислой среде.
Задание:Определить константу скорости реакции оксиления иодид-ионов пероксидом водорода в кислой среде в присутствии катализатора.
Оборудование и реактивы. Секундомер, бюретка, воронка, мерный цилиндр вместимостью 50 мл, мерная пробирка вместимостью 10 мл, коническая колба вместимостью 250 мл, капельницы, термометр, водяная баня. Растворы пероксида водорода, иодида калия, тиосульфата натрия, серной кислоты, молибдата аммония, сульфата меди, крахмала.
Сущность работы.См. лабораторную работу к занятию 01-02.
Катализаторы ускоряют только термодинамически возможные реакции. Механизм действия катализатора заключается в изменении пути процесса.
ВНИМАНИЕ! В работе используются два раствора катализатора: разбавленный (0,0025 моль/л) для проведения кинетических измерений Vt и t; концентрированный (0,5 моль/л) – для проведения реакции до конца и определения Vо.
Ход работы.Работу проводят аналогично описанному в занятии 01-02 с той лишь разницей, что при изучении влияния катализатора на скорость химической реакции в реакционную смесь до добавления пероксида водорода вводят рекомендуемое преподавателем количество катализатора, а при изучении влияния температуры на скорость химической реакции, колбу с реакционной смесью до добавления пероксида водорода помещают на водяную баню и пероксид водорода добавляют по достижении реакционной смесью требуемой температуры. Дальнейшие измерения проводят не вынимая колбу из водяной бани. При этом необходимо следить за постоянством температуры во время всего эксперимента.
Экспериментальные данные
| V, мл | Катализатор | Vо = | ||||
| Показания секундомера (текущее время) | t , с | Константа скорости k , с-1 | ||||
| - | ||||||
| kср = | ||||||
Обработка результатов эксперимента.Для расчета константы скорости реакции (k) используют формулу: 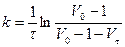 , где Vt – объем раствора тиосульфата натрия, добавленный к моменту времени t.
, где Vt – объем раствора тиосульфата натрия, добавленный к моменту времени t.
Константу скорости рассчитывают для всех проведенных измерений и вычисляют ее среднее значение (kср ).
Энергию активации Еа каталитической реакции рассчитывают по формуле:
kкаталит
Еа каталитической р. - Еа некаталитической р. = ΔЕа = RT ln- -----------
k некаталит
Расчеты
* В выводах указывают полученные значения константы скорости и энергии активации каталитической реакции.
Вывод
Дата __________ Занятие ____________
МОДУЛЬ 04. Свойства растворов
Задания для самостоятельной работы
4.59; 4.64; 4.68; 4.70; 4.72; 4.77
Дата _______
Лабораторная работа 5.1
