Сульфирование хлорсульфоновой кислотой
Важное место среди сульфирующих агентов занимает хлорсульфоновая кислота. Применение этого реагента позволяет получать в зависимости от условий проведения процесса либо сульфокислоты, либо их хлорангидриды (сульфохлориды).
Доказано, что хлорсульфоновая кислота является полухлорангидридом серной кислоты и соответствует формуле:
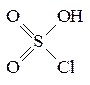
хотя ранее некоторые исследователи рассматривали её как комплексное соединение триоксида серы и хлорида водорода SO3.HCl. Температура плавления хлорсульфоновой кислоты (-80)°С, температура кипения 155°С (с разл.). Хлорсульфоновая кислота является более сильной кислотой, чем серная. Следует считать, что при сульфировании хлорсульфоновой кислотой имеет место взаимодействие субстрата не только с серным ангидридом:
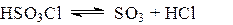
но и с катионом HSO3Å
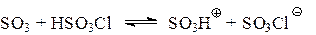
Последнее можно рассматривать как кислотно-катализируемое сульфирование SO3.
Хлорсульфоновая кислота бурно реагирует с водой, образуя H2SO4 и HCl. Тепловой эффект такого взаимодействия велик, так как складывается из теплового эффекта трёх экзотермических реакций: образования H2SO4 и HCl и взаимодействия последних с водой. В связи с этим хлорсульфоновая кислота является опасным реагентом: она вызывает ожоги кожи и тяжёлые поражения дыхательных путей.
При проведении реакции сульфирования в среде хлорсульфоновой кислоты последняя выступает как очень сильный сульфирующий агент, так как образование SO3 за счёт диссоциации HSO3Cl проходит очень легко и концентрация триоксида серы высока, и дополнительно образующийся HSO3Å является более активным реагентом, чем SO3. При сульфировании в инертных растворителях сульфирование должно идти в основном по пиросульфатному механизму, а при сульфировании в среде эфира и подобных ему растворителей - за счёт образующегося комплекса SO3.эфир, диссоциация которого подавлена.
Для образования сульфокислот следует использовать эквимольное по отношению к субстрату количество хлорсульфоновой кислоты, так как при использовании избытка HSO3Cl образуются хлорангидриды сульфоновых кислот (сульфохлориды):

Такой метод проведения процесса неудобен технологически вследствие образования вязкой реакционной массы и выделения газообразного HCl. Поэтому реакцию предпочитают проводить в среде инертного растворителя (метиленхлорид, дихлорэтан, хлороформ, тетрахлорэтан и т.п.).
Сульфирование хлорсульфоновой кислотой является хорошим методом введения сульфогруппы в молекулу арена, так как не связано с использованием избытка реагента и, как правило, приводит к получению продукта с высоким выходом при высокой селективности процесса. Однако, вследствие опасности работы с хлорсульфоновой кислотой, этот метод редко используется в промышленных синтезах.
