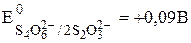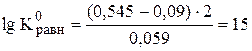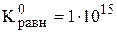Общие принципы растворения осадков малорастворимых электролитов
Растворение осадка, как это следует из произведения растворимости, происходит, если в растворе над осадком произведение активностей ионов станет меньше величины произведения растворимости. Частичное или полное растворение осадков может происходить при разбавлении раствора; нагревании (если, конечно, нагревание приводит к повышению растворимости), увеличении ионной силы; добавлении к раствору вещества, реагирующего с ионами, образующимися при растворении осадка.
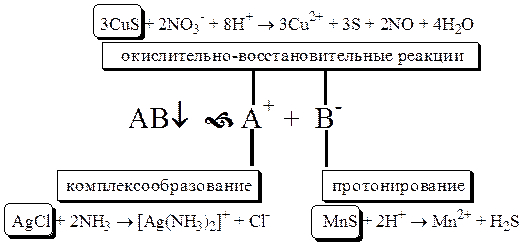
Попробуйте объяснить и подтвердить, если необходимо, расчётами, почему Cu(OH)2 растворяется в растворе NH3, а Mg(OH)2 - нет, почему AgCl не растворяется в разбавленной HNO3, зачем из BaSO4 в процессе переведения его в раствор вначале получают ВаСO3 и т.д.
ГЛАВА 7

7.1. Общая характеристика окислительно-восстановительных реакций
Окислительно-восстановительными называют реакции, в процессе которых происходит обмен электронами между реагирующими веществами.
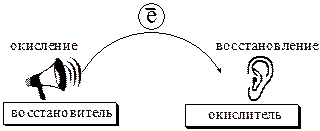
В любой окислительно-восстановительной реакции окислитель и восстановитель взаимодействуют друг с другом c образованием нового восстановителя и нового окислителя.
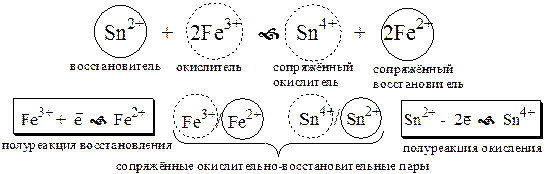
Поскольку в процессе окислительно-восстановительной реакции происходит лишь перераспределение электронов между реагирующими веществами, то число электронов, отданных восстановителем, должно быть равно числу электронов, полученных окислителем.
7.2. Количественная оценка окислительно-восстановительной способности веществ
Обычно для количественной оценки способности веществ отдавать и принимать электроны используют не константы равновесия, а электродные потенциалы. Это возможно потому, что процессы окисления и восстановления могут быть пространственно разделены.
Электродные потенциалы
Электродомв электрохимии называется поверхность раздела между проводником электрического тока с электронной проводимостью и проводником электрического тока с ионной проводимостью, или, иными словами, место, где электронный механизм переноса электрического заряда изменяется на ионный (и наоборот). В более узком смысле слова электродом часто называют проводник электрического тока с электронной проводимостью.
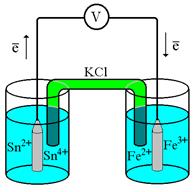 Рис. 7.1. Схематическое изображение гальванического элемента Рис. 7.1. Схематическое изображение гальванического элемента |
Проведём реакцию взаимодействия Sn2+ и Fe3+ так, чтобы процессы окисления и восстановления были пространственно разделены (рис. 7.1). В сосуде, содержащем Sn2+ и Sn4+, будут проходить следующие процессы. Ионы Sn2+ будут отдавать электроны платиновой проволоке и превращаться в Sn4+. Параллельно будет происходить и обратный процесс. Через некоторое время в системе установится равновесие:
Sn4+ + 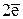 › Sn2+
› Sn2+
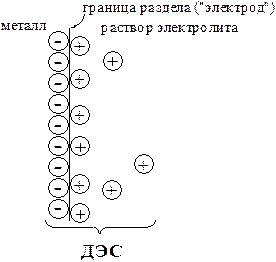 Рис. 7.2.Возникновение электродного потенциала Рис. 7.2.Возникновение электродного потенциала |
Вследствие установления данного равновесия поверхность платиновой проволоки и раствор вблизи неё будут иметь различный заряд, произойдёт образование так называемого «двойного электрического слоя» (рис. 7.2). На границе раздела «металл - раствор» возникнет разность потенциалов, называемая электродным потенциалом.
Аналогичные процессы будут происходить и в системе, содержащей Fe2+ и Fe3+. Однако, так как ионы Fe2+ обладают меньшей способностью отдавать электроны, чем Sn2+, а ионы Fe3+, соответственно, большей способностью принимать электроны, чем Sn4+, то поверхность платиновой проволоки, опущенной в раствор, содержащий Fe2+ и Fe3+, будет заряжена менее отрицательно, чем опущенной в раствор Sn2+ и Sn4+.
Соединим платиновые пластинки, опущенные в растворы, металлическим проводником. Для замыкания цепи соединим оба раствора солевым мостиком - трубкой, содержащей раствор KCl. В полученной системе, называемой гальваническим элементом, начнёт протекать электрический ток. Если включить в данную цепь потенциометр или высокоомный вольтметр, то можно измерить её ЭДС, которая будет характеризовать способность ионов Fe3+ получать электроны от Sn2+.
Абсолютную величину электродного потенциала индивидуального электрода определить невозможно. Возможно определить лишь разность потенциалов двух электродов. В принципе, это можно делать для каждой конкретной реакции. Однако гораздо более удобно выбрать какой-нибудь один стандартный электрод, относительно которого затем будут проводиться все измерения электродных потенциалов. В качестве такого электрода сравнения используется стандартный водородный электрод.
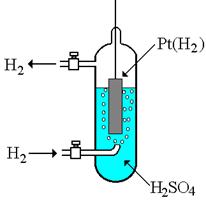 Рис. 7.3 Стандартный водородный электрод Рис. 7.3 Стандартный водородный электрод |
Стандартный водородный электрод представляет собой платиновую пластинку, насыщенную водородом, которая находится в растворе H2SO4 или HCl с 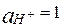 (рис. 7.3). Для увеличения адсорбирующей способности платину покрывают слоем губчатой платины. Для насыщения поверхности платины водородом через раствор пропускают газообразный H2 (р = 1 атм). Между водородом, растворённым в платине, и гидратированными катионами водорода, находящимися в растворе, устанавливается равновесие:
(рис. 7.3). Для увеличения адсорбирующей способности платину покрывают слоем губчатой платины. Для насыщения поверхности платины водородом через раствор пропускают газообразный H2 (р = 1 атм). Между водородом, растворённым в платине, и гидратированными катионами водорода, находящимися в растворе, устанавливается равновесие:
2H+ + 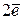 › H2 (Pt)
› H2 (Pt)
Потенциал стандартного водородного электрода принят равным нулю при любой температуре.
Стандартный электродный потенциал полуреакции (E0, j0) - это ЭДС гальванического элемента, состоящего из находящегося в стандартных условиях электрода, на котором протекает данная полуреакция, и стандартного водородного электрода.
Водородный электрод неудобен в работе, поэтому на практике в качестве стандартных используются вторичные стандартные электроды, потенциал которых относительно СВЭ определён с высокой точностью. Одним из таких электродов является хлоридсеребряный электрод,
Знак стандартного потенциала полуреакции зависит от выбранного направления полуреакции. При изменении направления знак меняется на противоположный. Например, для полуреакции (А) E0 = +0,771 В, следовательно, для обратной ей полуреакции (Б) E0 = - 0,771 В.
(А) Fe3+ + 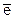 ® Fe2+ (Б) Fe2+ -
® Fe2+ (Б) Fe2+ - 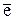 ® Fe3+
® Fe3+
Потенциал, характеризующий процесс восстановления, например, такой как (А), называется восстановительным, а потенциал, характеризующий процесс окисления, например, такой как (Б) - окислительным. В настоящее время величину электродного потенциала полуреакции принято относить к процессу восстановления окисленной формы
Чем больше величина электродного потенциала, тем более сильными окислительными свойствами обладает окисленная форма вещества и более слабыми восстановительными свойствами его восстановленная форма. Например, перманганат-ион при стандартных условиях в кислой среде является более сильным окислителем, чем дихромат-ион.
Cr2O72- + 14H+ + 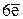 ® 2Cr3+ + 7H2O E0 = +1,33 В
® 2Cr3+ + 7H2O E0 = +1,33 В
MnO4- + 8H+ + 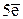 ® Mn2+ + 4H2O E0 = +1,51 В
® Mn2+ + 4H2O E0 = +1,51 В
Если для интересующей нас полуреакции значение Е0 в справочной литературе, по той или иной причине, не приведено, то его можно рассчитать, используя потенциалы других полуреакций.
Пример 7.1. Рассчитайте величину Е0 для окислительно-восстановительной пары Fe3+/Fe¯, если известно, что
Fe2+ + 2 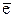 ® Fe¯ (
® Fe¯ ( 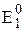 = -0,473В) Fe3+ +
= -0,473В) Fe3+ + 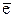 ® Fe2+ (
® Fe2+ ( 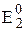 = +0,771В)
= +0,771В)
При сложении первого и второго уравнения мы получим уравнение интересующей нас полуреакции:
Fe3+ + 3 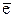 ® Fe¯
® Fe¯
Значение стандартного электродного потенциала данной полуреакции не будет равно сумме 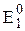 и
и 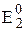 , т.е. 0,298В. Величина Е0 не зависит от количества вещества (потенциал - это интенсивная, а не экстенсивная величина), поэтому потенциалы нельзя складывать.
, т.е. 0,298В. Величина Е0 не зависит от количества вещества (потенциал - это интенсивная, а не экстенсивная величина), поэтому потенциалы нельзя складывать.
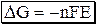
В отличие от электродного потенциала DG зависит от количества вещества, поэтому DG3 = DG1 + DG2. Следовательно
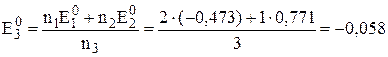 В
В
Разность электродных потенциалов окислителя, участвующего в прямой реакции, и окисленной формы восстановителя, образующегося в процессе реакции, называется ЭДС реакции (DЕ).
По величине ЭДС можно судить о том, возможно или нет самопроизвольное протекание данной реакции.
Пример 7.2. Определить, может ли самопроизвольно протекать при стандартных условиях реакция окисления иодид-ионов ионами Fe3+.
2Fe3+ + 2I- ® 2Fe2+ + I2
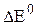 =
= 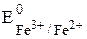 -
- 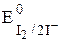 = 0,771 - 0,536 = 0,235В
= 0,771 - 0,536 = 0,235В
Данная реакция может самопроизвольно протекать в прямом направлении.
Уравнение Нернста
Влияние активности компонентов, участвующих в процессе, и температуры на величину потенциала описывается уравнением Нернста
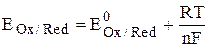
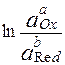
Если объединить постоянные величины в одну константу, а натуральный логарифм заменить десятичным, то при T = 298 К
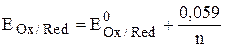
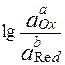
Например, для Cr2O72- + 14H+ + 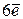 ® 2Cr3+ + 7H2O
® 2Cr3+ + 7H2O
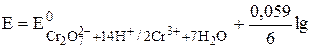
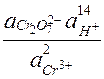
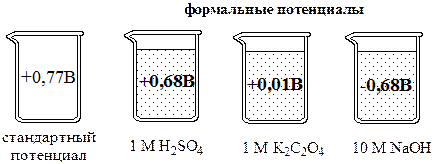
Формальный электродный потенциал 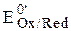 - это потенциал полуреакции, измеренный при условии, что концентрации окисленной и восстановленной формы равны 1 моль/л, а концентрации посторонних ионов известны.
- это потенциал полуреакции, измеренный при условии, что концентрации окисленной и восстановленной формы равны 1 моль/л, а концентрации посторонних ионов известны.
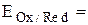
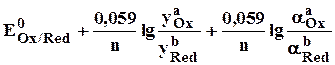
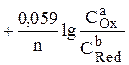
Формальный электродный потенциал является аналогом условной концентрационной константы равновесия в рассмотренных ранее равновесиях. Он равен выделенной полужирным шрифтом сумме первых трех членов в приведенном выше уравнении. Величина формального потенциала зависит от ионной силы раствора, природы и концентрации посторонних электролитов. Например, для Fe3+/Fe2+:
Константа равновесия окислительно-восстановительной реакции
Способность одного вещества отдавать электроны другому веществу можно оценить также с помощью константы равновесия окислительно-восстановительной реакции. Эта константа связана с ЭДС реакции следующим образом. Пусть реакция между окислителем Ox1 и восстановителем Red2 состоит из двух полуреакций (полуреакцию с участием Red2 для удобства запишем как процесс восстановления окисленной его формы):
Ox1 + n1 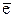 › Red1
› Red1 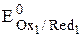
Ox2 + n2 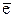 › Red2
› Red2 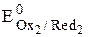
Наименьшее общее кратное для n1 и n2 обозначим как m. Суммарное уравнение реакции будет иметь следующий вид
aOx1 + bRed2 › aRed1 + bOx2,
где a = m/n1, b = m/n2.
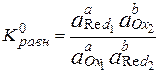
В состоянии равновесия DG = 0, DЕ = 0 и 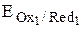 =
= 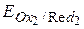
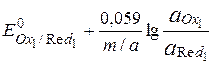 =
= 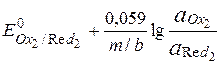
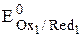 -
- 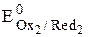 =
= 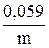
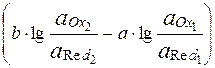
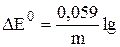
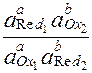 =
= 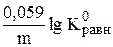
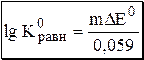
Обратите внимание, что в выражение для расчёта константы равновесия окислительно-восстановительной реакции входит не произведение числа электронов n1 и n2, а их наименьшее общее кратное m, которое может быть равно этому произведению, а может быть и не равно.
Если lgK > 0, реакция может самопроизвольно протекать в прямом направлении. Чем больше величина K, тем больше “глубина” протекания окислительно-восстановительной реакции.
Пример 7.3. Рассчитать термодинамическую константу равновесия реакции
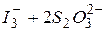 ›
› 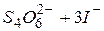
если 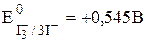 ,
,