Реакционные центры в спиртах, теолах и аминах. Кислотные свойства. Основные свойства. Кислоты и основания Бренстеда.
17. Реакционная способность альдегидов и кетонов. Общая характеристика. Реакционные центры альдегидов и кетонов. Общее описание механизму нуклеофильного присоединения (AN). Присоединение спиртов. Присоединение воды. Присоединение аминов и их производных. Реакции полимеризации. Реакции конденсации. Механизм альдольной конденсации. Восстановление и окисление.
18. Реакционная способность карбоновых кислот и их функциональных производных. Общая характеристика карбоновых кислот. Реакционные центры в карбоновых кислотах. Кислотные свойства. Нуклеофильное замещение (образование сложных эфиров, амидов, ангидридов кислот). Механизм реакции этерификации.
Функциональные производные карбоновых кислот. Общая характеристика. Номенклатура. Тетраэдрический механизм нуклеофильного замещения. Сложные эфиры. Тиоэфиры. Амиды и гидразиды. Ангидриды. Сульфоновые кислоты и их производные.
20. Стехиометрические основы строения молекул органических веществ.Стереохимия – химия соединений в трехмерном пространстве.Изомеры – соединения с одинаковым составом, но отличающиеся последовательностью связывания атомов и (или) расположением их в пространстве.Стереоизомеры – соединения, в молекулах которых имеется одинаковая последовательность химических связей атомов, но различное расположение этих атомов относительно друг друга в пространстве.
Конфигурация – порядок расположения атомов в пространстве без учета различий, возникающих вследствие вращения вокруг одинарных связей. Конфигурационные изомеры могут переходить друг в друга только путем разрыва одних и образованием других химических связей. 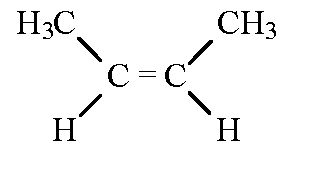 цис-бутен-2 \
цис-бутен-2 \ 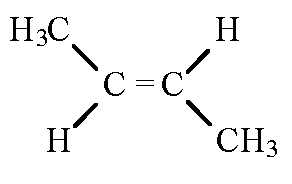 транс-бутен-2.
транс-бутен-2.
Хиральность – способность объекта быть несовместимым со своим зеркальным изображением. Центр хиральности – асимметрический атом С и др. – атом связанный с 4мя различными атомами или группами (Обозначается *С).
Энантиомеры –стереоизомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное отображение. Способны вращать плоскость поляризации света, т.е. обладают оптической активностью. Имеют одинаковые значения угла вращения α, но противоположенные направления: один – левовращающийся (-), другой – правовращающийся (+). Для их изображения используют проекционные формулы Фишера.
Относительная и абсолютная (истинное расположение в пространстве заместителей у хирального центра) конфигурации.
Диастереомерия – стереоизомеры, не являющиеся энантиомерами.
1) Ω-диастереомеры – содержат несколько центров хиральности. Подсчет числа стереоизомеров для них производится по формуле: 2n, n – число центров хиральности.
2) π-диастереомеры – конфигурационные изомеры, содержащие π-связь.
Конформация – геометрические формы молекул переходящие друг в друга путем вращения вокруг одинарных связей. Различаются по своей энергии.
Заслоненные конформации – заместители находятся в наиболее близком положении друг к другу.
Заторможенные – заместители расположены наиболее далеко друг от друга в пространстве (более устойчивая).
Торсионное напряжение – увеличение потенциальной энергии системы, связанное с взаимодействием противостоящих связей, затрудняющих свободное вращение вокруг одинарных связей.
Ван-дер-ваальсово напряжение – обусловлено силами отталкивания между валентно не связанными большими по объему заместителями.
Проекционные формулы Ньюмена – получают при проецировании на плоскость молекулы вдоль связи С-С.
Конформации циклических соединений– для них характерен специфический вид напряжения – угловое напряжение, связанное с наличием замкнутой цепи. Угловое напряжение (байеровское) – напряжение вызванное отклонением валентных углов между атомами С в цикле от нормального значения.
