Адсорбция уксусной кислоты активированным углем
Цель работы – изучение характера зависимости адсорбции уксусной
кислоты на поверхности угля в зависимости от
концентрации при постоянной температуре;
знакомство с титриметрическим методом анализа.
Опыт 1. Адсорбция водных растворов уксусной кислоты на поверхности активированного угля
Выполнение опыта
В пронумерованные стаканчики с активированным углем массой 1 г (предварительно измельченным в фарфоровой ступке) поместите по 50 мл растворов СН3СООН (0,5 М и 0,3 М соответственно). Оставьте на 40 мин. Периодически (каждые 5 мин) встряхивайте содержимое стаканчиков для ускорения достижения адсорбционного равновесия. Следите, чтобы при перемешивании частицы угля не оставались на стенках стаканчика.
По истечении времени адсорбции суспензию угля отфильтруйте, используя фильтры, смоченные водой. Первые порции фильтратов (5 – 10 мл) отбросьте, так как в них концентрация кислоты может быть понижена за счет адсорбции кислоты фильтровальной бумагой.
Определите концентрацию кислоты (С) в отфильтрованных растворах. Для этого в пронумерованные конические колбы для титрования отмерьте по 10 мл полученных фильтратов и оттитруйте 0,1 М раствором NаОН
в присутствии фенолфталеина до перехода окраски раствора из бесцветной в розовую. Рассчитайте концентрацию раствора СН3СООН после адсорбции С:
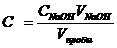
СNaOH – концентрация раствора NaOH, моль/дм3;
VNaOH – объем раствора щелочи на титрование кислоты после адсорбции, дм3;
Vпробы – объем пробы раствора СН3СООН на титрование после адсорбции, дм3.
Найдите значение удельной адсорбции кислоты для каждого раствора по формуле:
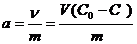 ,
,
а – удельная адсорбция – количество вещества, адсорбированного одним граммом адсорбента, моль/г;
ν – количество вещества кислоты, содержащееся в фильтрате, моль;
С0 – исходная концентрация уксусной кислоты, моль/дм3;
С – концентрация раствора СН3СООН после адсорбции, моль/дм3;
m – масса адсорбента, г;
V – объем раствора, из которого идет адсорбция, дм3.
Результаты опыта занесите в таблицу:
| Номер колбы | ||
| Концентрация растворов СН3СООН до адсорбции (С0, моль/дм3) | ||
| Объем пробы раствора СН3СООН на титрование после адсорбции (Vпробы, см3) | ||
| Расход раствора щелочи на титрование после адсорбции (VNaOH, см3) | ||
| Концентрация СН3СООН после адсорбции (С, моль/дм3) | ||
| Адсорбция а, моль/г |
Вопросы для самоконтроля знаний
1. Дайте определение понятиям: адсорбция, адсорбент, адсорбтив, адсорбат.
2. Какие факторы влияют на адсорбцию? Почему адсорбция – процесс самопроизвольный?
3. В чем заключается особенность адсорбции на границе раздела твердое тело – жидкость?
4. По каким признакам можно отличить физическую адсорбцию от хемосорбции?
5. Какой частью молекулы уксусной кислоты происходит ее адсорбция на поверхности угля?
6. Какие уравнения используются для описания процессов адсорбции?
7. Какие вещества называют поверхностно-активными? Приведите примеры.
8. Какова причина возникновения избыточной поверхностной энергии?
9. Что такое поверхностное натяжение? В каких единицах измеряется эта величина?
10. От каких факторов зависит поверхностное натяжение?
Литература
Основная
1. Ахметов Н.С. Общая и неорганическая химия: Учебник для вузов. М.: Высшая школа, 2006. 639 с.
2. Задачи и упражнения по общей химии: Учеб. пособие /Под ред. Н.В. Коровина. М.: Высшая школа, 2006. 249 с.
3. Коровин Н.В. Общая химия: Учебник для вузов. М.: Высшая школа, 2007. 557 с.
4. Слинкина М.В., Харина Г.В. Методические указания и контрольные задания по химии. Екатеринбург: ГОУ ВПО «Рос. гос. проф.-пед. университет», 2009. 68 с.
5. Артеменко А.И. Органическая химия: Учебник для вузов. М.: Высшая школа, 2007. 558 с.
Дополнительная
1. Ахметов Н.С. Лабораторные и семинарские занятия по общей и неорганической химии: Учебное пособие для вузов. М.: Высшая школа, 1999. 365 с.
2. Коржуков Н.Г. Общая и неорганическая химия: Учеб. пособие. М.: Мисис, 2004. 511с.
3. Оганесян Э.Т. Важнейшие понятия и термины в химии: Справ. пособие. М.: Высшая школа 1993. 351с.
6. Угай Я.А. Общая и неорганическая химия: Учебник для вузов. М.: Высшая школа, 2002. 527 с.
4. Хомченко Г.П., Цитович И.К. Неорганическая химия: Учебник для вузов. М.: Высшая школа, 1998. 445 с.
5. Глинка Н.Л. Задачи и упражнения по общей химии: Учебное пособие для вузов. М.: Химия, 1998. 272 с.
Методические указания к выполнению
практических и лабораторных работ
по дисциплине «Химия»
Подписано в печать Формат 60х84/16. Бумага для множ. аппаратов.
Печать плоская. Усл. печ. л. Уч.-изд. л. Тираж экз. Заказ
ФГАОУ ВПО «Российский государственный профессионально-педагогический университет». Екатеринбург, ул. Машиностроителей, 11.
__________________________________________________________________
Ризограф ФГАОУ ВПО РГППУ. Екатеринбург, ул. Машиностроителей, 11.
