Условия самопроизвольного протекания процессов
Факультет «нефти и газа»
Кафедра «математических и естественнонаучных дисциплин»
Утверждаю:
Ректор НОУ ВПО «КИГИТ»
О. А. Дегтева ______________
____________________ 20__г.
УЧЕБНОЕ ПОСОБИЕ
по выполнению контрольной работы
ПО ДИСЦИПЛИНЕ «Физическая и коллоидная химия»
Для направления подготовки
131000.62 Нефтегазовое дело
Профиль подготовки: «Сооружение и ремонт объектов
систем трубопроводного транспорта»,
«Эксплуатация и обслуживание объектов транспорта
и хранения нефти, газа и продуктов переработки»
Степень выпускника: БАКАЛАВР
Форма обучения заочная
Ижевск 2011
Составитель: доцент, к.х.н. Шумилова М.А.
Рассмотрен и утвержден на заседании кафедры «математических и естественнонаучных дисциплин»
Протокол № ____ от «___»_______2012г.
Зав. кафедрой _______________
(подпись)
Согласовано:
Начальник УМУ __________________Е. Ю. Соснина
Учебно-методическим советом НОУ ВПО «КИГИТ»
Протокол № ____ от «____»__________2012г.
В учебном пособии представлены основные разделы физической и коллоидной химии. В каждом разделе рассмотрены основные теоретические положения, приведены примеры решения типовых заданий, даны задания для выполнения контрольной работы и примерный перечень вопросов для подготовки к зачету. В конце пособия приводятся справочные данные, необходимые при решении типовых задач.
Предлагаемое пособие предназначается для студентов, изучающих в соответствии с государственным образовательным стандартом в цикле общепрофессиональных дисциплин курс «Физическая и коллоидная химия» по направлению подготовки 131000.62 «Нефтегазовое дело» дипломированного специалиста – бакалавра с профилем подготовки «Сооружение и ремонт объектов систем трубопроводного транспорта» и «Эксплуатация и обслуживание объектов транспорта и хранения нефти, газа и продуктов переработки».
Пособие рекомендуется использовать при выполнении контрольной работы по данной дисциплине, а также при подготовке к зачету по изучаемому курсу.
© Шумилова М.А., 2012
© НОУ ВПО «Камский институт гуманитарных и инженерных технологий», 2012
Содержание
стр
Общие методические указания 2
Правила оформления контрольной работы 3
Список литературы 3
Введение 4
Термодинамика и термохимия 4
Основы термодинамики 4
Основные газовые законы 18
Фазовые равновесия 24
Химическая кинетика 31
Электрохимия 40
Коллоидная химия 55
Поверхностные явления 55
Коллоидное состояние вещества 65
Электрокинетические свойства коллоидных растворов 72
Приложения 77
Примерный перечень вопросов к зачету по курсу «Физическая
и коллоидная химия» 83
Общие методические указания
Физическая химия исследует неразрывную связь между физической и химической формами движения материи. Наименование «физическая химия» указывает на то, что эта наука находится на границе физики, изучающей главным образом энергию и её превращения, и химии, изучающей вещества и их превращения. Данная наука, используя фундаментальные законы физики, изучает процессы, связанные с превращением вещества и энергии. Другими словами, физическая химия – это наука, исследующая связь химических и физических свойств веществ, химических и физических явлений и процессов.
Основными проблемами, определяющими предмет физической химии, являются проблемы химической термодинамики, изучающей связь между химической и другими формами энергии. Учение о строении вещества рассматривает строение атомов, молекул и агрегатное состояние веществ. Химическая кинетика изучает скорость и механизм химических реакций, а также явление катализа. Учение о растворах рассматривает природу растворов, их внутреннюю структуру, важнейшие свойства, зависящие от концентрации и химической природы компонентов, составляющих раствор, а также свойства растворов электролитов.
Изучение данной дисциплины позволяет осуществить переход от описательного восприятия физико-химических данных к количественным представлениям, к предсказанию протекающих процессов в рассматриваемой системе.
Изучение раздела физической химии - "Коллоидная химия" имеет важное значение для студентов, обучающимся по техническим специальностям в нефтегазовой отрасли. Данная дисциплина завершает цикл общеобразовательных химических дисциплин и является теоретической основой для изучения курса «Химия нефти и газа», когда нефть рассматривают с точки зрения дисперсной системы.
Коллоидная химия – это наука о поверхностных явлениях и дисперсных системах, их физических, химических, механических свойствах. Если химические дисциплины дают знания о свойствах веществ, то предметом изучения коллоидной химии являются свойства и закономерности поведения реальных тел, состоящих из различных веществ.
В предлагаемом учебном пособии представлены основные разделы коллоидной химии: дисперсные системы, поверхностные явления, адсорбционные равновесия, агрегативная устойчивость и коагуляция коллоидных систем.
В каждом разделе предлагаемого методического пособия теоретический материал изложен в конспективном плане, чтобы дать краткие определения понятий, явлений и законов. В некоторых, наиболее трудных вопросах, пояснения значительно расширены. Прежде, чем приступить к самостоятельному решению задач, следует ознакомиться с соответствующей главой учебника, с теоретическим введением по данному разделу пособия и с примерами решения задач. Однако, при ответе на качественные вопросы, пособие служит для первичной ориентации и получения исходных сведений по интересующему вопросу, но не отменяет рекомендованной литературы для полного ответа и подготовки к зачету. В конце каждого раздела находятся варианты заданий для выполнения контрольной работы по изучаемой дисциплине, а также в разделе «Приложение» представлены необходимые для решения задач табличные данные. Если с первого раза с решением некоторых задач студенту не удаётся справиться, ему необходимо ещё раз обратиться к предлагаемому пособию, учебной литературе, другим пособиям, прибегнуть к консультации преподавателя. Перечень литературы и других методических материалов приводится после методических указаний.
Контрольная работа выполняется в соответствии с шифром зачетной книжки студента. Так, если шифр зачётной книжки ЗЭ-10-6, то последняя цифра (в данном случае - 6) означает номер варианта контрольной работы.
Правила оформления контрольной работы
1 Контрольная работа должна содержать титульный лист, список использованной литературы (в конце работы), иметь поля для замечаний преподавателя. В тексте работы необходимо:
2 Записать номер варианта, номер и полную формулировку каждого конкретного задания.
3 Дать четкие и краткие ответы по сути на теоретические вопросы.
4 При решении задачи нужно записать её условия, используемые расчетные формулы в общем виде, пояснить входящие в них величины, после чего произвести вычисления, обосновывая каждое действие и соблюдая соответствие размерностей используемых величин в системе СИ.
5Строить необходимые графики на миллиметровой бумаге и вклеивать их в работу по ходу текста.
Список литературы
Основная
1. Кругляков П.М., Хаскова Т.Н. Физическая и коллоидная химия. Учеб. пособие. М.: Высшая школа, 2005.
2. Гельфман М.И., Практикум по физической химии. – СПб.: Издательство «Лань», 2004.
3. Липатников В.Е., Казаков К.М. Физическая и коллоидная химия. – М.: Высшая школа, 1981.
4. Киреев В.А. Курс физической химии. - М.: Химия, 2000.
5. Воронин Н.Н., Липин А.Б. Коллоидная химия: Сборник задач. – СПб.: изд. Санкт-Петербургского государственного горного института, 2002.
6. Гамеева О.С. Сборник задач и упражнений по физической и коллоидной химии. - М.: Высшая школа, 1999.
Дополнительная
7. Ярославцев А.Б. Основы физической химии. - М.: Научный мир, 2000.
8. Рович-Щербо М.И., Новиков В.В. Физическая и коллоидная химия. - М.: Высшая школа, 1975.
9. Балезин С.А., Парфенов Г.С. Основы физической и коллоидной химии. – М.: Просвещение, 1975.
10. Эткинс П. Физическая химия. В 2-х т. – М.: Мир, 1980.
ВВЕДЕНИЕ
Физическая химия изучает неразрывную связь между физической и химической формами движения материи. Физическая химия изучает химические процессы физическими методами, устанавливая свойственные этим процессам общие количественные закономерности. Иными словами, физическая химия – это наука, изучающая связь химических и физических свойств вещества, химических и физических явлений и процессов.
Предметом физической химии является объяснений химических явлений на основе более общих законов физики. В курсе физической химии обычно выделяют несколько разделов.
Учение остроении вещества рассматривает строение атомов, молекул и агрегатное состояние веществ. Химическая термодинамикаизучает связь между химической и другими формами энергии. Химическая кинетика изучает скорость и механизм химических реакций, а также явление катализа. Учение о растворах рассматривает природу растворов, их внутреннюю структуру, важнейшие свойства, зависящие от концентрации и химической природы компонентов, составляющих раствор, а также свойства растворов электролитов. Электрохимияизучает особенности свойств растворов электролитов, явление электропроводности, электролиза, коррозии, работу гальванических элементов.
Все разделы физической химии объединяет единая основа – общие законы природы, которые применимы к любым процессам и любым системам, независимо от их строения.
ТЕРМОДИНАМИКА И ТЕРМОХИМИЯ
Основы термодинамики
Термодинамика изучает процессы взаимного превращения разных видов энергии. Она базируется только на экспериментально обнаруженных объективных закономерностях, выраженных в двух основных началах термодинамики.
Основные понятия и определения
Химическая термодинамика рассматривает не отдельные частицы, а их совокупность – системы.
Термодинамической системой называется тело или совокупность тел, находящихся во взаимодействии и условно обособленных от окружающей среды. Всё, что не входит в систему, называется внешней средой.
Согласно трём статистическим ансамблям Гиббса различают три типа термодинамических систем:
· Открытыми называют системы, обменивающиеся с окружающей средой и веществом и энергией (макроканоническое распределение Гиббса). Примером могут служить живые объекты.
· Закрытыми считаются системы, обменивающиеся с окружающей средой энергией, но не веществом (каноническое распределение Гиббса). Например, газ, находящийся в баллоне.
· Изолированными являются системы, не обменивающиеся с окружающей средой ни энергией, ни веществом (микроканоническое распределение Гиббса). Примером может быть запаянная ампула, полностью изолированная от внешней среды.
Фазой называется совокупность всех однородных частей системы, обладающих одинаковыми свойствами и отделённых от остальных частей системы поверхностью раздела. Все термодинамические системы можно разделить на две большие группы - гомогенные и гетерогенные. Гомогенными (однофазными) называют системы, состоящие только из одной фазы, например, воздух – смесь газов. Системы, содержащие две или более число фаз, называются гетерогенными (неоднородными, разнофазными). Например, не растворившиеся в воде кристаллы поваренной соли образуют гетерогенную систему из двух фаз. В гетерогенной системе составные её части – фазы – разделены поверхностью раздела.
Совокупность всех физических и химических свойств системы характеризует её состояние.
Физические величины, позволяющие определять состояние системы, называются параметрами состояния. К ним относят переменные величины, которые непосредственно могут быть заданы и измерены: температура Т, объём V, давление Р. Уравнение, описывающее взаимосвязь параметров состояния, называется уравнением состояния. Например, для идеального газа применимо уравнение состояния Менделеева-Клапейрона:
pV = νRT,
где ν – количество газа, R – универсальная газовая постоянная.
К термодинамическим функциям относят переменные величины, зависящие от параметров состояния, которые не могут быть непосредственно измерены. Их подразделяют на функции процесса: теплота Q и механическая работа А, и функции состояния(или характеристические функции): внутренняя энергия U, энтальпия Н, энтропия S, изобарно-изотермический потенциал (свободная энергия Гиббса) G и изохорно-изотермический потенциал (свободная энергия Гельгольца) F. Функции состояния являются количественной мерой изменения свойств в термодинамике. К особенностям характеристических функций относится их независимость от способа (пути) достижения данного состояния системы. Их значение определяется состоянием системы, т.е. параметрами системы (давлением, температурой и др.). К особенностям характеристических функций также относится зависимость их величин от количества или массы вещества, поэтому принято относить их к одному молю вещества.
Если при отсутствии каких-либо внешних воздействий на систему термодинамические параметры с течением времени не изменяются, то такое её состояние называется равновесным. Состояние системы называется неравновесным, если её параметры изменяются при отсутствии внешнего воздействия.
При изменении хотя бы одного из параметров системы равновесие нарушается и начинается изменение состояния системы, т.е. протекает какой-либо процесс. Термодинамическим процессом называется всякое изменение в системе, связанное с изменением хотя бы одного термодинамического параметра.
Термодинамика базируется на двух фундаментальных законах (началах), являющихся всеобщими законами природы. Они не могут быть выведены, но и не могут быть отвергнуты, поэтому рассматриваются как постулаты.
Первый закон термодинамики
Первый закон термодинамики – это закон сохранения энергии в изолированной системе.
Теплота Q, переданная системе, идёт на увеличение её внутренней энергии ΔU и на совершение работы системой против внешних сил:
Q = ΔU + A (1)
Для бесконечно малого изменения величин:
δQ = dU + δA, (2)
бесконечно малое изменение функций состояния принято обозначать буквой d, а функций процесса – δ.
Внутренняя энергия - это общий запас энергии системы. Она включает в себя все виды энергии системы (энергию движения и взаимодействия молекул, атомов, ядер и др. частиц, внутриядерную и др. виды энергии), кроме кинетической энергии движения системы, как целого, и потенциальной энергии её положения. Абсолютную величину внутренней энергии измерить нельзя, можно определить её изменение при переходе системы из начального состояния в конечное. Внутренняя энергия представляет собой способность системы к совершению работы или передачи тепла.
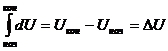 (3)
(3)
При увеличении внутренней энергии ΔU>0, при уменьшении ΔU<0.
Работа процесса – это энергия, передаваемая одним телом другому при их взаимодействии. В химической термодинамике обычно рассматривают работу расширения газа А = р · ΔV. Если система совершает работу, то величина А положительна, так как
ΔV = 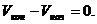
Поскольку работа является функцией процесса, то её изменение
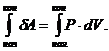 (4)
(4)
Для изохорных процессов, т.е. процессов, протекающих при постоянном объёме (V=const, dV=0):
δQv = dU, Qv = ΔU. (5)
Для изобарных процессов, протекающих при постоянном давлении (p=const, dp=0), выражение первого закона термодинамики можно преобразовать, если использовать функцию состояния системы, называемую энтальпией. Энтальпия H, как и внутренняя энергия, не зависит от пути процесса, характеризует полную энергию системы и «теплосодержание»:
H = U + pV;
dH = dU + d(pV) = dU + pdV + Vdp; (6)
при р=const, dp=0, Vdp=0
δQp = dU + pdV = (dH – pdV) + pdV = dH,
Qp = ΔH (7)
Для изотермических процессов,протекающих при постоянной температуре (T = const и U = const, dU = 0)
δQ = δA, Q = A. (8)
Для адиабатных процессов, при которых нет теплообмена системы с окружающей средой (δQ = 0):
δA = - dU, A = - ΔU. (9)
Основы термохимии
Термохимия – раздел физической химии, который изучает тепловые эффекты реакций. Тепловые эффекты реакции – это наибольшее количества тепла, которое выделяется или поглощается при необратимо идущей химической реакции. При этом должно соблюдаться условие, чтобы система не совершала никакой работы, кроме расширения.
Если теплота поглощается системой, т.е. процесс является эндотермическим, величина Q берётся со знаком «плюс». В случае выделения тепла (экзотермический процесс), величина Q берётся со знаком «минус».
Согласно уравнениям (5) и (6), тепловой эффект реакций равен изменению функций состояния и приобретает свойства функций состояний состояния. В случае химической реакции изменение энтальпии равно взятому с обратным знаком тепловому эффекту реакции, проведённой при постоянной температуре и постоянном давлении. На этом положении базируется основной постулат термохимии, сформулированный в 1840г. русским химиком акад. Гессом и называется законом Гесса:
Тепловой эффект химической реакции не зависит от пути протекания процесса, а определяется начальным и конечным состояниями системы.
Закон Гесса позволяет вычислять тепловой эффект реакции, если по каким-либо причинам его невозможно определить экспериментально.
Тепловой эффект реакции образования 1 моля данного вещества из простых в стандартных условиях (давлении 1 атм и температуре 25º С (298К)) называется стандартной теплотой образования Н 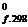 сложного вещества. Теплоты образования простых веществ равны нулю (O2, N2, H2 и др.). Теплоты образования Н
сложного вещества. Теплоты образования простых веществ равны нулю (O2, N2, H2 и др.). Теплоты образования Н 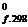 многочисленных соединений в стандартных условиях приводятся в термодинамических таблицах.
многочисленных соединений в стандартных условиях приводятся в термодинамических таблицах.
Из закона Гесса вытекают два следствия, позволяющие определять тепловые эффекты химических реакций, не прибегая к измерениям.
Первое следствие из закона Гесса: тепловой эффект химической реакции при стандартных условиях равен сумме стандартных теплот образования продуктов реакции, умноженных на стехиометрические коэффициенты, минус стандартные теплоты образования исходных веществ, умноженные на соответствующие коэффициенты:
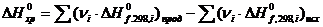 . (10)
. (10)
Теплотой сгорания ΔНсгор называют тепловой эффект реакции сгорания 1 моля данного вещества с образованием СО2, Н2О, N2 и др. Значения стандартных теплот сгорания ΔНсгор приводятся в справочных таблицах.
Второе следствие из закона Гесса: тепловой эффект химической реакции при стандартных условиях равен сумме стандартных теплот сгорания исходных веществ, умноженных на стехиометрические коэффициенты, минус стандартные теплоты сгорания продуктов реакции, умноженные на соответствующие коэффициенты:
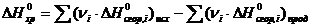 . (11)
. (11)
Индекс º у энтальпии образования и энтальпии сгорания указывает на стандартность условий, ν – число молей различных веществ.
Пример 1. Рассчитать тепловой эффект реакции получения водорода из природного газа в стандартных условиях
СН4 + 2 Н2О(г) = СО2 + 4Н2
Решение.
В соответствии с уравнением (10), вытекающим из первого следствия из закона Гесса получаем:
ΔН 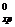 = ΔН
= ΔН 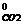 + 4 ΔН
+ 4 ΔН 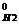 - ΔН
- ΔН 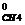 - 2 ΔН
- 2 ΔН 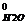
Подставляем значения стандартных величин образования (в кДж/моль) из справочных данных (табл,1 Приложения) и получаем
ΔН 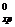 = 1·(-393,51) + 4·0 – 1·(-74,85) – 2 ·(241,82)
= 1·(-393,51) + 4·0 – 1·(-74,85) – 2 ·(241,82)
Как видно, данная реакция является эндотермической.
Пример 2. Рассчитать стандартную энергию образования пропана С3Н8, если изменение стандартной энтальпии реакции его сгорания
С3Н8 + 5О2 = 3СО2 + 4Н2О(г)
равно ΔН 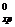 = -2043,86 кДж/моль.
= -2043,86 кДж/моль.
Решение.
В соответствии с уравнением (10):
ΔН 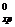 = 3 ΔН
= 3 ΔН 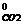 + 4 ΔН
+ 4 ΔН 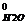 – ΔН
– ΔН 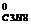 – 5 ΔН
– 5 ΔН 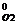 ,
,
откуда
ΔН 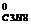 = – ΔН
= – ΔН 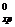 + 3 ΔН
+ 3 ΔН 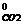 + 4 ΔН
+ 4 ΔН 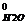 – 5 ΔН
– 5 ΔН 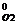 ,
,
Подставив значение ΔН 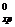 и справочные данные из табл. 1 Приложения, получим:
и справочные данные из табл. 1 Приложения, получим:
ΔН 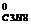 = –(–2043,86) + 3(–393,51) + 4(–241,82) –5∙0 = -103,85 кДж/моль.
= –(–2043,86) + 3(–393,51) + 4(–241,82) –5∙0 = -103,85 кДж/моль.
Как видно, реакция образования пропана относится к экзотермическим реакциям.
В общем случае тепловой эффект химического процесса зависит от температуры и давления, при которых осуществляется химическое превращение. Влиянием давления на ΔU и ΔН реакции обычно пренебрегают.
Теплоёмкостью с называют количество теплоты, необходимое для нагревания 1г (удельная теплоёмкость) или 1 моля (молярная теплоёмкость) вещества на 1 К.
с = 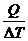 . (12)
. (12)
С повышением температуры теплоёмкость твёрдых, жидких и газообразных веществ увеличивается.
Различают истинную теплоёмкость, т.е. при теплоёмкость при данной температуре
с = 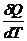 (13)
(13)
и среднюю теплоёмкость
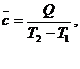 (14)
(14)
которая соответствует конечному интервалу температур. При незначительной величине интервала теплоёмкость считают не зависящей от температуры.
В зависимости от условий нагревания теплоёмкость бывает изобарной ср и изохорной сv:
ср = 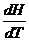 , (15)
, (15)
сv = 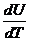 . (16)
. (16)
Для выведения зависимости теплового эффекта от температуры продифференцируем уравнение (6):
Qp = ΔН = H2 – H1,
учитывая уравнение (14), получаем:
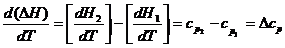 . (17)
. (17)
Уравнение (17) называют уравнением Кирхгофа, где Δср – это разность молярных теплоёмкостей продуктов реакции и исходных веществ с учётом стехиометрических коэффициентов.
Для вычисления теплового эффекта при заданной температуре Т, необходимо проинтегрировать уравнение Кирхгофа:
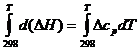 , (18)
, (18)
ΔНТ = ΔН 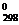
 +
+ 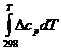 . (19)
. (19)
В широком диапазоне температур зависимость теплоёмкости веществ от температуры выражается в виде эмпирических уравнений:
ср = a + bT + 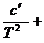 c·T2. (20)
c·T2. (20)
Коэффициенты a, b, c, c' для продуктов реакции и исходных веществ приводятся в справочниках, далее вычисляют Δa, Δ b, Δc, Δ c' как суммы соответствующих величин для продуктов реакции, умноженные на стехиометрические коэффициенты минус соответствующие значения для исходных веществ. Затем зависимость
Δ ср = Δa + ΔbT + 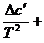 Δc·T2 (21)
Δc·T2 (21)
подставляются под знак интеграла в уравнение (19) и производится расчёт ΔНТ по правилам интегрирования.
При использовании табличных значений средних теплоемкостей 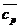 величина Δ
величина Δ 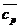 является постоянной и может быть вынесена из-под знака интеграла:
является постоянной и может быть вынесена из-под знака интеграла:
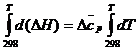 , (22)
, (22)
ΔНТ = ΔН 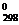 +
+ 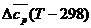 . (23)
. (23) 
Для процессов, протекающих при постоянном объёме, соответственно, зависимость теплового эффекта от температуры описывается уравнением:
ΔUT = 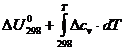 . (24)
. (24)
Пример 3. Определить теплоту, поглощённую при нагревании 100 г двуокиси углерода от 15 до 1000ºС при постоянном объёме, если
с 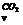 = 27,24 + 0,00809t Дж/моль·град.
= 27,24 + 0,00809t Дж/моль·град.
Решение. Объёмная теплоёмкость равна количеству теплоты, которое необходимо для нагревания на 1ºС 1м3 газа, приведённого к нормальным условиям. При повышении температуры от Т1 до Т2 количество поглощаемой теплоты можно рассчитать по формуле:
Q = 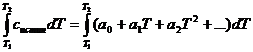 (для 1 моля вещества)
(для 1 моля вещества)
После интегрирования выражение примет вид:
Q=[a0 (T2 – T1) + a1 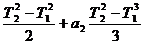 ]
]
При вычислении по данной формуле температуру можно брать в градусах Цельсия.
Число молей углекислого газа определяем по формуле
ν = 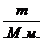
и тогда количество поглощённой теплоты в рассматриваемом процессе будет равно
Q = 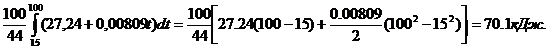
Второй закон термодинамики
Второй закон термодинамики устанавливает критерии, позволяющие определить направление самопроизвольного протекания процессов.
Самопроизвольными называют процессы, которые протекают в системе без затраты энергии извне.
Процессы бывают обратимыми и необратимыми. Необратимые процессы идут самопроизвольно лишь в одном направлении. После протекания данных процессов, сопровождающихся изменениями в системе и окружающей среде, невозможно вернуть одновременно и систему и окружающую среду в исходное состояние.
Обратимыми являются процессы, после которых систему и окружающую среду можно вернуть в исходное состояние.
Второй закон термодинамики имеет несколько формулировок, в варианте, предложенном Клаузиусом, он выглядит следующим образом: невозможен самопроизвольный переход теплоты от холодного тела к горячему.
Физический смысл второго закона термодинамики заключается в том, что любой самопроизвольный процесс протекает в направлении, при котором система из менее вероятного состояния переходит в более вероятное состояние. Другими словами, самопроизвольному протеканию процесса способствует увеличение неупорядоченности в системе.
Для характеристики меры неупорядоченности используется термодинамическая функция – энтропия S, которая связана с термодинамической вероятностью системы формулой Больцмана:
S = k · lnW, (25)
где k – постоянная Больцмана.
Под термодинамической вероятностью W понимают число равновероятных микроскопических состояний, которыми может быть реализовано данное макроскопическое состояние системы. Для определения термодинамической вероятности системы необходимо найти число различных вариантов положений всех частиц системы в пространстве.
Энтропия является количественной мерой беспорядка в системе. Чем больше W, тем хаотичнее система, тем больше величина энтропии. Нагревание вещества приводит к увеличению энтропии, а охлаждение – к уменьшению. При приближении к абсолютному нулю (-273ºС) энтропия стремится к нулю, что позволяет определить абсолютные значения энтропии различных веществ, значения которых при стандартных условиях представлены в таблицах. Следует отметить, что в отличие от энтальпии образования, энтропия простого вещества, даже находящегося в кристаллическом состоянии, не равна нулю, т.к. при температуре, отличающейся от абсолютного нуля, макросостояние кристалла может быть реализовано не единственным макросостоянием, а большим числом равновероятных состояний.
Другая формулировка второго закона термодинамики выглядит так: полная энтропия всегда увеличивается в самопроизвольном процессе.
Увеличение энтропии ΔS при протекании процесса должно превышать или быть равным отношению количества теплоты Q, переданного системе, к температуре Т, при которой теплота передаётся:
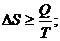
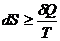 . (26)
. (26)
Уравнение (26) является математической записью второго начала термодинамики. В данном уравнении знак неравенства относится к необратимым самопроизвольным процессам, а знак равенства – к обратимым процессам.
Согласно уравнению (26), изменение энтропии при обратимом переходе системы из состояния 1 в состояние 2 можно определить как:
ΔS = S2 – S1 = 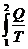 . (27)
. (27)
Фазовые переходысопровождаются тепловым эффектом, называемым теплотой фазового перехода ΔНф.п., и являются изотермическими процессами (Тф.п.= const). Для фазового перехода одного моля вещества изменение энтропии равно:
ΔSф.п.= 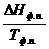 . (28)
. (28)
В процессах плавления, испарения жидкости или сублимации вещества энтропия увеличивается, так как разрушается упорядоченная кристаллическая решётка. Обратные процессы: кристаллизации, конденсации, десублимации сопровождаются уменьшением неупорядоченности в системе, и следовательно, уменьшением энтропии.
При изменении температурывещества от Т1 до Т2 при постоянном давлении изменение энтропии определяется по формуле:
ΔS = 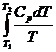 , (29)
, (29)
поскольку Ср = const, то
ΔS = Ср· ln 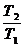 . (30)
. (30)
Для изохорных процессов
ΔS = 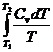 , (31)
, (31)
при Сv = const
ΔS = Сv· ln 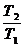 . (32)
. (32)
Стандартной энтропией ΔS 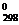 называется энтропия 1 моля вещества в стандартных условиях. Изменение стандартной энтропии ΔS
называется энтропия 1 моля вещества в стандартных условиях. Изменение стандартной энтропии ΔS 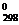 при протекании химической реакции можно рассчитать по уравнению, основываясь на следствии из закона Гесса:
при протекании химической реакции можно рассчитать по уравнению, основываясь на следствии из закона Гесса:
ΔS 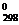 =
= 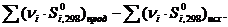 (33)
(33)
Наиболее хаотичной формой вещества является газообразное состояние, поэтому если в результате химической реакции число молей газа увеличивается, то хаотичность, а следовательно, и энтропия системы возрастает.
Обычно определяют не абсолютн6ое значение энтропии, а её изменение (S2 – S1) в том или ином процессе. Для вычисления изменения энтропии при переходе одного моля идеального газа из одного состояния в другое используют формулы:
S2 – S1 = R 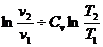 (34)
(34)
S2 – S1 = R 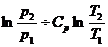 (35),
(35),
где Ср и Сv – постоянные величины. Изменение энтропии при нагревании единицы массы вещества, находящегося в твёрдом или жидком состоянии, рассчитывают по формуле:
S2 – S1 = 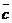 ln
ln 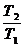 (36),
(36),
где 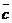 - удельная теплоёмкость вещества.
- удельная теплоёмкость вещества.
При переходе вещества из одного агрегатного состояния в другое изменение энтропии определяется по формуле:
S2 – S1 = 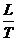 (37),
(37),
где L – скрытая теплота обратимого фазового перехода (испарения, плавления и др.); Т – температура фазового перехода.
Вариант 1
1. Рассчитайте тепловой эффект реакции при 298 К и постоянном давлении:
2Н2 + СО = СН3ОН(ж)
Стандартные энтальпии образования веществ возьмите из справочника.
2. Укажите знак ΔS 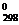 для реакции:
для реакции:
NH3(г) + HCl(г) = NH4Cl(к).
3. Каково изменение энтропии при охлаждении 5 молей воды от температуры кипения до температуры замерзания при 1 атм.; считая теплоёмкость воды постоянной и равной 17,96 Дж/моль·К.
4. Определите возможность самопроизвольного протекания химической реакции при стандартных условиях, для которой ΔН0 = -50 кДж/моль, ΔS0 = 18 Дж/моль∙К.
Вариант 2
1. Рассчитайте тепловой эффект реакции при 298 К и постоянном давлении:
4НСl + O2 = 2H2O(ж) + 2Cl2
Стандартные энтальпии образования веществ возьмите из справочника.
2. Укажите знак ΔS 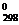 для реакции:
для реакции:
COCl2(г) = CO(г) + Cl2(г).
3. Каково изменение энтропии при конденсации 1 моля паров ртути при температуре кипения (630 К), если её теплота испарения 59,36 кДж/моль.
4. Для некоторой реакции ΔН0 = 100 кДж/моль, а ΔS0 = 40 Дж/моль∙К. При какой температуре установится равновесие, если ΔН0 и ΔS0 от температуры не зависят?
Вариант 3
1. Рассчитайте тепловой эффект реакции при 298 К и постоянном давлении:
4NH4Cl(тв) = NH3 + HCl
Стандартные энтальпии образования веществ возьмите из справочника.
2. Укажите знак ΔS 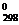 для реакции:
для реакции:
PCl3(г) + Cl2(г) = PCl5(г).
3. Каково изменение энтропии при охлаждении4,4 г газообразного диоксида углерода от 600 К до 300 К (средняя молярная теплоёмкость в этом интервале температур равна 37,07 Дж/моль·К).
4. Тепловой эффект некоторой реакции ΔН0 = +50 кДж/моль и не зависит от температуры; при температуре 1250 К в системе установилось равновесие. Чему равно изменение энтропии в ходе этой реакции?
Вариант 4
1. Рассчитайте тепловой эффект реакции при 298 К и постоянном давлении:
2N2 + 6H2О(ж) = 4NH3 + 3O2
Стандартные энтальпии образования веществ возьмите из справочника.
2. Укажите знак ΔS 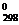 для реакции:
для реакции:
2NO2(г) + O2(г) = 2NO(г).
3. Каково изменение энтропии при превращении 1 моля льда в воду при 0º С?
4. Изменение стандартной свободной энергии Гиббса для одной реакции ΔG 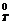 = -25 кДж/моль, а для другой - ΔG
= -25 кДж/моль, а для другой - ΔG 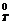 = 35 кДж/моль. Какая из двух реакций характеризуется большей величиной константы равновесия? Какая реакция протекает полнее?
= 35 кДж/моль. Какая из двух реакций характеризуется большей величиной константы равновесия? Какая реакция протекает полнее?
Вариант 5
1. Рассчитайте тепловой эффект реакции при 298 К и постоянном давлении:
2NO + 6H2О(ж) = 4NH3 +
