Тема: «Химическая кинетика и равновесие»
1. Химическое равновесие реакции СОСl2(г) <=> СО(г) + Сl2(г) установилось при концентрациях реагирующих веществ (моль/л):  = 10; ССO=2;
= 10; ССO=2; 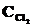 = 4. В равновесную систему добавили хлор в количестве 4моль/л. Определить новые равновесные концентрации реагирующих веществ после смещения равновесия.
= 4. В равновесную систему добавили хлор в количестве 4моль/л. Определить новые равновесные концентрации реагирующих веществ после смещения равновесия.
2. В каком направлении сместится равновесие реакции
СН4(г) + Н2О(г) <=> СО(г) + ЗН2(г) при уменьшении объёма в 3 раза?
3. В каком направлении сместится равновесие реакции
2СО + 2Н2 <=> СН4 + СО2, если концентрации всех реагирующих веществ уменьшить в 3 раза?
4. Реакция протекает по уравнению 4НС1 + О2 <=> 2Н2О + 2Сl2. В каком направлении сместится химическое равновесие, если концентрацию всех реагирующих веществ увеличить в 2 раза?
5. Определить равновесные концентрации водорода и йода в реакции Н2 + J2 <=> 2HJ, если их начальные концентрации составляли по 0,02 моль/л, а равновесная концентрация HJ равна 0,03 моль/л. Вычислить константу равновесия.
6. Константа равновесия реакции: N2 + ЗН2 <=> 2NН3, Кр = 0,1 при 673К. Равновесные концентрации (моль/л): 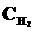 = 0,6;
= 0,6; 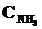 = 0,18. Вычислить начальную и равновесную концентрации азота .
= 0,18. Вычислить начальную и равновесную концентрации азота .
7. При 393К реакция заканчивается за 18мин. Через сколько времени эта реакция закончится при 453К, если температурный коэффициент скорости реакции равен З?
8. Реакция протекает по уравнению
Nа2S203 + Н2S04 = Nа2S04 + Н2S03 + S. Как изменится скорость реакции после разбавления реагирующей смеси в 4 раза?
9. В начальный момент протекания реакции N2 + ЗН2 <=> 2NН3 концентрации были равны (моль/л): 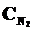 = 1,5;
= 1,5; 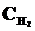 = 2,5;
= 2,5; 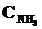 = 0. Каковы концентрации азота и водорода тогда, когда концентрация аммиака 0,5моль/л?
= 0. Каковы концентрации азота и водорода тогда, когда концентрация аммиака 0,5моль/л?
10. В реакции N2 + ЗН2 <=> 2NН3 равновесие установилось при следующих концентрациях реагирующих веществ (моль/л): СN2 = 2,5; СH2 = 1,8; СNH3 = 3,6. Рассчитайте константу равновесия этой реакции и исходные концентрации азота и водорода.
11. Начальные концентрации веществ в реакции
СО(г) + Н2О(г) <=> СО2(г) + Н2(г) были равны (моль/л): Ссо = 0,5; СH2O =0,6; СCO2 = 0,4; СH2 = 0,2. Вычислить концентрации всех участвующих веществ в реакции после того, как прореагировало 60% Н2О.
12. Реакция идёт по уравнению 4NН3 + 5О2 <=> 4NО + 6Н2О. Как изменится скорость реакции, если увеличить давление в 2 раза?
13. Определите, как изменится скорость прямой реакции
2SО2 + О2 <=> 2SО3, если общее давление в системе увеличить в 4 раза?
14. Напишите выражение для константы равновесия обратимой реакции FеС13(р) + ЗКСNS(р) <=> Fе(СNS)3(р) + ЗКС1(р). В каком направлении будет смещаться равновесие при добавлении к системе соответственно KCNS; FеС13; КС1 и как это отразится на окраске системы? Fе(СNS)3 имеет интенсивно красную окраску.
15. В смеси NО2 (бурого цвета) и N2O4 (бесцветен) протекает обратимая реакция: 2NО2 <=> N2O4, ∆Н= –54,3кДж. Как будет влиять изменение температуры на состояние равновесия системы? Как это скажется на изменение окраски смеси?
16. В каком направлении произойдет смещение равновесия системы N2 + ЗН2 <=> 2NН3, ∆Н= –92кДж при понижении температуры Как объяснить, что на практике синтез аммиака ведут при повышенной температуре (не ниже 400 –500°С).
17. Исходные концентрации окиси азота и хлора в системе
2NО(г)+Сl2(г)<=>2NОС1(г) составляют соответственно 0,5 моль/л и 0,2 моль/л. Вычислить константу равновесия, если к моменту наступления равновесия прореагировало 20% окиси азота.
18. Во сколько раз следует увеличить давление, чтобы скорость образования NО2 по реакции 2NO(г)+О2<=>2NО2(г) возросла в 1000 раз?
19 Во сколько раз изменится скорость прямой и обратной реакции в системе 2SО2(г) + О2(г) <=> 2SО3(г), если объём газовой смеси уменьшить в 3 раза. В какую сторону сместится равновесие системы.
20. Константа равновесия гомогенной системы
СО(г) + Н2О(г) <=> СО2(г) + Н2(г), при 850°С равна 1. Вычислить концентрации всех веществ при равновесии, если исходные концентрации СО и Н2О соответственно равны 3моль/л и 2моль/л.
21. Реакция идёт по уравнению Н2(г) + J2(г )= 2HJ(г). Константа скорости этой реакции при 508°С равна 0,16 Исходные концентрации реагирующих веществ Н2 и J2 были соответственно 0,04моль/л и 0,05 моль/л. Вычислить начальную скорость реакции и скорость её, когда концентрация H2 стала равной 0,03 моль/л.
22. Напишите выражение для константы равновесия гетерогенной системы СO2(г) + C(т) <=> 2СО(г). Как изменится скорость прямой реакции, если концентрацию СО2 уменьшить в 4 раза. Как следует изменить давление, чтобы повысить выход СО.
23. Напишите выражение для константы равновесия гетерогенной системы С(т) + Н2О(г) <=> СО(г) + Н2(г). Как следует изменить концентрацию и давление, чтобы сместить равновесие в сторону обратной реакции.
24. Константа равновесия реакции FеО(к) + СО(г) <=> Fе(к) + СО2(г) при некоторой температуре равна 0,5. Найти равновесные концентрации СО и СО2, если начальные концентрации этих веществ соответственно равны 0,05моль/л и 0.01моль/л.
25. Напишите выражения для констант равновесия следующих реакций: 2Н2(г) + О2(г) <=> 2Н2О(г), ∆Н = –483,6кДж
С(графит) + Н2О(г) <=> СО(г) + Н2(г), ∆Н = 131,3кДж.
Как повлияет на равновесие этих реакций
а) повышение температуры;
б) повышение давления.
26. При некоторой температуре в реакции 2SО2 + О2 <=> 2SО3 установилось равновесие при следующих концентрациях веществ (моль/л): 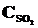 = 0,04,
= 0,04, 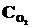 = 0,06,
= 0,06, 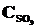 = 0,02. Вычислить константу равновесия этой реакции и исходные концентрации SО3 и О2.
= 0,02. Вычислить константу равновесия этой реакции и исходные концентрации SО3 и О2.
27. Напишите выражение константы равновесия реакции:
CO2(г) + С(графит) <=> 2СО(г), ∆Н = 172,5кДж. В каком направлении произойдет смещение равновесия этой реакции:
а) при повышении давления;
б) при повышении температуры;
в) при повышении концентрации СО.
28. Для реакции: 2SO2 + O2 <=> SO3 начальные концентрации исходных веществ были равны 1,6 моль/л – SO2 и 1,2 моль/л – О2. Вычислите константу равновесия этой реакции, если равновесная концентрация SO3 равна 0,6 моль/л?
29. Напишите выражение константы равновесия реакции:
2H2(г) + С(графит) <=> СН4(г), ∆Н= –74,9кДж.
В каком направлении произойдет смещение равновесия этой реакции:
а) при добавлении Н2;
б) при повышении давления;
в) при охлаждении.
30. Вычислить константу равновесия реакции CO + Cl2 <=> COCl2 если известно, что начальные концентрации CO и Cl2 были равны соответственно 0,28моль/л и 0,09моль/л, а равновесная концентрация СО равна 0,2моль/л.
Контрольное задание № 5
