Количественные соотношения в химии
Строение вещества
Одним из основных понятий химии и других естественных наук является атом. Этот термин имеет давнее происхождение; он насчитывает уже около 2500 лет. Впервые понятие атома зародилось в Древней Греции, примерно в V в. до н. э. Основоположниками атомистического учения были древнегреческие философы Левкипп[1] и его ученик Демокрит. Именно они выдвинули идею о дискретном строении материи и ввели термин «АТОМ». Демокрит определял атом как наименьшую, далее неделимую, частицу материи.
Учение Демокрита не получило широкого распространения, и в течение большого исторического периода в химии (а во времена средневековья –
алхимии) господствовала теория Аристотеля (384 – 322 гг. до н. э.). Согласно учению Аристотеля, основными началами природы являются абстрактные «принципы»: холод, тепло, сухость и влажность, при комбинации которых образуются четыре основных «элемента-стихии»: земля, воздух, огонь
и вода.
И только в начале XIX столетия английский ученый Джон Дальтон возвращается к атомам как наименьшим частицам материи и вводит в науку этот термин. Этому предшествовали работы таких замечательных ученых, как Р. Бойль (в книге «Химик-скептик» он нанес сокрушительный удар по представлениям алхимиков), Дж. Пристли и К. В. Шееле (открытие кислорода), Г. Кавендиш (открытие водорода), А. Л. Лавуазье (попытка составить первую таблицу простых веществ), М. В. Ломоносов (основные положения атомно-молекулярного учения, закон сохранения массы), Ж. Л. Пруст (закон постоянства состава) и многие другие.
Открытия в области физики, сделанные в конце XIX – первой трети ХХ столетий, заставили ученых совершенно иначе смотреть на атомно-молекулярное учение. Оказалось, что атом обладает сложным строением и не является наименьшей частицей материи.
Здесь мы не будем приводить устаревшее определение этого понятия, а сразу дадим формулировку, базирующуюся на современных представлениях.
Атом (греч. atomoz – неделимый) – это наименьшая частица химического элемента, способная к самостоятельному существованию и являющаяся носителем его свойств. Атом представляет собой электронейтральную микросистему, состоящую из положительно заряженного ядра и соответствующего числа электронов.
Химический элемент – вид атомов с одинаковым зарядом ядра.
Химический элемент – это понятие, а не материальная частица. Это не атом, а совокупность атомов, характеризующихся определенным признаком – одинаковым зарядом ядра.
Электрон [др.греч. hlektron – янтарь (хорошо электризуется при трении)] – стабильная элементарная частица, имеющая массу покоя, равную 9,109 × 10–31 кг = 5,486 × 10–4 а. е. м.[2], и несущая элементарный отрицательный заряд, равный 1,6 × 10–19 Кл.
В химии и в физике при решении многих задач заряд электрона принимают за – 1 и заряды всех остальных частиц выражают в этих единицах. Электроны входят в состав всех атомов.
Протон (греч. prwtos – первый) – элементарная частица, являющаяся составной частью ядер атомов всех химических элементов, обладает массой покоя mp =1,672 × 10–27 кг = 1,007 а. е. м. и элементарным положительным электрическим зарядом, равным по величине заряду электрона, т. е. 1,6 × 10–19 Кл.
Число протонов в ядре определяет порядковый номер химического элемента.
Нейтрон (лат. neutrum – ни то, ни другое) – электрически нейтральная элементарная частица с массой покоя, несколько превышающей массу покоя протона mn = 1,675 × 10–27 кг = 1,009 а. е. м.
Наряду с протоном нейтрон входит в состав всех атомных ядер (за исключением ядра изотопа водорода 1Н, представляющего собой один протон).
Таблица 1
Некоторые характеристики элементарных частиц,
входящих в состав атома
| Элементарная частица | Обозначение | Масса | Электрический заряд | ||
| в ед. СИ(кг) | в а. е. м. | в Кл | в зарядах электрона | ||
| Электрон | e– | 9,109 × 10–31 | 5,468 × 10–4 | 1,6 × 10–19 | –1 |
| Протон | p | 1,672 × 10–27 | 1,007 | 1,6 × 10–19 | |
| Нейтрон | n | 1,675 × 10–27 | 1,009 |
Обобщающее (групповое) название протонов и нейтронов – нуклоны.
Массовое число – общее число нуклонов (протонов и нейтронов) в ядре.
Ядро атома состоит из протонов, число которых равно порядковому номеру элемента (Z), и нейтронов (N). A = Z + N, где A – массовое число.
Нуклиды (лат. nucleus – ядро) – общее название атомных ядер, характеризуются определенным числом протонов и нейтронов (величиной положительного заряда и массовым числом).
Для того чтобы указать химический элемент, достаточно назвать только одну величину – заряд ядра, т. е. порядковый номер элемента в Периодической системе. Для определения нуклида этого недостаточно – надо указать также и его массовое число.
Иногда, не совсем точно, понятие «нуклид» относят не к самому ядру, а ко всему атому.
Изотопы (греч. isoz – одинаковый + topoz – место) – нуклиды, имеющие одинаковое число протонов, но различающиеся массовыми числами.
Изотопы – нуклиды, занимающие одно и то же место в Периодической системе, т. е. атомы одного и того же химического элемента.
Например: 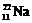 ,
,  ,
, 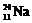 – изотопы натрия.
– изотопы натрия.
Изобары (греч. izo – равный + baros – вес) – нуклиды, имеющие одинаковые массовые числа, но различное число протонов (т. е. относящиеся к различным химическим элементам), например, 90Sr, 90Y, 90Zr.
Изотоны – нуклиды с одинаковым числом нейтронов.
Довольно долго химики не делали четкого различия между атомами и молекулами простых веществ. В 1811 г. А. Авогадро предложил гипотезу, которая позволяла однозначно определить эти понятия, однако современники ее не оценили, и она получила признание только в 1860 г., после состоявшегося в Карлсруэ (Германия) первого международного съезда химиков, когда молекула стала пониматься как мельчайшая частица вещества, участвующая в его химических превращениях. По мере развития естественных наук определение молекулы претерпело некоторые изменения.
Молекула (уменьшительное от лат. moles – масса) – это наименьшая частица вещества, определяющая его свойства. Состоит из атомов одного или различных химических элементов и существует как единая система атомных ядер и электронов. В случае одноатомных молекул (например, благородных газов) понятия атома и молекулы совпадают.
Атомы удерживаются в молекуле с помощью химических связей.
В химии, кроме атомов и молекул, приходится рассматривать и другие структурные единицы: ионы и радикалы.
Ионы (греч. ion – идущий) – электрически заряженные частицы, образовавшиеся из атомов (или атомных групп) в результате присоединения или потери электронов.
Положительно заряженные ионы называются катионами (греч. kata – вниз + ион), отрицательно заряженные – анионами (греч. ana – вверх + ион).
Например, K+ – катион калия, Fe2+ – катион железа, 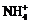 – катион аммония, Cl– – анион хлора (хлорид-анион), S2– – анион серы (сульфид-анион),
– катион аммония, Cl– – анион хлора (хлорид-анион), S2– – анион серы (сульфид-анион), 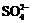 – сульфат-анион.
– сульфат-анион.
Радикалы (лат. radicalis – коренной) – частицы (атомы или группы атомов) с неспаренными электронами.
Они обладают высокой реакционной способностью. Например, H × – радикал водорода, Cl × – радикал хлора, × CH3 – радикал-метил. В то же время парамагнитные молекулы, например, O2 , NO, NO2 , имеющие неспаренные электроны, не являются радикалами.
Простое вещество – вещество, состоящее из атомов одного химического элемента.
Простое вещество – это форма существования химического элемента. Многие элементы могут существовать в виде нескольких простых веществ, например, углерод (графит, алмаз, карбин, фуллерены), фосфор (белый, красный, черный), кислород (озон, кислород).
Известно около 400 простых веществ.
Аллотрóпия (греч. allos – другой + trope – поворот) – способность химического элемента существовать в виде двух или нескольких простых веществ, отличающихся количеством атомов в молекуле (например, O2 и O3) или разной структурой кристаллов (графит и алмаз).
Полиморфизм (греч. polimorjos – многообразный) – способность твердых веществ существовать в двух или нескольких формах с различной кристаллической структурой и различными же свойствами. Такие формы называются полиморфными модификациями.
Например, FeS2 может образовывать два вещества с различными кристаллическими структурами (полиморфные модификации): одно называется пирит, а другое – марказит. Являются ли эти вещества аллотропными модификациями? Не являются.
Аллотропия относится только к простым веществам и рассматривает как различие в составе их молекул, так и различие в строении кристаллических решеток. Если речь идет о различии в строении кристаллических решеток простых веществ, то понятия полиморфизм и аллотропия совпадают, например, о графите и алмазе можно сказать, что это аллотропные формы, а можно – полиморфные формы.
Возможность образования двух и более видов молекул,
содержащих различное число атомов
Кислород. Образует две аллотропные формы: O2 и O3 – озон. Они различаются как по физическим, так и по химическим свойствам.
Кислород O2 – бесцветный газ, без запаха. Озон O3 – газ голубого цвета с характерным запахом (даже свое название он получил от греч. wzein (ozein) – пахнуть).
В жидком и твердом состояниях кислород окрашен в бледно-голубой цвет. Озон в жидком состоянии интенсивно окрашен в фиолетовый цвет, в твердом состоянии имеет черно-фиолетовый цвет.
Кислород парамагнитен, озон диамагнитен.
Таблица 2
Температуры фазовых переходов О2 и О3
| Ткипения,°С | Тплавления,°С | плотность, г/см3 | |
| О2 | -182,8 | -218,2 | ж. 1,14 |
| О3 | -112 | -193 | ж. 1,51 |
По химической активности кислород и озон резко различаются. Озон более реакционноспособен, чем кислород, и проявляет более сильные окислительные свойства.
Несмотря на то, что кислород взаимодействует почти со всеми элементами в свободном виде, во многих случаях эти реакции протекают только при повышенной температуре. Озон же реагирует со многими веществами в таких условиях, когда кислород остается инертным, например,
O3 + 2 KI + H2O = O2 + I2 + 2 KOH
PbS + 2 O3 = PbSO4 + O2
Озон окисляет ртуть и серебро в оксиды.
Фосфор. Известны две аллотропные формы фосфора: белая и красная. Белый фосфор состоит из тетраэдрических молекул P4 . Красный фосфор можно рассматривать как полимерные молекулы P. Безусловно, в твердом состоянии эти модификации отличаются и строением кристаллических решеток, и физическими свойствами.
Все аллотропные формы фосфора также проявляют значительное различие и в химических свойствах, которые, прежде всего, заключаются в их различной реакционной способности. Белый фосфор – более активная, а красный – менее активная формы.
Белый фосфор медленно окисляется на воздухе уже при обычной температуре (чем обусловлено свечение белого фосфора), в то время как красный устойчив на воздухе и загорается только при нагревании.
Образование различных кристаллических решеток
Этот случай аллотропии можно рассматривать также и как полиморфизм простых веществ.
Углерод. Для углерода известно несколько аллотропных модификаций: графит, алмаз, карбин, фулерены.
Графит и алмаз образуют атомные кристаллические решетки, различающиеся по строению. Эти два вещества резко различаются и по своим физическим свойствам: алмаз бесцветный, прозрачный, графит черно-серого цвета, непрозрачный, алмаз – самое твердое вещество, графит – мягкий, алмаз не проводит электрический ток, графит проводит электрический ток. При обычных условиях алмаз является метастабильной (менее устойчивой) формой. При нагревании алмаза (t > 1 000°С) он необратимо переходит в графит. Переход графита в алмаз протекает при более высокой температуре и обязательно при очень высоком давлении.
Олово. Хорошо известны две аллотропные формы олова – серое и белое.
Серое олово (a-олово) существует при температуре ниже 13,2°С, проявляет полупроводниковые свойства, очень хрупкое вещество с плотностью 5,846 г/см3.
Белое олово (b-олово) – по физическим свойствам типичный металл серебристо-белого цвета, хорошо проводит тепло и электрический ток, пластичный, плотность 7,295 г/см3 устойчиво в интервале температур 13,2 – 173°С. Выше этой температуры b-олово переходит в другую модификацию –
d-олово, которое имеет другое строение кристаллической решетки и плотность 6,54 г/см3.
Многие полиморфные (или аллотропные) модификации могут находиться в метастабильном состоянии, т. е. существовать продолжительное время при условиях для них не характерных («в чужой области»).
Например, белое олово может переохлаждаться и существовать продолжительное время при температуре ниже 13,2°С, однако его состояние при этих условиях неустойчиво, поэтому механические повреждения, резкое сотрясение и т. п. могут вызвать резкий переход в a-форму. Это хорошо известное явление назвали «оловянной чумой». Примеси также оказывают существенное влияние на переход из одной формы в другую. Например, незначительная примесь висмута практически предотвращает переход белого олова в серое, а добавка алюминия, наоборот, ускоряет этот переход.
Для каждой аллотропной (или полиморфной) формы существует свой определенный интервал температур и давлений, где эта модификация устойчива. Например, при температурах до 95,6°С устойчива ромбическая сера (a-форма), а при более высокой температуре – моноклинная (b-форма). Эти две аллотропные формы отличаются друг от друга строением кристаллических решеток.
Сложное вещество, или соединение – вещество, состоящее из атомов разных химических элементов.
Изоморфизм (греч. izo – равный, подобный + morje – форма) – способность сходных по составу веществ образовывать смешанные кристаллы, в которых близкие по размеру атомы, ионы или атомные группировки случайным образом замещают друг друга.
Например, в кристаллах алюмокалиевых квасцов KAl(SO4)2 × 12 H2O ионы калия могут быть замещены ионами рубидия или аммония, а ионы Al3+ ионами Cr3+ или Fe3+. В этом случае говорят, что катионы калия изоморфны катионам рубидия или аммония, а катионы алюминия изоморфны катионам хрома или железа.
Задачи с разбором
1. Сколько атомов водорода содержится в 1 л водорода при н. у.?
Решение. Т. к. 1 моль любого идеального газа занимает при н. у. 22,4 л, то в 1 л водорода (мы можем считать его приближенно идеальным газом) будет содержаться 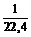 = 0,045 моль молекул водорода. Каждая молекула водорода состоит из двух атомов, значит, количество атомов в два раза больше: 2 × 0,045 = 0,09 моль. Чтобы найти, сколько атомов находится в этом количестве вещества, умножим его на число Авогадро:
= 0,045 моль молекул водорода. Каждая молекула водорода состоит из двух атомов, значит, количество атомов в два раза больше: 2 × 0,045 = 0,09 моль. Чтобы найти, сколько атомов находится в этом количестве вещества, умножим его на число Авогадро:
0,09 × 6,022 × 1023 = 5,4 × 1022 штук.
2. Какова масса 1 молекулы NaOH?
Решение. Рассчитаем сначала молекулярную массу NaOH в единицах а. е. м., исходя из значений атомных масс натрия, кислорода и водорода.
Mr(NaOH) = 23 + 16 + 1 = 40 а. е. м.
А теперь переведем в единицы СИ:
40 × 1,6606 × 10–27 = 6,64 × 10–26 кг.
3. Какая энергия выделяется при образовании атома гелия из элементарных частиц?
Решение. Атомная масса гелия 4,0026 а. е. м. Рассчитаем суммарную массу элементарных частиц, составляющих гелий:
2mp + 2mn + 2me = 2(1,007 + 1,009 + 5,5 × 10–4) = 4,0331 а. е. м.
Дефект массы составляет
4,0331 – 4,0026 = 3,05 × 10–2 а. е. м.
или
3,05 × 10–2 × 1,6606 × 10–27 = 5,1 × 10–29 кг.
Е = Dmc2 = 5,1 × 10–29 × (3 × 108)2 = 4,6 × 10–13 Дж.
4. А г СаО растворили в избытке воды массой В г. Выразите массовую долю вещества в полученном растворе.
Решение. Для решения этой задачи необходимо помнить, что при растворении оксида кальция в воде происходит реакция СаО + Н2О = Са(ОН)2, поэтому растворенным веществом будет гидроксид кальция.
w = 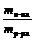 (´ 100%).
(´ 100%).
Массу вещества найдем по уравнению реакции:
m(Са(ОН)2) = М(Са(ОН)2) × 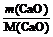 = 74 ×
= 74 ×  = 1,32А.
= 1,32А.
Масса раствора складывается из массы веществ, образовавших этот раствор (поскольку в результате реакции не выпадает осадок и не выделяется газ, ничего вычитать не требуется) A + B. Таким образом, w = 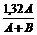 (´ 100%).
(´ 100%).
5. Смешали 11,2 л хлора и 22,4 л водорода. Найдите объемные доли газов в смеси после прохождения реакции.
Решение. Протекает реакция H2 + Cl2 = 2 HCl. Так как объемы газов пропорциональны их количествам веществ, то 1 объем водорода будет реагировать с 1 объемом хлора, при этом образуются 2 объема хлороводорода. Хлор в недостатке, он прореагирует полностью; 11,2 л водорода вступит в реакцию и еще 11,2 л останется. Хлороводорода получится 2 × 11,2 = 22,4 л.
Суммарный объем системы 11,2 + 22,4 = 33,6 л. Объемная доля водорода 11,2 / 33,6 = 0,33 (33%), хлороводорода 22,4 / 33,6 = 0,67 (67%), или
100 – 33 = 67%.
6. В сплаве содержится 40 % K и 60 % Na. Найдите мольные доли компонентов.
Решение. М(K) = 39, M(Na) = 23. Если в 100 г сплава содержится 40 г K, то это составляет 40 / 39 = 1,03 моль. 60 г натрия – это 60 / 23 = 2,61 моль. Общее количество вещества в 100 г сплава 1,03 + 2,61 = 3,64 моль. Отсюда мольные доли: калия 1,03 / 3,64 = 0,28 (28%), натрия 2,61 / 3,64 = 0,72 (72%), или 100 – 28 = 72%.
7. Соединение углерода с водородом содержит 75 % углерода по массе. Найдите формулу этого соединения.
Решение. Напишем формулу в общем виде: СхНу . Масса углерода в молекуле этого вещества пропорциональна 12х, водорода – у. Т. к. массовая доля углерода 75%, получаем: 12х : у = 75 : 25, отсюда х : у = 6,25 : 25 = 1 : 4. Искомая формула СН4.
8. Плотность газа по воздуху 0,55. Что это за газ?
Решение. Средняя молярная масса воздуха 29. Чтобы найти молярную массу газа, умножим 29 на плотность газа: 29 × 0,55 = 16. Эта молярная масса соответствует метану СН4, других вариантов нет.
Задачи для решения
1. Суммарный заряд какого количества электронов составляет 1 Кл? Какова масса 1 моль электронов?
2. Сколько атомов водорода содержится в 3 л воды а) при 20°С и 1 атм; б) при 150°С и 1 атм?
3. Какая энергия выделится при образовании из элементарных частиц 1 моль нуклидов 16О?
4. В избытке воды объемом 1 лрастворили х г калия. Какова массовая доля вещества в полученном растворе?
5. 16,8 л хлороводорода и 5,6 л бромоводорода растворили в 100 мл воды. Найдите массовые доли веществ в растворе.
6. При 2000°С степень термической диссоциации (т. е. мольная доля молекул, распавшихся под действием тепла) воды составляет около 2%. Рассчитайте мольные и объемные доли всех компонентов в равновесной смеси при этой температуре.
7. Рассчитайте массовую долю спирта в водном растворе с объемной долей 40%, если плотность спирта (при 20°С) 0,79 г/мл.
8. Слили два раствора: 10 г 20% хлорида бария и 20 г 10% сульфата калия. Найдите массовые доли всех растворенных веществ.
9. В соединении азота с водородом содержится 87,5% азота по массе. Найдите формулу этого соединения.
10. Некий газ имеет плотность по водороду 8,5. Что это за газ?
11. Изобразите графические формулы азота, оксида железа (III), фосфорной кислоты.
Глава II
Строение атома
Ранние модели атома
Изучение прохождения электрического тока через различные среды (газы, растворы, расплавы), проводившееся в прошлом столетии, дало первые экспериментальные факты, натолкнувшие на мысль о сложном строении атома.
В 30-х годах XIX века английский физик Майкл Фарадей установил, что электрохимические процессы характеризуются определенными соотношениями, которые указывают на то, что электрические заряды, так же как и материя, имеют дискретный характер, и существует некий минимальный заряд.
Эксперименты с газоразрядными трубками, проведенные во второй половине прошлого века, с очевидностью показали, что в состав атомов должны входить отрицательно заряженные частицы, которые впоследствии были названы электронами[3]. Эти опыты с разреженными газами имели достаточно простое оформление. В стеклянную трубку впаивали два электрода, затем трубку вакуумировали до давления примерно 10 мм рт. ст. (0,013 Па). На электроды подавали высокое напряжение (несколько киловольт) и по свечению стенок трубки и остаточных газов наблюдали поток частиц, которые перемещались от отрицательного электрода к положительному. Если на пути этого пучка устанавливали какое-либо препятствие, например, вертушку, то она начинала вращаться, указывая, что частицы имеют конечную массу. Если газоразрядную трубку помещали между пластинами плоского конденсатора, то поток частиц отклонялся к одной из них, а именно к той, которая заряжена положительно, что говорило об отрицательном заряде частиц.
В 1896 году Анри Беккерель, работая с соединениями урана, открыл явление радиоактивности – самопроизвольного распада атомов одного элемента и превращения их в атомы другого химического элемента. При этом было обнаружено, что такие превращения сопровождаются испусканием невидимых глазом излучений.
Несколько позже супруги Пьер Кюри и Мария Склодовская-Кюри обнаружили, что невидимое излучение испускают не только соединения урана, но и другие вещества. В результате кропотливой работы ими были открыты два новых химических элемента, которые были названы “радий” и “полоний”.
В 1899 г. Резерфорд обнаружил, что радиоактивные элементы испускают два вида излучений, которые он назвал a- и b-лучи. Позже было установлено, что радиоактивные вещества могут испускать три вида излучений: a, b и g. a-излучение представляет собой поток ядер атомов гелия и, соответственно, a-частицы имеют массу 4 а. е. м. и электрический заряд +2, b-лучи – это поток электронов, а g-лучи – электромагнитное излучение с очень короткой длиной волны[4].
Все эти экспериментальные факты говорили о том, что атом имеет сложное строение и в его состав должны входить электроны. А т. к. атом в целом является электронейтральной частицей, то отрицательный заряд электронов должен компенсироваться положительным зарядом.
Около 1900 г. Дж. Дж. Томсон предлагает первую модель атома, согласно которой положительный заряд равномерно заполняет весь объем атома, а отрицательный, представленный электронами, вкраплен в эту положительно заряженную сферу. Эта модель получила название «пудинг Томсона». Все полученные к тому времени экспериментальные данные модель объяснить не могла. Она в какой-то мере объясняла опыты Фарадея и эксперименты с газоразрядными трубками, но не могла ответить на самый главный вопрос: «как вообще может существовать такая система электрических зарядов?»[5] Несмотря на это, ученые некоторое время пользовались этой моделью.
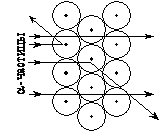
Рис. 1. Опыт по прохождению a-частиц через вещество.
В 1910 г. студенты Резерфорда Ханс Гейгер и Эрнест Марсден проводили эксперименты по бомбардировке a-частицами тонких металлических пластинок. Они обнаружили, что большинство a-частиц проходят через фольгу, не изменяя своей траектории. И это было неудивительно, если принять правильность модели атома Томсона.
Удивительным было как раз то, что некоторые частицы отклонялись от первоначальной траектории и к всеобщему удивлению примерно 1 из 20 000 a-частиц отклонялась на угол близкий к 180°, т. е. отскакивала обратно (см. рис. 1).
Из результатов этого эксперимента можно было сделать следующие выводы:
1) в атоме есть некоторое «препятствие», которое было названо ядром;
2) ядро имеет положительный заряд (иначе положительно заряженные a-частицы не отражались бы назад);
3) ядро имеет очень маленькие размеры по сравнению с размерами самого атома (лишь незначительная часть a-частиц изменяла направление движения);
4) ядро имеет большую массу, по сравнению с массой a-частиц.
Эксперименты по рассеянию a-частиц позволили также оценить размеры ядер и атомов:
‑ ядра имеют диаметры порядка 10–15 – 10–14 м,
‑ атомы имеют диаметры порядка 10–10 м.
Для объяснения полученных результатов Резерфорд выдвинул идею планетарного строения атома. Он рассматривал атом как подобие Солнечной системы: в центре – ядро, содержащее основную массу и весь положительный заряд атома, а вокруг, по разным орбитам, вращаются электроны. Эта модель довольно хорошо объясняла накопившийся к тому времени экспериментальный материал, но страдала двумя недостатками:
1) В соответствии с уравнениями классической электродинамики заряженная частица, движущаяся с ускорением (а электрон в атоме движется с центростремительным ускорением), должна излучать энергию. При этом потеря энергии должна приводить к уменьшению радиуса орбиты и падению электрона на ядро.
2) Непрерывное изменение траектории электрона должно способствовать и непрерывному изменению частоты излучения и, следовательно, непрерывному спектру испускания. Но эксперименты показывали, что спектр испускания водорода, а также других атомов, находящихся в газообразном состоянии, состоит из нескольких полос, т. е. имеет дискретный характер.
Выход из создавшегося положения был найден в 1913 году датским физиком Нильсом Бором, который предложил свою теорию строения атома. При этом он не отбрасывал полностью прежние представления о планетарном строении атома, но для объяснения устойчивости такой системы сделал предположение, что законы классической физики не всегда применимы для описания таких систем, как атомы, и сформулировал два постулата.
Первый постулат Бора. Электроны могут вращаться вокруг ядра по строго определенным стационарным орбитам, при этом они не излучают и не поглощают энергию.
Второй постулат Бора. При переходе с одной орбиты на другую электрон поглощает или испускает квант энергии.
Бор предположил, что момент импульса для электрона в атоме может принимать дискретные значения, равные только целому числу квантов действия 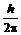 , что математически может быть записано так:
, что математически может быть записано так:
mvr = 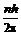 , (7)
, (7)
где m – масса электрона, v – линейная скорость его вращения, r – радиус орбиты, n – главное квантовое число, принимающее целочисленные значения от 1 до бесконечности, а h = 6,625 × 10–34 Дж/с – постоянная Планка. Уравнение (7) представляет собой математическое выражение первого постулата Бора.
Энергия электрона на соответствующей орбите определяется выражением:
E = 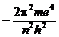 . (10)
. (10)
В этом уравнении, все величины, кроме n, являются константами. Таким образом, энергия электрона в атоме определяется значением главного квантового числа. Для атома водорода при n = 1, E = 2,176 × 10–18 Дж, или 13,6 эВ (1 электронвольт – это энергия, которую приобретает электрон, проходя разность потенциалов в 1 вольт, и равна 1,6 × 10–19 Дж).
Используя приведенные выше уравнения, Бор рассчитал спектр излучения атома водорода.
В атоме водорода электрон имеет минимальную энергию на первой орбите. Такое состояние электрона называется основным, или не возбужденным. Если этому электрону сообщить достаточную энергию, то он может перейти на другую орбиту с большим радиусом, например на орбиту № 2, 3 и т. д., в зависимости от сообщенной энергии. Такое состояние называется возбужденным, оно является неустойчивым. Электрон может находиться на этих орбитах непродолжительное время, а затем переходит на другую орбиту с меньшей энергией, в конечном итоге возвращаясь в основное состояние. При этих переходах происходит испускание энергии в виде электромагнитного излучения.
В 1900 г. Планк предположил, что излучение и поглощение энергии может происходить только строго определенными порциями, названными им квантами. Частота излучения связана с энергией уравнением:
E = hn или E =  , (11)
, (11)
где c – скорость света в вакууме равная 3 × 108 м/с. Поэтому частота этого излучения зависит от разности между энергиями уровней (DE ). В зависимости от длины волны l это излучение может относиться к различным областям спектра: рентгеновской, ультрафиолетовой, видимой или инфракрасной. На рис. 2 схематически показаны переходы электрона в возбужденном атоме водорода, которые вызывают излучение в различных областях спектра.
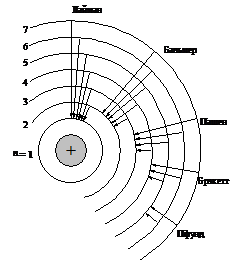
Рис. 2. Электронные переходы в атоме водорода,
соответствующие разным сериям.
Расчеты Бора оказались в великолепном согласии с результатами, полученными экспериментально (см. табл. 6).
Таблица 6
Длины волн спектральных линий в серии Бальмера (видимая область)
| l, нм (эксперимент) | l, нм (расчетные) |
| 656,466 | 656,47 |
| 486,271 | 486,28 |
| 434,171 | 434,17 |
| 410,291 | 410,293 |
| 397,12 | 397,123 |
При детальном изучении спектральных линий оказалось, что некоторые из них представляют собой не одну, а несколько близко расположенных линий. Это указывало на то, что существуют различные орбиты, на которых электроны имеют близкие значения энергий. Для объяснения этого факта Зоммерфельд предположил, что электроны могут вращаться не только по круговым, но и по эллиптическим орбитам.
Однако теория Бора не являлась универсальной. С ее позиций нельзя было описать поведение атома водорода в магнитном поле. Не удается также объяснить образование молекулы водорода, возникают непреодолимые трудности принципиального характера при описании многоэлектронных атомов. Боровская теория в химии практически не используется.
Указанные трудности можно преодолеть, если подходить к описанию строения атома с позиций более широкой теории – квантовой механики, рассматривающей поведение частиц в микромире. Законы, которые описывают явления, происходящие в микромире, существенно отличаются от законов, описывающих поведение макротел. Квантовое число n, которое было искусственно введено в теории Бора, оказывается с точки зрения квантовой теории неизбежным следствием более общих законов.
Двойственная природа микромира была впервые установлена для света. С одной стороны, для света характерны такие явления как интерференция и дифракция, которые могут быть объяснены только с позиций его волновой природы. С другой стороны, явление фотоэффекта с позиций этой теории описать невозможно. Это можно сделать, предположив для света корпускулярную (от лат. corpusculum – частица) природу. В 1905 г. Эйнштейн высказал мысль, согласно которой свет испускается в виде частиц, названных фотонами или квантами. Каждый фотон обладает энергией, определяемой уравнением (11).
Из корпускулярной природы света следовало, что фотоны должны обладать определенной массой. Масса покоя фотона равна нулю, а при движении фотон приобретает динамическую массу. Для вычисления этой массы Эйнштейн предложил уравнение эквивалентности массы и энергии:
E = mc2. (12)
Объединяя уравнения (11) и (12) получим:
m =  ; p = mc =
; p = mc = 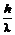
или
l = 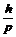 , (13)
, (13)
где p – импульс фотона.
В 1924 г. французский физик де Бройль исходя из представления о двойственной природе микромира, предположил, что электрон имеет определенную длину волны, которая укладывается на орбите целое число раз. Это означает, что 2pr = nl.
Предположение де Бройля в 1927 году получило экспериментальное подтверждение. Американские физики Девисон и Джермер наблюдали дифракцию электронов на кристаллах хлорида натрия.
В теорию Бора принцип квантования был введен произвольно. В ней в основном использовались законы классической механики. Открытие волновых свойств электрона, фотоэффект, опыты с абсолютно черным телом привели к созданию нового раздела физики – квантовой механики. Большую роль в ее создании сыграли Э. Шредингер и В. Гейзенберг.
Квантовомеханическая модель атома не такая наглядная, как модель, предложенная Бором, а математический аппарат квантовой механики несравненно сложнее. Поэтому основные положения квантовомеханической модели строения атома будут рассмотрены чисто качественно, без использования математического аппарата. Многое из того, что будет изложено в следующем разделе, читателю придется принять «на веру», без доказательств. Квантовые числа будут просто введены для описания поведения электрона в атоме, в то время как они являются следствием решения уравнения Шредингера.
Задачи с разбором
1. Могут ли электроны иона Rb+ находиться на следующих орбиталях: 1) 4р; 2) 3f; 3) 5s; 4) 5p?
Решение. Элемент Rb находится в главной подгруппе I группы V периода таблицы Менделеева, значит, у него начинает заполняться электронный уровень с главным квантовым числом n = 5: 5s1. У иона Rb+ внешний электрон потерян. Значит, ни на 5р, ни на 5s-орбиталях невозбужденного иона Rb+ электронов нет. Однако электроны могут переходить на эти орбитали при возбуждении атома.
Изобразим предпоследний уровень (n = 4): 4s2p6d 0f 0. На нем находится 8 электронов, как и у любого s-элемента (т. е. элемента главной подгруппы I или II группы Периодической таблицы, у которого заполняется s-подуровень). Почему 4d и 4f-подуровни пустые? Дело в том, что энергия 4d-подуровня выше, чем 5s, а 4f – даже выше, чем 6s, а сначала заполняются подуровни с меньшей энергией (правило Клечковского). Итак, электроны Rb+ могут находиться на 4р-орбиталях.
Осталось понять, могут ли они находиться на 3f-орбиталях. При n = 3 орбитальное квантовое число l принимает значения 0,1,2, которые соответствуют s, p и d-подуровням. А 3f-подуровня попросту не существует.
2. Приведите примеры трех частиц (атомы, ионы) с электронной конфигурацией 1s22s2p63s2p6.
Решение. Подходящий элемент Периодической системы – Ar (8 электронов на третьем – внешнем – электронном уровне). Ясно, что других атомов с такой электронной ко
