Диаграмма плавкости веществ с неограниченной растворимостью в жидком и твердом состояниях
Весьма часто твердая фаза, выделяющаяся при охлаждении расплавов, состоит из кристаллов, образованных обоими компонентами. Такая однородная система имеет переменный состав и называется твердым раствором. Твердые растворы – системы однофазные, подобно обычным жидким растворам, но в отличие от последних имеют кристаллическую структуру.
а) б)
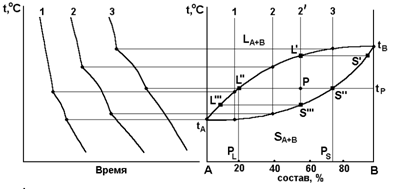
Рис. 8.2. Диаграмма плавкости для веществ, неограниченно растворимых в твердом и жидком состояниях
а) кривые охлаждения, б) диаграмма плавкости.
Неограниченной взаимной растворимостью в твердом состоянии обладают вещества, имеющие близкие значения атомных или ионных радиусов, энергии химической связи, сходное строение электронных оболочек и одинаковый тип кристаллической решетки (изоморфные вещества). Примерами таких систем могут служить Au-Ag, Cu-Au, Se-Ge, NaCl-NaBr и др.
Представленная на рис.8.2б диаграмма состоит из двух непрерывных сопряженных кривых: верхней tAL’tB (кривой ликвидуса) и нижней tAStB (кривой солидуса). Выше линии ликвидуса находится однофазная область – расплав компонентов А и В: при любых температурах и концентрациях система будет находиться в жидком состоянии (С =2 + 1 – 1 = 2). Ниже кривой солидуса система существует только в виде одной твердой фазы, представляющую собой непрерывный ряд твердых растворов (С =2 + 1 – 1 = 2).
Точки tA и tB – температуры плавления компонентов А и В. Между кривыми ликвидуса и солидуса находится двухфазная область, в которой сосуществуют жидкие и твердые растворы (С = 2 + 1 – 2 = 1). Кристаллизация всех промежуточных составов проходит в интервале температур. На кривых охлаждения отмечаются два излома, отвечающих началу и концу кристаллизации (рис. 8.2а).
Рассмотрим особенности кристаллизации систем этого типа (рис. 8.2б). Расплав состава, отвечающий фигуративной точке 2’, охлаждаем до точки L’. Начинают выпадать кристаллы S’. При охлаждении до точки Р выпадают кристаллы S’’, состав расплава отвечает точке L’’. По мере охлаждения состав кристаллов изменяется по кривой S’ – S’’ – S’’’, состав расплава по кривой L’ – L’’ – L’’’. Если отделить выкристаллизовавшиеся первые порции, обогащенные тугоплавким компонентом В, то неоднократным повторением процесса можно разделить А и В.
Составы жидкой и твердой фаз, сосуществующих при данной температуре, определяют точками пересечения изотермы соответственно с линиями ликвидуса и солидуса и отнесением их на ось составов. Так, для системы Р (рис.8.2б) при температуре tP состав жидкой фазы PL – 80% A и 20% B, твердой – PS – 28% A и 72% B. Количественное соотношение жидкой и твердой фаз в точке Р определяют отношением отрезков PS’’ : PL’’ = mж : mтв.
Аналогичный вид имеет диаграмма состав – температура для двух жидкостей, неограниченно смешивающихся в жидком и газообразном состоянии.
На рис. 8.3 представлены двухкомпонентные системы с образованием непрерывного ряда твердых растворов с максимумом и минимумом на диаграмме состояния.
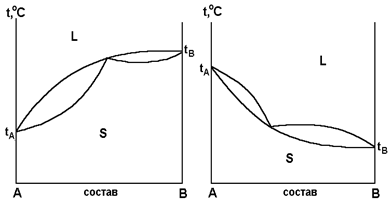
Рис. 8.3. Основные типы диаграмм для систем с непрерывным рядом твердых растворов
На кривых охлаждения составы, отвечающие экстремальным точкам, имеют нонвариантную остановку – площадку (С = 0), хотя равновесие двух фаз должно быть моновариантным (С = 2 + 1 – 2 = 1). В данном случае необходимо учесть, что составы жидкой и твердой фаз совпадают. Это приводит к тому, что в точках максимума и минимума система ведет себя как однокомпонентная и поэтому кристаллизуется при постоянной температуре (С = 1+ 1 – 2 = 0).
