Занятие 1. Семинар «Молекулярная природа генетического материала»
Часа
Цель:изучить химическую природу, особенности строения и свойства нуклеиновых кислот, выяснить зависимость их функций от строения, рассмотреть классификацию нуклеиновых кислот.
Основная литература:
1. Филлипович С.Б., Ковалевская Н.И., Севастьянова Г.А. Биологическая химия: учебное пособие для вузов. М.: Академия, 2005. – 254 с.
2. Проскурина И.К. Биохимия: Учебное пособие для вузов. – М.: ВЛАДОС-Пресс, 2003. – 235с.
3. Филлипович С.Ю., Коничев А.С., Севастьянова Г.А., Кутузова Н.М. Биохимические основы жизнедеятельности человека: учебное пособие для вузов. – М.: ВЛАДОС, 2005 г. – 404с.
4. Опарина С.А. Биохимия и основы биорегуляции организмов: Учебно-методическое пособие. - Арзамас: АГПИ, 2009. – 144 с.
Дополнительная литература:
1. Основы биохимии: Учебник для студ. биол. спец. универ. /А.А. Анисимов, А.Н.Леонтьева, И.Ф. Александрова и др. – М.: Высшая школа, 1986. – С.178-204.
2. Грин Н. Биология в 3-х томах / Н. Грин, У. Стаут, Д. Тейлор. – М.: Мир, 1993.- С.182-188.
3. Ленинджер А. Л. Основы биохимии в 3-х томах. – М.: Мир, 1985.- Т3. - С.852-891.
4. Марри Р. Биохимия человека в 2-х томах. Мари Р., Греннер Д. и др. – М.: Мир, 1993. - Т2 – С.5-12, С.53-58.
5. Березов Т.Т. Биологическая химия / Т.Т. Березов, Б.Ф Коровкин. – М.: Москва, "Медицина", 2007 г.- С.140-148.
Методические рекомендации к занятию
При подготовке к занятию студенты должны
знать:
- особенности строения и свойств нуклеиновых кислот;
- классификацию и биологическую роль нуклеиновых кислот;
- зависимость между строением, свойствами и функциями нуклеиновых кислот.
уметь:
- записывать формулы азотистых оснований, нуклеозидов, нуклеотидов; формулы отдельных фрагментов цепочек ДНК и РНК;
-давать сравнительную характеристику ДНК и РНК;
-вычислять содержание (в %) азотистых оснований и длину (в нм) молекул нуклеиновых кислот.
Терминологический словарь к семинару
Азотистые основания пуриновые (гуанин, аденин), пиримидиновые (урацил, цитозин, тимин), пентозы, нуклеозиды, нуклеотиды, гликозидная связь, фософдиэфирная связь, ДНК, РНК (рРНК,тРНК,мРНК, мяРНК), А,В формы спиралей, нуклеопротеины, хромосомы, рибосомы, АТФ, цАМФ.
План занятия
I.СЕМИНАР-КОЛЛОКВИУМ
Общие и частные вопросы из [4], с.76-78.
II.РЕШЕНИЕ ЗАДАЧ
Решение задач № 1,3, 5, упр.1,3,6,8, 11 с.78-79.
III. КОНТРОЛЬНАЯ РАБОТА
Вопросы и задания для самоконтроля
На каждую незаконченную фразу выберите одно верное завершение.
1. При полном кислотном гидролизе нуклеиновых кислот возникают все перечисленные вещества, кроме:
а) фосфорной кислоты; б) пентозы; в) пуриновых оснований; г) аденозинтрифосфорной кислоты; д) аденина.
2. В составе РНК содержится:
а) рамноза; б) фруктофураноза; в) р, D-рибофураноза; г) β, D-галактоза; д) β- D-2-дезоксирибофураноза.
3. В составе продуктов кислотного гидролиза РНК обнаруживают: а) только аденин; б) только гуанин; в) только цитозин; г) только урацил; д) все указанные гетероциклические основания.
4. В состав ДНК некоторых фагов входит:
а) рамноза; б) ксилулоза; в) фруктоза; г) сорбоза; д) глюкоза.
5. Только в состав РНК входит основание:
а) тимин; б) цитозин; в) урацил; г) гуанин; д) аденин.
6. Нуклеиновые кислоты имеют абсорбционный максимум в области 240-270 нм. Абсорбция их в этой области обусловлена наличием в составе нуклеиновых кислот: а) водородной связи; б) рибозы; в) гетероциклических оснований; г) фосфодиэфирной связи; д) фосфорной кислоты.
7. Соединения, характеризующиеся структурами:
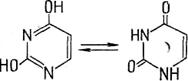
являются:
а) оптическими изомерами; б) цис-, транс-изомерами;в) геометрическими изомерами; г) таутомерными формами; д) конформационными изомерами.
8. В результате мягкого кислотного гидролиза РНК образуются:
а) только D-дезоксирибоза, цитозин и аденин; б) только D-рибоза, тимин и гуанин; в) D-рибоза, цитозин, урацил и тимин; г) D-рибоза, урацил, аденин, гуанин, цитозин; д) D-дезоксирибоза, цитозин, тимин, аценин, гуанин.
9. При действии азотистой кислоты в результате окислительного дезаминирования из аденина образуется:
а) гуанин; б) гипоксантин; в) ксантин; г) мочевая кислота; д) аллантоин.
10. С цитозином не сочетается водородными связями: а) ксантин; б) гуанин; в) гипоксантин; г) 5-оксиметилцитозин; д) 2-аминопурин.
11. На один виток двойной спирали ДНК, находящейся в В-форме, приходится следующее число пар оснований: а) 5; б) 10; в) 15; г) 20; д) 100.
12. Конечным продуктом катаболизма пуринов у человека является:
а) аллантоин; б) мочевина; в) аммиак; г) мочевая кислота; д) гипоксантин.
13. Мочевая кислота образуется из дезаминированных пуриновых оснований при участии фермента: а) аденинаминогидролазы; б) уреазы; в) урикооксидазы; г) аллантоиказы; д) ксантиноксидазы.
14. У большинства млекопитающих, исключая человека и человекообразных обезьян, мочевая кислота: а) восстанавливается до аммиака; б) окисляется до аллантоина; в) распадается до аммиака и углекислого газа; г) распадается на мочевину и глиоксиловую кислоту; д) превращается в аллантоиновую кислоту.
15. 5-фосфорибозил-1-пирофосфат необходим для биосинтеза: а) пуриновых и пиримидиновых нуклеотидов; б) только пиримидиновых нуклеотидов; в) только пуриновых нуклеотидов; г) дезоксирибозы из рибозы; д) АТФ из АДФ.
16. Адениловая кислота синтезируется в результате реакции:
а) инозин-5'-фосфат + NH3;
б) инозин-5'-фосфат + НАД+ + глутамин;
в) инозин-5'-фосфат + ГТФ + аспарагиновая кислота;
г) гипоксантин + рибозо-1-фосфат;
д) гипоксантин + 5-фосфорибозил-1-пирофосфат.
17. Фосфорибозилтрансфераза ускоряет реакцию:
а) гуанин + 5-фосфорибозил-1-пирофосфат → гуанозин-5'-монофосфат;
б) урацил + АТФ → уридин-5'-монофосфат;
в) аденин- рибозо-1 -фосфат → аденозин;
г) ГМФ + АТФ → ГДФ + АДФ;
д) урацил + рибозо-5-фосфат → УМФ.
18. Источниками атомов азота пуринового кольца являются: а) аспарагиновая кислота, глутамин и глицин; б) глутамин и аммиак; в)
19. Инозиновая кислота является предшественником:
а) урацила и тимина; б) уридиловой и цитидиловой кислот; в) пуриновых и пиримидиновых оснований; г) оротовой кислоты; д) адениловой и гуаниловой кислот.
20. В процессе биосинтеза пуриновых оснований атомы в положениях:
а) 3 и 9 - происходят из глутамина; б) 1 и 6 - происходят из глицина; в) 7,8 и 9 - происходят из мочевины; г) 3 и 9 - происходят из аспарагина; д) 3,4 и 5 - происходят из глицина.
21. В процессе биосинтеза пиримидиновых оснований:
а) атомы 1, 2 и 3 происходят из мочевины; б) атомы 3, 4 и 5 происходят из глутамина; в) атом 6 происходит из СО2; г) атомы 2 и 3 происходят из карбамилфосфата; д) атомы 3, 4 и 5 происходят из глицина.
22. Нуклеиновые кислоты — линейные полимеры, в которых нуклеотидные остатки соединены при помощи: а) водородных связей; б) ионных связей; в) 3',5'-фосфодиэфирных связей; г) координационных связей; д) иных связей.
23. В молекуле ДНК число остатков аденина всегда равно числу остатков:
1. а) тимина; б) гуанина; в) цитозина; г) ксантина; д) урацила.
24. Полидезоксирибонуклеотидные цепи в биспиральной молекуле ДНК, кроме водородных связей, удерживаются: а) электростатическими взаимодействиями; б) ковалентными связями; в) гидрофобными взаимодействиями; г) координационными связями; д) всеми указанными выше.
25. Водородные связи не возникают между: а) А-Т; б) А-У; в) Г-Ц; г) Г- 5МЦ; д) Г-А.
Сопоставьте два утверждения или показателя (обозначены буквами А и Б), приведенные в каждом пункте раздела, и дайте ответ в форме: А > Б; Б > А; А = Б.
1. А. Содержание ДНК в ядре. Б, Содержание ДНК в других субклеточных структурах.
2. А. Соотношение РНК/ДНК в клетке при высоком уровне биосинтеза белка в ней. Б. Соотношение РНК/ДНК в клетке при низком уровне белкового синтеза в ней.
3. А. Относительная молекулярная масса тРНК. Б. Относительная молекулярная масса рРНК.
4. А. Коэффициент поликонденсации нуклеотидных остатков в молекуле рРНК. Б. Коэффициент поликонденсации нуклеотидных остатков в молекуле тРНК.
5. А. Содержание тимина в ДНК. Б. Содержание тимина в тРНК.
6. А. Седержание РНК в рибосомах. Б. Содержание РНК в растворимой части цитоплазмы.
7. А. Количество видов рРНК. Б. Количество видов тРНК.
8. А. Содержание тРНК в клетке. Б. Содержание рРНК в клетке.
9. А. Число ГЦ-пар в тРНКала. Б. Число ГЦ-пар в 50S рРНК.
10. А. Температура плавления ДНК с содержанием ГЦ-пар, равным 50%. Б. Температура плавления ДНК с содержанием ГЦ-пар, равным 58%.
11. А. Содержание в клетке мРНК. Б. Содержание в клетке тРНК.
12. А. Число нуклеотидных звеньев в РНК с относительной молекулярной массой 5 • 105. Б. Число нуклеотидных звеньев в ДНК с относительной молекулярной массой 5 • 105.
13. А. Коэффициент специфичности ДНК, новообразованной in vitro при участии ДНК-полимеразы. Б. Коэффициент специфичности ДНК-затравки.
14. А. Доля метилированных нуклеотидов в составе рРНК. Б. Доля метилированных нуклеотидов в составе тРНК.
15. А. Разнообразие минорных оснований в тРНК. Б. Разнообразие минорных оснований в рРНК.
Выберите из нижеследующих утверждений правильные.
1. а) Нуклеотиды являются мономерными единицами нуклеиновых кислот; б) в составе ДНК бактериофагов обнаружен 5-оксиметилцитозин, иногда связанный гликозидной связью с остатками глюкозы; в) метилированные пуриновые и пиримидиновые основания обнаружены только в составе РНК; г) в составе тРНК содержится нуклеозид урацила - псевдоуридин, имеющий С-гликозидную связь.
2. а) РНК и ДНК содержат в своем составе одинаковые пуриновые основания; б) РНКи ДНК содержат в своем составе одинаковые пиримидиновые основания; в) только в РНК обнаружен 5-метилцитозин; г) только в составе ДНК есть минорные пуриновые и пиримидиновые основания.
3. а) У всех организмов обнаружено только три вида рРНК; б) РНК представлена одноцепочечным полирибонуклеотидом, биспирализованным на некотором протяжении; в) в последовательности нуклеотидных остатков рРНК заключена информация о биосинтезе специфического белка; г) рРНК являются структурной основой для формирования рибонуклеопротеидного тяжа, дающего начало 30-40 S и 50-60 S субчастицам рибосомы.
4. а) Содержание ДНК в клетках зависит от степени их плоидности; б) содержание пуринов в составе ДНК равно таковому пиримидинов; в) последовательность нуклеотидов в одной цепи ДНК однозначно определяет таковую в другой цепи; г) температура плавления ДНК не зависит от содержания ГЦ-пар в ее составе
5. а) Для бактериальных мРНК характерно ДНК-подобие нуклеотидного состава; б) мРНК про- и эукариот являются долгоживущими молекулами; в) мРНК содержат в своем составе информативные и неинформативные участки; г) спирализация сама на себя не характерна для полинуклеотидной цепи мРНК.
6. Вторичная структура молекул ДНК в В-форме характеризуется следующими параметрами: а) один виток дезоксиполинуклеотидной биспирали содержит 10 пар нуклеотидных остатков; б) расстояние между остатками соседних дезоксирибонуклеотидов составляет 0,56 нм; в) шаг спирали равен 0,34 нм; г) внешний диаметр биспирального дезоксиполирибонуклеотида равен 1 нм.
7. Молекула тРНК: а) представлена небольшим полирибонуклеотидом с относительной молекулярной массой около 25 000; б) в 75% случаев открывается остатком 5-фосфогуаниловой кислоты; в) всегда завершается триплетом - фЦфЦфА; г) несмотря на присутствие минорных оснований, обладает высокой степенью внутрицепочечной комплементарности.
8. Оротовая кислота: а) реагирует с 5-фосфорибозил-1-пирофосфатом с образованием оротидин-5'-фосфата; б) является промежуточным соединением при биосинтезе пиримидиновых нуклеотидов; в) является предшественником адениловой кислоты; г) посредством серии энзима-тических реакций может превращаться в ЦТФ и УТФ.
Выберите правильные парные сочетания ключевых слов или фрагментов фраз (обозначены буквами А, Б, В, Г, Д) и смысловых завершающих предложений (обозначены буквами а, б, в, г, д).
1. А. 6-Аминопурин. Б. 6-Оксипурин. В. 2,6,8-Триоксипурин. Г. 2,4-Диоксипиримидин. Д. 5-Метил-2,4-диоксипиримидин.
а) Тимин; б) урацил; в) гипоксантин; г) аденин; д) мочевая кислота.
2. А. Пуриновое основание. Б. Пиримидиновое основание. В. Нуклеозид. Г. Нуклеотид. Д. Рибонуклеиновая кислота.
а) Адениловая кислота; б) РНК; в) аденозин; г) аденин; д) урацил.
3. На рисунке изображены формулы:
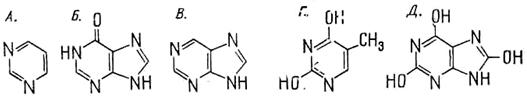
а) Гипоксантин; б) пурин; в) мочевая кислота; г) пиримидин; д) тимин.
4. На рисунке изображены формулы:
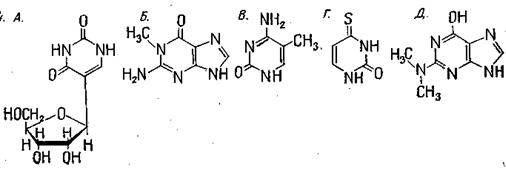
а) 1-Метилгуанин; б) 5-метилцитозин; в) псевдоуридин; г) 4-тиоурацил; д) диметилгуанин.
5. А. Глутамин. Б. β-Аланин. В. АТФ. Г. НАД'. Д. Карбамилфосфат.
а) Требуется для биосинтеза нуклеозидтрифосфатов; б) необходим для синтеза оротовой кислоты; в) продукт распада урацила и цитозина; г) необходим для превращения ксантозин-5-монофосфата в гуанозин-5-монофосфат; д) необходим для превращения инозиновой кислоты в ксантиловую кислоту.
6. А. Рибозилтрансфераза. Б. Нуклеозидаза. В. 3'-Нуклеотидаза.
Г. Нуклеотидаминогидролаза. Д. Нуклеозидаминогидролаза.
а) Ускоряет реакцию: уридин-3'-монофосфат + Н2О → уридин + Н3РО4;
б) катализирует процесс: аденозин + Н3РО4 → аденин + рибозо-1-фосфат;
в) обеспечивает ускорение реакции: цитидин + Н2О → цитозин + рибоза;
г) каталитически ускоряет реакцию: гуанозин + Н2О → ксантозин + NH3;
д) катализирует реакцию:
аденозин -5'-монофосфат + Н2О → инозин -5'-монофосфат + NН3.
7. А. Фосфорилирование. Б. Метилирование. В. Восстановление.
Г. Аминирование. Д. Дезаминирование.
2. а) Осуществляется при превращении: УМФ → ЦМФ;
3. б) происходит в реакции: дТМФ → дТДФ;
4. в) имеет место в реакции: дУМФ →дТМФ;
5. г) характерно для процесса: ЦДФ→ дЦДФ;
6. д) имеет место при преобразовании: 5-метил-дЦДФ → дТДФ.
Решите расчетные задачи и выполните упражнения.
1. Рассчитайте относительную молекулярную массу ДНК фагов, если длина неразветвленной двойной спирали: а) ДНК фага ФХ174 (ее двухцепочечной репликативной формы) равна 2,0 мкм; б) ДНК фага Я - 17,5 мкм; в) ДНК фага Т2 - 63 мкм.
2. Рассчитайте число нуклеотидных пар в отрезке двойной спирали ДНК длиной 1 мкм, находящейся: а) в А-форме и б) в В-форме.
3. В-форма кристаллической ДНК устойчива в условиях 97%-ной относительной влажности. Если влажность понизить до 76%, то происходит резкий переход В-формы ДНК в А-форму. Вычислите, на какую величину (мкм) изменится длина фрагмента ДНК, относительная молекулярная масса которого равна 1 000 000, если из В-формы он перейдет в А-форму.
4. Рассчитайте среднюю длину (мм) двухцепочечных молекул ДНК, находящихся в одной клетке у различных представителей животного мира, если известно количество нуклеотидных пар (в млн.) в составе клеточной ДНК: а) млекопитающие - 5500; б) амфибии - 6500; в) рыбы - 2000; г) птицы - 2000; д) ракообразные - 2800; е) грибы - 20; ж) бактерии - 2.
5. Клетка печени крысы содержит 9,1 • 10 -12 г ДНК. Допуская, что вся ДНК равномерно распределена между 42 хромосомами и существует в каждой хромосоме в виде единой молекулы, рассчитайте длину двухцепочечной ДНК (см), находящейся в одной хромосоме, принимая значение постоянной Авогадро равным 6 • 1023 моль-1.
6. Относительная молекулярная масса фрагмента ДНК равна 500 000. Рассчитайте объем фрагмента молекулы ДНК (нм3) при условии, что она имеет форму цилиндра.
7. В составе рибосомы кишечной палочки содержится по одной молекуле 23S, 16S и 5S РНК. Рассчитайте процентное соотношение трех видов РНК в рибосоме кишечной палочки.
8. Фрагменты одной цепи ДНК имеют следующие последовательности нуклеотидов: а) ЦААТГГГЦТАТ; б) АЦТАГТГЦЦА; в) ГЦТ5МЦАГГАТ. Какую нуклеотидную последовательность имеют комплементарные фрагменты второй цепочки той же молекулы?
9. Определите нуклеотидную последовательность участков молекулы РНК, синтезированной с помощью РНК-полимеразы, если затравка имела следующие нуклеотидные фрагменты: а) АТЦГААЦТАЦГ; б) ЦТТАГЦТАЦЦ; в) ТГАЦАГТААГЦГ.
10. В мРНК содержание аденина, цитозина, гуанина и урацила составляет 22, 27, 23 и 28% соответственно. Рассчитайте нуклеотидный состав участка двухцепочечной ДНК, на котором был осуществлен синтез указанной мРНК.
11. Валиновая тРНК из дрожжей, первичная структура которой расшифрована А. А. Баевым и его сотрудниками, содержит 77 нуклеотидных остатков в молекуле. Акцепторный конец этой тРНК биспирализован в наибольшей степени - 7 пар нуклеотидов. В антикодоновой петле в спирализованной области находятся 5 пар нуклеотидов, сочетающихся водородными связями. В «дигидроуридиновой» петле биспирализованная часть включает 3 пары нуклеотидных остатков. Рассчитайте в процентах долю нуклеотидных остатков, находящихся в биспирализованных областях молекулы и поддерживающих вторичную структуру дрожжевой валиновой тРНК.
12. Последовательность нуклеотидов в цепи м - РНК ... У У Ц А А Г У Г Ц А А Ц Т Ц А ... Пользуясь триплетным кодом, составьте тетрапептид, закодированный в этой последовательности нуклеотидов, дайте ему правильное название.
13. Укажите соответствие между следующими соединениями:
1. Аденозин А. Рибонуклеотид.
2. АМФ. Б. Дезоксирибонуклеотид.
3. ТМФ. В. Нуклеозид
4. УМФ. Г. Рибонуклеозидтрифосфат
5. ЦМФ.
6. АТФ
14. Зная первичную структуру молекулы белка, установите нуклеотидную последовательность в гене инсулина?
Рекомендуемая литература
1. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. – М.: Медицина, 2007.
2. Браунштейн Л.Е. На стыке химии и биологии. – М.: Наука, 1987.
3. Грин Н.Биология в 3-х т./Н. Грин, Стаут У., Тейлер Д. – М.: Мир, 1990.
4. Досон Р.Справочник биохимика. – М.: Мир, 1991.
5. Кюре Д.Г. Биохимия: Учебник для хим., биолог., медиц. спец. вузов
/ Д.Г.Кюре, Мызина С.Д. – М.: Высш. школа, 1998.
6. Ленинджер А. Основы биохимии, в 3-х томах. – М., 1985.
7. Марри Р. Биохимия человека в 2-х томах – М.: Мир, 1993.
8. Мусил Я. Современная биохимия в схемах / Я.Мусил, О. Новакова, К. Кунц – М.: Мир, 1981.
9. Основы биохимии: Учебник для студ. биол. спец. универ. /А.А. Анисимов, А.Н.Леонтьева, И.Ф. Александрова и др. – М.: Высшая школа, 1986.
10. Проскурина И.К. Биохимия: Учебное пособие для вузов. – М.: ВЛАДОС-Пресс, 2003.
11. Рис Э. От клеток к атомам / Э. Рис, М. Стенберг – М.: Мир, 1988.
12. Сидорская Э.А., Афиногенова С.Г. Витамины. – Арзамас: АГПИ, 1990.
13. Страйер Л. Биохимия, в 3-х томах – М.: Мир, 1985.
14. Тюкавина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991.
15. Филлипович Ю.Б. Упражнения и задачи по биологической химии/ Ю.Б. Филлипович, Г.А. Севастьянова, Л.И. Щеголева – М., 1986.
16. Филлипович С.Ю., Коничев А.С., Севастьянова Г.А. Биохимические основы жизнедеятельности человека: учебное пособие для вузов. – М.: ВЛАДОС, 2005.
17. Филлипович С.Ю., Ковалевская Н.И., Севастьянова Г.А. Биологическая химия: учебное пособие для вузов. – М.: Академия, 2005.
Примерная тематика курсовых работ
1. Биологически активные пептиды и их будущее.
2. Обратная транскрипция и ее значение для общей генетики и онкологии.
3. Множественные формы ферментов и вопросы эволюции и систематики растений.
4. Внеядерная наследственность.
5. «Прыгающие» гены.
6. Организация и функция генома эукариот.
7. Строение и биологические функции сложных углеводов (гликолипидов, гликопротеидов).
8. Углеводы и углеводный обмен в животных и растительных организмах.
9. Посттрансляционная модификация белков.
10. Нейропептиды и синтез их методом генной инженерии.
11. ДНК сегодня.
12. Митохондрии - энергетические станции клеток.
13. Иммобилизированные ферменты. Перспективы их применения в медицине.
14. Поливитаминные металлы в биологических объектах.
15. Полиморфизм белков. Значение его в эволюции и онтогенезе.
16. Физиологически активные полимеры.
17. Продукты питания и процессы старения.
18. Химия пищевых белков. Белковое питание в профилактике и лечении ряда заболеваний.
19. Биологическая роль и пищевые источники моносахаридов, олигосахаридов, полисахаридов.
20. Биологически активные соединения и продукты питания.
21. Химия жира и жировых продуктов питания. Липиды в профилактике и лечении ряда заболеваний.
22. Молекулы милосердия (обезболивающие вещества).
23. Половые гормоны и противозачаточные средства.
24. Простагландины.
25. Физиологическая и патологическая роль некоторых элементов в организме.
26. Кислотно-основное равновесие и буферные растворы системы организма.
27. АТФ - аккумулятор, трансформатор и проводник энергии в процессе ее запасания и расходования в организме.
28. Биохимия возникновения жизни на Земле.
29. Демонстрационный эксперимент по биохимии.
30. Тонкослойная хроматография в биохимических исследованиях.
31. Сравнительная характеристика количественных методов определения витамина С.
32. Разделение липидов в тонком слое (метод ТСХ).
Приложение
ТАБЛИЦА ГЕНЕТИЧЕСКОГО КОДА
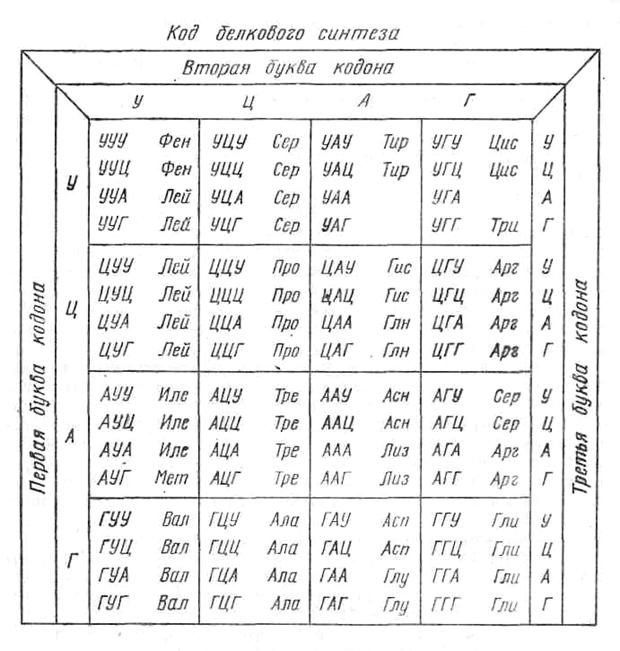
Учебное издание
Опарина Светлана Александровна
Методические рекомендации к к лабораторно-практическим
И семинарским занятиям
по дисциплине «Биохимия и основы биорегуляции организмов (ч.1.)»
В авторской редакции
Технический редактор С.П. Никонов
Вёрстка и вывод оригинала макета Опарина С.А.
Лицензия ИД №04436 от 03.04.2001. Подписано в печать:
Формат 60х84/16. Усл.печ.листов: 2,4. Тираж:100 экз. Заказ №
Издатель:
Арзамасский государственный педагогический институт
им. А.П. Гайдара
607220, г. Арзамас, Нижегородская обл., ул. К.Маркса, 36
Участок оперативной печати АГПИ
607220, г. Арзамас, Нижегородская обл., ул. К.Маркса, 36
