Атомные и молекулярные массы
Атомы и молекулы имеют абсолютные массы порядка 10–24–10–21 г, неудобные для сравнения, поэтому химики пользуются относительными значениями масс атомов. Представление об относительной атомной массе было введено Дж. Дальтоном в 1803 г. За единицу массы он принял массу самого легкого атома – водорода. В настоящее время в качестве эталона принята масса 1/12 массы атома углерода изотопа 12С, равная 1,66043×10–24 г.
Относительная атомная (Аr) масса показывает во сколько раз данный атом тяжелее 1/12 массы атома изотопа углерода 12С.
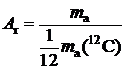 , , | (1.2) |
где mа – масса атома, mа(С) – масса атома изотопа углерода 12С.
Для определения атомной массы элементов в 19 веке использовался метод, основанный на законе теплоемкости П.Л. Дюлонга и А.Т. Пти (1819 г.): молярная теплоемкость (СМ) для различных простых веществ в кристаллическом состоянии одинакова и равна приблизительно 26,4 Дж. Она равна произведению удельной теплоемкости (Суд) на молярную массу элемента:
| Смолярная=Суд×М =26,4 Дж | (1.3) |
Используя величину удельной теплоемкости, которая легко определяется экспериментально (отношение количества теплоты полученного или отданного 1 г вещества к соответствующему изменению температуры) можно найти приближенное значение атомной массы. Исключения составляют легкие элементы, особенно неметаллы, имеющие теплоемкость значительно меньше (бериллий, бор, кремний, алмаз).
В настоящее время атомные массы элементов определяют методом масс-спектроскопии. Массы атомов определяют по отклонению траектории их ионов, двигающихся в магнитном поле, поскольку величина отклонение зависит от отношения массы иона к его заряду.
Относительная молекулярная масса (Mr)показывает во сколько раз данная молекула тяжелее 1/12 массы атома 12С.
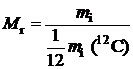 , , | (1.4) |
где mм – масса молекулы.
Количество вещества
Другой характеристикой вещества является количество вещества – физическая величина, определяемая числом частиц. Единица количества вещества – моль содержит такое же число частиц, как и 12 граммов углерода 12С. Это число частиц, равное 6,02×1023, называется Авогадровым числом (NA).
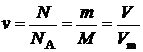 , , | (1.5) |
где n – количество вещества,
М – молярная масса (масса одного моля),
Vm – молярный объем.
Для железа M = 56 г/моль, для воды M = 18 г/моль.
Молярные объемы твердых и жидких веществ зависят от их плотности:
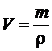 .
.
Vm(H2O) = 18 мл/моль, т.к. плотность воды (r) равна 1 г/мл.
Закон Авогадро
У газообразных веществ при атмосферном давлении собственные размеры молекул незначительны по сравнению с расстояниями между ними. Молярные объемы газов при одинаковых условиях постоянны, и при нормальных условиях близки к 22,4 л/моль. Это следствие из закона Авогадро(1811 г.): в равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул.
Относительная плотность газов
Из закона Авогадро следует, что плотности различных газов будут относиться друг к другу, как молярные массы. Для определения молярных масс газов используется значение относительной плотности газов – отношение массы определенного объема одного газа к массе такого же объема другого газа (при тех же условиях):
Измерив относительную плотность одного газа по другому, можно определить его молекулярную массу, что используется в аналитической химии для идентификации газообразных веществ.
