ОКИСЛИТЕЛЬНО – ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
221. Определите, к какому виду окислительно-восстановительных процессов относятся следующие реакции:
а) KMnO4 + KNO2 + H2SO4 → K2SO4 + MnSO4 + KNO3 + H2O;
б) H2S + SO2 ® S + H2O;
в) Zn + HNO3 (разб.) ® Zn (NO3)2 + N2O + H2O.
С помощью метода электронного баланса расставьте коэффициенты в этих уравнениях.
222.Составьтеэлектронные уравнения и расставьте коэффициенты в уравнениях реакций. Укажите, какое вещество является окислителем, какое – восстановителем.
а) P + HNO3(конц.) ® H3PO4 + NO2+ H2O;
б) S + HNO3 ® H2SO4 + NO;
в) Cu + H2SO4 (конц.) ® Cu SO4 + SO2 + H2O.
223.Определите степени окисления всех компонентов, входящих в состав следующих соединений: HСl, Cl2, HClO2 , HClO3 , Cl2O7 . Какие из веществ являются только окислителями, только восстановителями, и окислителями и восстановителями? Расставьте коэффициенты в уравнении реакции:
КСlO3 → КС1 + КСlO4.
Укажите окислитель и восстановитель.
224.Используя метод электронного баланса, подберитекоэффициенты в уравнениях реакций:
a) Na2SO3 → Na2S + Na2SO4;
б) MnO2 + HCl ® MnCl2 + Cl2 + H2O;
в) H2S + H2SO3 ® S + H2O.
225. Укажите реакции, в которых азот окисляется, восстанавливается, не изменяет степени окисления.
а) P + HNO3 + H2O = H3PO4 + NO;
б) С + HNO3 ® CO2 + NO + H2O;
в) NH4NO3 + KOH ® NH4OH + KNO3.
Составьте уравнения электронного баланса, расставьте коэффициенты.
226. Какие из приведенных реакций являются внутримолекулярными?
Расставьте коэффициенты в уравнениях реакций. Укажите восстановитель, окислитель.
а) KNO3 ® KNO2 + O2;
б) Mq+ N2 → Mq3N2;
в) KClO3 ® KCl + O2.
227.Какие ОВР относятся к реакциям диспропорционирования? Расставьте коэффициенты в реакциях:
а) Cl2 + KOH ® KCl + KClO3 + H2O;
б) KClO3 ®kat KCl + KClO4 .
228.Какие соединения и простые вещества могут проявлять только окислительные свойства? Выберите такие вещества из предложенного перечня: NH3, CO, SO2, K2MnO4, Сl2, HNO2. Составьте уравнение электронного баланса, расставьте коэффициенты в уравнении реакции:
HNO3 + H2S ® H2SO4 + NO + H2O.
229.Расставьте коэффициенты в уравнениях реакций. Укажите окислитель, восстановитель.
а) HClO3+ H2SO3 ® HCl + H2SO4;
б) KClO3 ®kat KCl + KClO4
в) MnCO3 + KClO3 ® MnO2 + KCl + CO2.
230.Определите, к какому виду ОВР относятся следующие реакции:
а) H2O + H2SO3 + I2 ® HI + H2SO4;
б) Fe2O3 + CO = Fe + CO2;
в) H2S + SO2 = S + H2O.
С помощью метода электронного баланса расставьте коэффициенты в этих уравнениях.
231.Определите, к какому типу ОВР относятся процессы, протекающие по схемам:
а) K2Cr2O7 + H2SO4 + H2S → Cr2(SO4)3 + H2O + S + K2SO4;
б) КМnО4 + Н3РО3 + H2SO4 → MnSO4 + Н3РО4 + K2SO4 + Н2О;
в) SO2 + Br2 + H2O = H2SO4 + HBr.
Расставьте коэффициенты в уравнениях реакций. Укажите окислитель, восстановитель.
232.Составьте электронные уравнения, укажите, какой процесс – окисление или восстановление – происходит при следующих превращениях:
a) S-2 ® S+6; б) Cu0 ® Cu+2; в) N+3 ® N+5.
Используя метод электронно-ионного баланса, расставьте коэффициенты в уравнении реакции, идущей по схеме:
NaI + KMnO4 + KOH ® I2 + K2MnO4 + NaOH.
Укажите окислитель, восстановитель.
233. Исходя из степени окисления хрома, укажите, какие из соединений проявляют только окислительные свойства: Cr, CrO, СrO3, K2Cr2O7 . Почему? Расставьте коэффициенты в уравнении реакции, идущей по схеме:
K2Cr2O7 + H2SO4 + 3H2S = Cr2(SO4) + H2O + S + K2SO4.
Укажите окислитель и восстановитель.
234.Составьте электронные уравнения для реакций, протекающих по схемам:
а) KMnO4 + H2О + Na2SO3 = MnО2 + Na2SO4 + КОН;
б) SO2 + H2S = S + H2O;
в) Са + H2O ® Са(OH)2+H2.
К какому виду ОВР относятся эти реакции? Расставьте коэффициенты, укажите окислитель и восстановитель.
235.Составьте электронные уравнения и укажите, какой процесс – окисление или восстановление - происходит при следующих превращениях:
а) Cl+7 ® Cl-; б) Mn+4 ® Mn+2; в) Na0 ® Na+1.
На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме:
КМnО4 + Н3РО3 + H2SO4 → MnSO4 + Н3РО4 + K2SO4 + Н2О.
236.Какие соединения и простые вещества могут проявлять как окислительные, так и восстановительные свойства: O2 , H2S, Zn, F2, KNO2 ? Почему?
С помощью метода электронного баланса расставьте коэффициенты в уравнении реакции:
Сu + HNO3 (конц.) ® Cu(NO3)2 + NO2 + H2O.
237.Определите, к какому виду ОВР относятся следующие реакции:
а) Zn + H2SO4 → ZnSO4+ H2S + H2O;
б) H2S + Cl2 + H2O → H2SO4 + HCl ;
в) P + HIO3 + H2O → H3PO4 + HI
С помощью метода электронного баланса подберите коэффициенты в этих уравнениях.
238.Реакции выражаются схемами:
а) P + HNO3 + H2O → H3PO4 + NO;
б) KClO3 + Na2SO3 → KCl + Na2SO4;
в) FeS + HNO3 → Fe(NO3)2 + S + NO + H2O.
Составьте электронные уравнения. Расставьте коэффициенты. Укажите окислитель, восстановитель.
239.Определите степени окисления всех элементов, входящих в соединения: F2, Cu, HCl, H2S, KCl, KNO2. Какие из перечисленных веществ проявляют только восстановительные свойства? Расставьте коэффициенты в уравнении реакции, укажите окислитель, восстановитель:
KBr + KBrO3 + H2SO4 ® Br2 + K2SO4 + H2O.
240.Определите, к какому типу ОВР относятся процессы, протекающие по схемам:
а) FeSO4 + KClO3 + H2SO4 → Fe2(SO4)3 + KCl + H2O;
б) Au + HNO3 + HCl → AuCl3 + NO + H2O;
в) HCl + CrO3 → Cl2 + CrCl3 + H2O.
Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите окислитель, восстановитель.
ЭЛЕКТРОДНЫЕ ПРОЦЕССЫ И ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ
241.Вычислите значение э.д.с. гальванического элемента:
(-) Mg / 0,01 М MgSO4 // 0,01 М CuSO4 / Cu (+)
Напишите процессы на аноде и катоде, реакцию, генерирующую ток, и определите в кДж энергию химической реакции, превращающуюся в электрическую.
242.Вычислите значение э.д.с. гальванического элемента:
(-) Al / 0,001 М Al2(SO4)3 // 0,01 М NiSO4 / Ni (+)
Напишите процессы на аноде и катоде, реакцию, генерирующую ток, и определите в кДж энергию химической реакции, превращающуюся в электрическую.
243. Составьте схемы двух гальванических элементов, в одном из которых медь является катодом, а в другом – анодом. Напишите для каждого из этих элементов уравнение анодного и катодного процессов. Рассчитайте стандартную ЭДС этих элементов.
244. Рассчитайте ЭДС гальванического элемента, составленного из стандартного водородного электрода и свинцового электрода, погруженного в 0,01 М раствор PbCl2. На каком электроде идёт процесс окисления, а на каком - восстанавление?
245. По уравнению токообразующей реакции составьте схему гальванического элемента:
Ni + СuSO4 = NiSO4 + Cu
Напишите уравнения анодного и катодного процессов. Рассчитайте стандартную ЭДС.
246. Вычислите электродный потенциал свинца электрода в растворе его соли с концентрацией 0,001 моль/л. Составьте схему гальванического элемента, в котором свинец является анодом. Напишите уравнения реакций, протекающих на катоде и аноде. Рассчитайте стандартную ЭДС этого элемента.
247. Составьте схему гальванического элемента, уравнения полуреакций анодного и катодного процессов, молекулярное уравнение реакции, проходящей при работе гальванического элемента, анодом которого является никель. Подберите материал для катода. Рассчитайте стандартную ЭДС этого гальванического элемента.
248. Составьте схему гальванического элемента из магния и свинца, погруженных в растворы их солей с концентрацией ионов:
[Mg2+] = 0,001 моль/л, [Pb2+] = 1 моль/л.
249. Составьте схему, напишите уравнения электродных процессов и вычислите ЭДС гальванического элемента, в котором один цинковый электрод погружен в 0,01 М раствор, а другой – в 1 М раствор.
250. Как изменится (увеличится, уменьшится) или останется постоянной масса пластины из кобальта, погруженной в раствор, содержащий соли Fe (II), Mg, Ag (I). Напишите молекулярные уравнения реакций.
251. Вычислите значение э.д.с. гальванического элемента:
(-) Zn / 0,001 М ZnSO4 // 0,001 М Bi2 (SO4)3 // Bi (+)
Напишите процессы на аноде и катоде, реакцию, генерирующую ток, и определите в кДж энергию химической реакции, превращающуюся в электрическую.
252. Вычислите электродный потенциал водородного электрода в водном растворе кислоты с рН=2.
253. На сколько изменится потенциал медного электрода, если раствор соли меди разбавить в 10 раз?
254. Рассчитать рН водородного электрода, погруженного в 0,1 М раствор соляной кислоты.
255. По уравнению токообразующей реакции:
Mg+ NiSO4 = MgSO4 + Ni
составьте схему гальванического элемента. Напишите уравнения катодного и анодного процессов. Рассчитайте стандартную ЭДС этого элемента.
256. Вычислить значение электродного потенциала процесса:
Co2+ →Co3+,
если концентрация [Co2+]= 0,01 моль/л, [Co3+]=10-2 моль/л.
257. Составьте схему гальванического элемента, составленного из магния и кобальта. Напишите уравнения электродных процессов. Вычислите ЭДС этого элемента, если:
[ Mg2+] = 1 моль/л, [ Co2+] = 0,1 моль/л.
258. Вычислить значение электродного потенциала процесса:
Co2+ →Co3+,
если концентрация [Co2+] = 0,01 моль/л, [Co3+]=10-2 моль/л.
259. Вычислите значение э.д.с. гальванического элемента
(-) Cr / 0,001 М Cr2(SO)3 // 0,1 М CuSO4 / Cu (+)
Напишите процессы на аноде и катоде, реакцию, генерирующую ток, и определите в кДж энергию химической реакции, превращающуюся в электрическую.
260. Как работает свинцовый (кислотный) аккумулятор? Составьте уравнения полуреакций и зарядки – разрядки аккумулятора.
ЭЛЕКТРОЛИЗ СОЛЕЙ
261. При электролизе соли трехвалентного металла ток силой в 3 А в течение 2 часов выделил на катоде 4,18 г металла. Определите, какой это металл. Напишите уравнения катодного и анодного процессов, а также суммарное уравнение электролиза расплава и водного раствора карбоната натрия с платиновым анодом.
262. На электролиз водного раствора нитрата серебра израсходовано 12500 Кл электричества. Вычислите массу выделяющихся на угольных электродах веществ. Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза.
263. При рафинировании меди током 4,5 А за 1,5 часа выделяется 7,5 г меди. Рассчитайте выход по току. Напишите уравнения катодного и анодного процессов, а также суммарное уравнение электролиза водного раствора Pb(NO3)2 : а) с угольным анодом; б) со свинцовым анодом.
264. Вычислите время, в течение которого должен быть пропущен ток в 1,5 А через раствор цинковой соли, чтобы покрыть пластину цинком массой 2 г. Выход по току 85%. Одинаковы ли продукты электролиза водного раствора BaCl2: а) с платиновым анодом; б) с цинковым анодом? Ответ подтвердите соответствующими уравнениями реакций.
265. Электрический ток силой 5 А пропускали в течение 1 ч 30 мин 15 секунд через водный раствор KI. Какие вещества и в каком количестве выделятся за это время на угольных электродах? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза.
266. Какие вещества и в каком количестве выделятся на угольных электродах при электролизе раствора NaCl течение 45 мин при силе тока 10 А? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза.
267. Как изменится за 1,5 часа масса цинкового анода при электролизе раствора Na3PO4 при силе тока 5 А? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза.
268. Ток силой 1 А в течение 80 мин выделил 2,5 г свинца из раствора Pb(NO3)2. Вычислите выход по току. Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза водного раствора и расплава.
269. Какие вещества и в каких количествах образуются при электролизе расплава 214 г NaCl? Сколько времени будет длиться электролиз, если сила тока равна 25 А? Одинаковы ли продукты электролиза водного раствора NaCl: а) с угольным анодом; б) с кадмиевым анодом? Ответ подтвердите соответствующими уравнениями реакций.
270. Найдите объем водорода, который выделится при пропускании тока силой в 5 А в течение 3,5 ч через водный раствор серной кислоты. Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза раствора Н2SО4 с инертным анодом.
271. Сколько времени потребуется на электролиз раствора KCl при силе тока 5 А, чтобы выделить хлор объемом 11,2 л (н.у.), если выход по току составляет 90%? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза.
272. При электролизе одного из соединений олова ток силой в 2,5А за 20 мин выделил на электродах металл массой 0,9 г. Чему равна валентность олова в этом соединении. Какие продукты могут быть получены при электролизе раствора SnSO4 с графитовыми электродами.
273. Сколько времени потребуется, чтобы нанести на пластинку слой цинка массой 5 г, если сила тока 8 А, выход по току 85%? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза раствора нитрата цинка с графитовыми электродами.
274. Какой силы ток следует пропустить через раствор поваренной соли в течение 1 час 40мин 10 сек, чтобы на катоде выделилось 10 л водорода? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза: а) если анод угольный, б) если анод кадмиевый.
275. Ток последовательно проходит через два электролизера, в которых содержатся водные растворы: а) CdSO4; б) MgCl2. Какие вещества и в каком количестве выделятся на катодах, если известно, что у анода второго электролизера выделилось 1,2л хлора? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза.
276. Вычислите силу тока, зная, что при электролизе раствора фторида натрия в течение 1 ч 15 мин 20 сек на катоде выделилось 0,56 л водорода. Какое вещество и в каком количестве выделится на аноде? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза.
277. При пропускании тока в течение 10 минут через раствор серной кислоты выделяется 0,06 л гремучего газа (1 часть кислорода и 2 части водорода), измеренного при н.у. Какова сила тока? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза раствора серной кислоты с медным анодом.
278. При какой силе тока можно получить на катоде 1,5г свинца, подвергая электролизу раствор нитрата свинца в течение 55 мин? Какова масса вещества, выделившегося на аноде? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза с инертным анодом.
279. Амперметр, включенный последовательно с электролизером с раствором сульфата цинка, показывает силу тока 1,5 А. Верен ли амперметр, если за 15 мин выделилось 455 мг цинка? Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза раствора и расплава сульфата цинка с инертным анодом.
280. Вычислите массы веществ, образующихся в прикатодном и прианодном пространстве, при электролизе раствора K2SO4 в течение 0,5 ч и силе тока 5 А. Напишите уравнения анодного и катодного процессов, а также суммарное уравнение электролиза.
КОРРОЗИЯ МЕТАЛЛОВ
281. В каком случае цинк корродирует быстрее: в контакте с никелем, железом или с висмутом? Ответ поясните. Напишите для всех случаев уравнение электрохимической коррозии в серной кислоте. Будет ли оксидная пленка, образующаяся на кальции, обладать защитными свойствами?
282. Приведите примеры двух металлов, пригодных для протекторной защиты железа. Для обоих случаев напишите уравнение электрохимической коррозии во влажной среде, насыщенной кислородом. Будет ли оксидная пленка, образующаяся на алюминии, обладать защитными свойствами?
283. Деталь сделана из сплава, в состав которого входит магний и марганец. Какой из компонентов сплава будет разрушаться при электрохимической коррозии? Ответ подтвердите уравнениями анодного и катодного процесса коррозии: а) в кислой среде; б) в кислой среде, насыщенной кислородом. Будет ли оксидная пленка, образующаяся на олове, обладать защитными свойствами?
284. С целью защиты от коррозии цинковое изделие покрыли оловом. Какое это покрытие: анодное или катодное? Напишите уравнение атмосферной коррозии данного изделия при нарушении целостности покрытия. Оценить коррозионную стойкость алюминия в серной кислоте, если убыль массы алюминиевой пластины размером 70х20х1 мм составила после 8 суток испытания 0,0348 г.
285. Если на стальной предмет нанести каплю воды, то коррозии подвергается средняя, а не внешняя часть смоченного металла. Чем это можно объяснить? Какой участок металла, находящийся под влиянием капли, является анодным, а какой катодным? Составьте электронные уравнения соответствующих процессов. Будет ли оксидная пленка, образующаяся на никеле, обладать защитными свойствами?
286. В подкисленный серной кислотой раствор бихромата калия поместили две железные пластины, одна из которых частично покрыта цинком, а другая - оловом. Напишите для обоих случаев уравнение анодного и катодного процессов. Будет ли оксидная пленка, образующаяся на вольфраме, обладать защитными свойствами?
287. Сплав содержит железо и никель. Какой из названных компонентов будет разрушаться при атмосферной коррозии? Приведите уравнение анодного и катодного процессов. Оценить коррозионную стойкость цинка на воздухе при высоких температурах. Образец цинка размером 50х30х1 мм после 180 часов окисления и снятия продуктов коррозии весил 10,6032 г.
288.С целью защиты от коррозии железное изделие покрыли оловом. Какое это покрытие: анодное или катодное? Напишите уравнения анодного и катодного процессов коррозии в кислой среде при нарушении целостности покрытия. Будет ли оксидная пленка, образующаяся на магнии, обладать защитными свойствами?
289. Почему химически чистое железо является более стойким против коррозии, чем техническое железо? Составьте уравнения анодного и катодного процессов, происходящих при коррозии технического железа во влажном воздухе и в азотной кислоте. Будет ли оксидная пленка, образующаяся на свинце, обладать защитными свойствами?
290. Приведите примеры двух металлов, пригодных для протекторной защиты никеля. Для обоих случаев напишите уравнение электрохимической коррозии в среде азотной кислоты. Оценить коррозионную стойкость кадмия на воздухе при высоких температурах. Образец кадмия размером 45х25х1 мм после 150 часов окисления и снятия продуктов коррозии весил 10,0031 г.
291. Деталь сделана из сплава, в состав которого входит алюминий и висмут. Какой из компонентов сплава будет разрушаться при электрохимической коррозии? Ответ подтвердите уравнениями анодного и катодного процесса коррозии: а) в кислой среде; б) в кислой среде хромата калия, подкисленного соляной кислотой. Будет ли оксидная пленка, образующаяся на барии, обладать защитными свойствами?
292. Если гвоздь вбить во влажное дерево, то ржавчиной покрывается та его часть, которая находится внутри дерева. Чем это можно объяснить? Анодом или катодом является эта часть гвоздя? Составьте электронные уравнения соответствующих процессов. Будет ли оксидная пленка, образующаяся на кобальте, обладать защитными свойствами?
293. Цинковую и оловянную пластинки опустили в раствор соляной кислоты. Что при этом происходит? Напишите уравнения реакций. Что изменится, если концы пластин соединить проводником? Напишите соответствующие уравнения. Оценить коррозионную стойкость титана в концентрированной серной кислоте. Титановая пластина размером 75х50х0,5 мм весила после 6 суток испытания 7,343 г.
294. Магний спаян с медью и находится во влажном воздухе. Напишите уравнения коррозии. Будет ли оксидная пленка, образующаяся на титане, обладать защитными свойствами?
295. Серебро не вытесняет водород из соляной кислоты, но если к нему прикоснуться цинковой палочкой, то на серебре начинает бурно выделяться водород. Почему? Напишите электронные уравнения. Будут ли оксидные пленки, образующиеся на железе, обладать защитными свойствами?
296. Какое покрытие: магниевое или кадмиевое надежней защитит железное изделие от коррозии? Почему? Напишите уравнения коррозии в кислой среде для обоих случаев. Будут ли оксидные пленки, образующиеся на хроме, обладать защитными свойствами?
297. Чем отличается коррозия сплава, состоящего из меди и олова, в бензине, содержащем растворенный кислород и примеси серы, от коррозии этого же сплава в воде, содержащей растворенный кислород и ионы водорода? Напишите уравнения реакций для обоих случаев. Будет ли оксидная пленка, образующаяся на серебре, обладать защитными свойствами?
298. Какой из перечисленных металлов: калий, свинец, алюминий или магний подойдет в качестве протектора для защиты кобальта? Напишите электронные уравнения процессов коррозии в кислой среде, содержащей растворенный кислород. Будет ли оксидная пленка, образующаяся на бериллии, обладать защитными свойствами?
299. Медь покрыта оловом. Напишите уравнения электродных процессов во влажном воздухе при нарушении покрытия. Будет ли оксидная пленка, образующаяся на цинке, обладать защитными свойствами?
300. Каковы продукты атмосферной коррозии оцинкованного железа и луженого железа? Напишите уравнения электродных процессов. Будут ли оксидные пленки, образующиеся на меде, обладать защитными свойствами?
Комплексные соединения
301. Из сочетаний частиц Hg2+, NH3, I- и K+ можно составить 5 координационных формул комплексных соединений ртути. Укажите формулы данных соединений, если координационное число ртути равно четырем. Назовите эти соединения и запишите уравнения их диссоциации на ионы.
302. Рассмотрите следующую реакцию:
2[Co(H2O)6)]Cl2 + 2NH4Cl + 10 NH3 + H2O2 ® 2[Co(NH3)6]Cl3 + 14 H2O,
катализатором которой является древесный уголь. Какую степень окисления имеет атом кобальта в комплексных соединениях [Co(H2O)6)]Cl2 и [Co(NH3)6]Cl3 ? Какую роль играет пероксид водорода и какую - аммиак?
303. Составьте уравнения диссоциации на ионы комплексных солей:
Cr(NH3)5Сl3; Cr(NH3)4(H2O)Cl3; Co(NH3)5(NO2)3; KСo(NH3)2(NO2)4,
заключив формулы комплексных ионов в квадратные скобки и имея в виду, что координационное число как хрома, так и кобальта равно шести.
304. Пользуясь таблицей констант нестойкости (см. табл.3 Приложений), определите, в каких случаях произойдет взаимодействие между растворами электролитов. Укажите для этих случаев молекулярные и ионные формы уравнений:
а) K2[HgBr4] +KCN;
б) Na3[Ag(S2O3)2] + KCN;
в) [Cu(NH3)4](NO3)2 +KCN;
305. Укажите возможные продукты следующих реакций, уравненных в левой части приведенных схем:
а) [Ni(H2O)6]2+ + 2C2O42- 
б) Zn(CN)2 + 2KCN 
в) [Fe(H2O)6] 2+ + 2NH3 
г) [Fe(H2O)5(OH)] 2+ + НNO3 
306. Приведите схемы диссоциации и выражения констант нестойкости следующих комплексных ионов:
а) [Fe(CN)6]4-; б) [Ag(NH3)(H2O)]+;
в) [Cr(H2O)6]3+.
Определите степень окисления указанных комплексообразователей.
307. Укажите координационное число и степень окисления центрального атома металла в каждом из следующих координационных соединений:
а) K2[FeCl4];
б) K3[FeCl6];
в) Na3[Cr(C2O4)3];
г) [Pt(NH3)4Cl2]Cl2;
д) [Cr(H2O)5Cl]Cl2.
Напишите соответствующие им выражения констант нестойкости комплексных ионов.
308. Укажите названия соединений, определите степень окисления комплексообразователя:
а) [Cr(NH3)6]Cl3;
б) [Cu(NH3)4]SO4;
в) K4[Fe(CN)6];
г)Na2[Be(OH)4];
д) [Co(NH3)3Cl3];
е)K[Pt(NH3)Cl3].
Составьте уравнения электролитической диссоциации перечисленных веществ и запишите соответствующие им выражения констант нестойкости комплексных ионов.
309. Напишите формулы комплексных соединений по указанным названиям:
а) хлорид тетрааммин цинка (II),
б) тетраиодокобальтат (III) натрия.
Составьте уравнение реакции между указанными соединениями и раствором KNO2 в молекулярной и ионно-молекулярной формах. Назовите образующиеся комплексные соединение.
310. Пользуясь таблицей констант нестойкости (см. табл.3 Приложений), определите, в каких случаях произойдет взаимодействие между растворами электролитов. Укажите для этих случаев молекулярные и ионные формы уравнений:
а) [Cr(H2O)6]Cl3 + 6KNСS 
б) K[Ag(NO2)2] + NH4OH 
в) [Ni(NH3)4]Cl2 + NaCN 
311. Приведите схемы диссоциации и выражения констант нестойкости следующих комплексных ионов:
а) [Fe(CN)6]3-;
б) [Fe(CN)6]4-;
в) [Ag(NH3)2]+;
г)[Ag(NH3)(H2O)]+;
д) [Cr(H2O)6]3+.
Определите степени окисления указанных комплексообразователей.
312. Эмпирическая формула соли CrCl3×5 H2O. Исходя из того, что координационное число хрома равно шести, определите, какой объем 1 н. раствора AgNO3 понадобится для осаждения внешнесферно связанного хлора, содержащегося в 300мл 0,1 М раствора комплексной соли. При вычислениях считать, что вся вода, входящая в состав соли, связана внутрисферно.
313. При взаимодействии раствора [Cu(NH3)4]Cl2 c раствором KCN образуется соль K2[Cu(CN)4]. Составьте уравнение реакции и объясните причину её протекания.
314. Определите величину и знак заряда перечисленных ниже комплексных ионов:
[Cr(H2O)4Cl2]; [Pt(NH3)3Cl3]; [Ag(CN)2]; [Co(NO2)6]; [Cr(NH3)5Cl]; [PtCl6], имея в виду, что комплексообразователями являются катионы Cr,3+Pt,4+ Ag+, Co3+. Приведите названия комплексных соединений.
315. Бромид кобальта образует с аммиаком следующие соединения:
CoBr3×6NH3; CoBr3×5NH3×H2O; CoBr3×5NH3; CoBr3×4NH3.
Действие раствора AgNO3 приводит к практически полному осаждению всего брома из первых двух соединений, около 2/3 брома из третьего соединения и около 1/3 брома из четвертого. Определите координационное число атома кобальта. Изобразите строение указанных комплексных соединений и составьте уравнения реакций их с нитратом серебра в молекулярной и ионной формах.
316. В чем заключается различие между комплексными и двойными солями с точки зрения ионной теории? Составьте уравнения диссоциации на ионы перечисленных ниже комплексных и двойных солей: Na3[Co(СN)6]; [Cr(H2O)4Cl2]Cl; KAl(SO4)2; KMgCl3. Назовите комплексные соли, укажите валентность и координационное число их комплексообразователей. При добавлении к каким из указанных солей раствора щелочи выпадет осадок гидроксида металла?
317. Составьте уравнение реакции в молекулярной и ионной формах, которые соответствуют следующим схемам:
а) K2[HgBr4]  K2[HgI4];
K2[HgI4];
б) K[Ag(NO2)2] 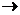 [Ag(NH3)2]NO2.
[Ag(NH3)2]NO2.
Укажите, какие комплексные ионы в указанных схемах, исходные или конечные, характеризуются меньшими по величине константами нестойкости. Почему?
318. На комплексные соединения CoCl2·6NH3 и CoCl2·5NH3 подействовали раствором AgNO3. На 1 моль одного соединения для осаждения хлора пошло 3 моля , а на 1 моль второго – 2 моль AgNO3. Укажите координационные формулы этих соединений и определите заряды комплексных ионов.
319. Составьте молекулярное уравнение реакции, протекающей по схеме:
[Fe(CN)6]4- + MnO4- + 8 H+ 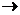 [Fe(CN)6]3- + Mn2+ + 4H2O.
[Fe(CN)6]3- + Mn2+ + 4H2O.
Определите степени окисления комплексообразователей и напишите выражения констант нестойкости комплексных анионов.
320. Укажите координационное число и степень окисления центрального атома металла в каждом из следующих координационных соединений:
а) K2[ВeCl4];
б) K3[Fe(CN)6];
в) [Pt(NH3)4Cl2]Cl2;
д) [Cr(H2O)4Cl2]Cl.
Напишите соответствующие им выражения констант нестойкости комплексных ионов
