Опыт 2. Точное определение рН растворов потенциометрическим методом
Для выполнения опыта необходимы: универсальный иономер ЭВ-74, электрод сравнения (каломельный электрод), индикаторный или измерительный электрод, набор растворов электролитов, дистиллированная вода, стаканчики вместимостью 50 мл, фильтровальная бумага.
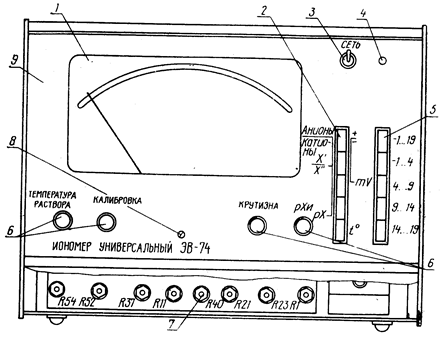 |
Для точного определения рН потенциометрическим методом необходимо подобрать набор растворов кислот и щелочей различных концентраций, в том числе те растворы, которыми пользовались в опыте 1. Значение рН каждого из этих растворов определяется с помощью иономера ЭВ-74 (рис. 2).
Рис. 2. Преобразователь (вид спереди) иономер:
1 – показывающий прибор; 2 – кнопки выбора рода работы;
3 – выключатель сети; 4 – индикация включения;
5 – кнопки выбора диапазона; 6 – ручки оперативного управления
Порядок определения рН растворов на иономере ЭВ-74
1. Включают прибор в сеть, предварительно нажав кнопку “t” и кнопку любого диапазона измерения рН в правом ряду кнопок, дают прибору прогреться в течение 20-30 минут.
2. Стеклянный и каломельный электроды укрепляют в держателе штатива. Стеклянный электрод присоединяют к гнезду прибора “изм”, а каломельный к гнезду “всп” на задней стенке прибора. Из каломельного электрода вынимают пробочку бокового ответвления для лучшего контакта электрода и исследуемого раствора.
3. Помещают электроды в стаканчик с исследуемым раствором.
4. Нажимают следующие клавиши: “1-19”, “анионы-катионы”, “рХи”.
5. Считывают значение рН раствора по стрелке с нижней шкалы панели прибора. Время установки значений рН 1-2 минуты.
6. Для более точного измерения рН используют клавиши диапазонов: “1-4”, “4-9”, “9-14” или “14-19”, снятие показаний производится по верхней шкале прибора “0-5”. Например, при нажатой кнопке диапазона “4-9” стрелка прибора остановилась на отметке 2 верхней шкалы “0-5”. Прибавив к начальному значению рН этого диапазона (4) величину 2, получаем искомое значение рН = 4 + 2 = 6.
Полученные данные записывают в табл. 4.
Таблица 4
Результаты определения рН растворов
| Раствор | Концентрация раствора | рН раствора |
В выводе сравните индикаторный и потенциометрический методы по точности определения значения рН.
Опыт 3. Гидролиз солей. Определение степени гидролиза солей методом
Измерения рН растворов
Для выполнения опыта необходимы: универсальный иономер ЭВ-74, электрод сравнения (каломельный электрод), индикаторный или измерительный электрод, набор растворов электролитов, дистиллированная вода, стаканчики вместимостью 50 мл, фильтровальная бумага.
Гидролиз солей - это реакция взаимодействия ионов воды с ионами растворенных в ней солей с образованием слабого электролита.
Гидролиз обнаруживается по смещению равновесия реакции диссоциации воды: Н2О ⇄ Н+ + ОН–, вследствие связывания одного или двух ионов воды ионами соли с образованием слабодиссоциирующего или нерастворимого продукта. Гидролиз – процесс, обратный реакции нейтрализации.
Количественно гидролиз определяется по степени гидролиза h. Для вещества, подвергающегося гидролизу, степень гидролиза – это отношение числа молекул, подвергшихся гидролизу, к общему числу растворенных молекул. Степень гидролиза зависит от константы гидролиза, а также от температуры и от концентрации соли.
Для определения степени гидролиза солей необходимо:
Этап 1. Измерить рН воды и рассчитать концентрации ионов Н+ и ОН– .
Этап 2. Измерить рН растворов солей заданных молярных концентраций.
Этап 3. Рассчитать значение концентраций ионов Н+ или ОН−, образующихся в растворе за счет процесса гидролиза данной соли.
Этап 1. Измерение рН дистиллированной воды и расчет концентрации ионов Н+ + ОН− в воде.В стакан емкостью 50 мл наливают 25 мл дистиллированной воды и измеряют рН. Зная значение рН, определяют СН+, а затем, используя значение ионного произведения воды, определяют СОН-.
Этап 2. Измерение рН растворов солей заданных молярных концен- траций и расчет концентраций ионов Н+ и ОН– в этих растворах.В стакан емкостью 50 мл наливают 25 мл одного из растворов по указанию преподавателя и проводят измерение рН среды с помощью универсального иономера ЭВ-74. Результаты измерений заносят в табл. 5 и записывают уравнение гидролиза взятой для исследования соли в молекулярном и ионном виде.
Таблица 5
Результаты исследования гидролиза растворов солей
| Раствор | Концентрация раствора | рН раствора | Вывод по гидролизу соли (по катиону или по аниону, полный или частичный гидролиз) |
Этап 3. Расчет степени гидролиза (h) данной соли.Расчет степени гидролиза исследуемой соли проводят следующим образом.
Для кислотного гидролиза используют формулу
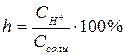 . (5)
. (5)
Для щелочного гидролиза используют формулу
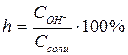 , (6)
, (6)
где СН+ , СОН- и Ссоли – молярные концентрации соответственно ионов Н+ , ОН– и соли (в моль/л).
В выводе укажите, подвергается ли изучаемая соль гидролизу ? По скольким ступеням проходит гидролиз? Протекает ли полный гидролиз или он идет частично, какие продукты гидролиза указывают на полный или частичный гидролиз ? Является ли гидролиз данной соли обратимым или он необратим ?
