Параметры состояния. Законы и уравнения состояния идеальных газов.
Параметры состояния. Законы и уравнения состояния идеальных газов.
1.4; 3.11; 3.15; 3.22; 3.23.
1.4 В машинном зале электростанции работают три турбины, в конденсаторах которых поддерживается абсолютное давление p1 = 2,94 кПа, р2 = 3,923 кН/м2 и р3 = 0,711 lbf/in2. Определите величины вакуумов в процентах барометрического давления. Показание барометра в машинном зале В = 753 мм рт. ст.
Решение. Давление:
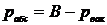 ,
,
где 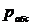 - абсолютное давление;
- абсолютное давление;
В – барометрическое (атмосферное) давление;
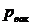 - давление разряжения (вакуум).
- давление разряжения (вакуум).
Тогда 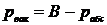 . Выражаем все в Па (таблица 5, с. 291, [3]).
. Выражаем все в Па (таблица 5, с. 291, [3]).
1) p1 = 2,94 кПа = 2940 Па; 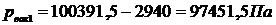 ;
; 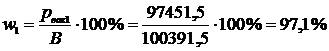 ;
;
2) р2 = 3,923 кН/м2 = 3,923 кПа = 3923 Па; 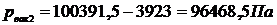 ;
; 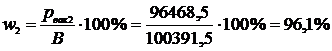
3) 10 lbf/in2 = 0,68948·105 Па
0,711 lbf/in2 = р3. р3 = 4902,2 Па. 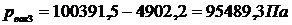 ;
; 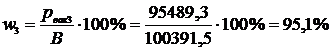
4) 103 мм рт. ст. = 1,33322·105 Па
753 мм рт. ст. = В. В = 100391,5 Па.
Ответ: 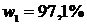 ,
, 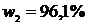 ,
, 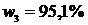 .
.
3.11 Определите массу воздуха, находящегося в комнате площадью 25 м2 и высотой 3,2 м. Принять, что температура воздуха в комнате t = 220С, а барометрическое давление В = 986,5 гПа.
Решение.Уравнение состояния идеальных газов 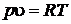 , для произвольной массы газа m, кг:
, для произвольной массы газа m, кг:
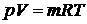 ,
,
где р – абсолютное давление, Па;
V – объем, м3;
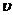 - удельный объем, м3/кг;
- удельный объем, м3/кг;
Т – температура, К;
R – удельная газовая постоянная, Дж/(кг·К).
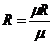 ,
,
где 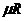 - универсальная газовая постоянная, Дж/(кмоль·К).
- универсальная газовая постоянная, Дж/(кмоль·К).
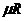 = 8314,51 Дж/(кмоль·К)
= 8314,51 Дж/(кмоль·К)
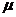 - молекулярная масса, кг/ кмоль (таблица 7, с. 292, [3])
- молекулярная масса, кг/ кмоль (таблица 7, с. 292, [3])
Газовая постоянная 1 кг газа R = 8314,51/ 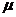 .
.
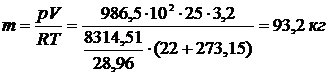
Ответ: 93,2 кг.
3.15 В комнате площадью 35 м2 и высотой 3,1 м воздух находится при t = 230C и барометрическом давлении В = 973 гПа. Какое количество воздуха проникнет с улицы в комнату, если барометрическое давление увеличится до В = 1013 гПа. Температура воздуха остается постоянной.
Решение. 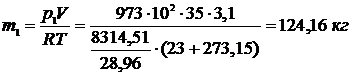
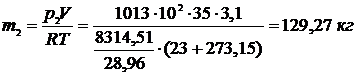
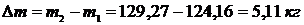 .
.
Ответ : 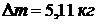
3.22 При температуре t = 8000C и давлении р = 0,1 МПа плотность газа 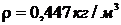 . Что это за газ?
. Что это за газ?
Решение. 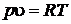 ,
, 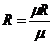 →
→ 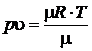 ,
, 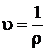 .Откуда
.Откуда 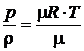 . Следовательно,
. Следовательно, 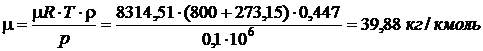
По таблице 7, с. 292 [3] определяем по молекулярной массе, что искомый газ – аргон.
Ответ:аргон.
3.23 Компрессор подает кислород в резервную емкость 3 м 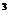 . Избыточное давление в резервуаре увеличивается при этом от 0,01 до 0,6 МПа, а температура газа – от 15 до 30 0С. Определите массу поданного компрессором кислорода. Барометрическое давление 993гПа.- гекто
. Избыточное давление в резервуаре увеличивается при этом от 0,01 до 0,6 МПа, а температура газа – от 15 до 30 0С. Определите массу поданного компрессором кислорода. Барометрическое давление 993гПа.- гекто
Решение. 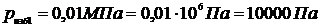
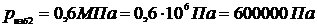
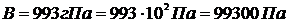
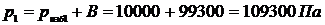 ,
, 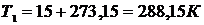
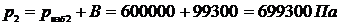 ,
, 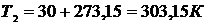
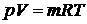
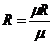 =
= 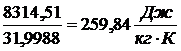
Изначальное количество кислорода, кг, в резервуаре:
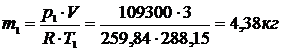
После подачи кислорода компрессором, кг:
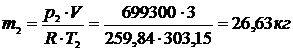
Масса поданного компрессором кислорода:
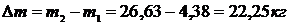
Ответ: 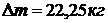 .
.
Решение.
1) Используя [5, табл. III, с.47] определяем, что это перегретый пар;
2) Используя [5, табл. II, с.26] определяем
р = 0,4 МПа = 4·105 Па. При этом давлении 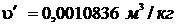
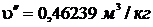
Т.к. 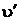 <
< 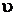 <
< 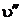 , т.е. 0,0010836<0,015<0,46239, то состояние воды – влажный пар.
, т.е. 0,0010836<0,015<0,46239, то состояние воды – влажный пар.
3) Используя [5, табл. I, с.19] определяем
t = 1700С. При этой температуре 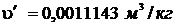
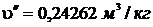
Т.к. 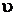 <
< 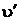 , т.е. 0,00105<0,0011143, то состояние воды – жидкость.
, т.е. 0,00105<0,0011143, то состояние воды – жидкость.
4) Используя [5, табл. II, с.31] определяем
р = 18,2 МПа = 1,82·107 Па. При этом давлении t = 357,900С. Поэтому, это может быть состояние кипящей жидкости, влажного пара, сухого насыщенного пара.
Ответ:1) перегретый пар; 2) влажный пар; 3) жидкость; 4) кипящая жидкость, влажный пар, сухой насыщенный пар.
9.5 В сосуде объемом V = 500 см3 находится в равновесии смесь сухого насыщенного пара и кипящей воды общей массой m = 0,05 кг. Температура внутри сосуда t = 310 0С. Найдите степень сухости смеси.
Решение. Удельный объем влажного пара: 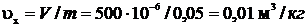
Используя [5, табл. I, с.22] определяем
t = 310 0С. При этой температуре 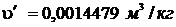
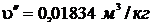
Степень сухости: 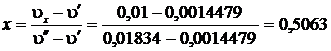 или х = 50,63%
или х = 50,63%
Ответ: х = 50,63%.
9.6 В барабане котельного агрегата находится кипящая вода и над ней водяной пар под давлением р = 9 МПа. Масса воды m = 5000 кг. Объем барабана V = 8 м3. Какова масса пара, находящегося над зеркалом испарения, если пар считать сухим насыщенным?
Решение. Удельный объем влажного пара: 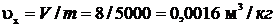
Используя [5, табл. II, с.30] определяем
р = 9 МПа = 9·106 Па. При этом давлении 

Степень сухости: 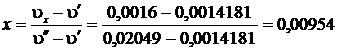
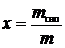 , откуда масса сухого насыщенного пара:
, откуда масса сухого насыщенного пара: 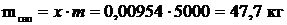 .
.
Ответ: 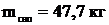 .
.
9.9 В резервуаре объемом 5 м3 находится влажный пар со степенью сухости х = 0,3. Определите массу влажного пара, объем, занимаемый водой, и объем, занимаемый сухим насыщенным паром. Давление в резервуаре р = 19,0 МПа.
Решение. Масса влажного пара: 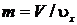
Удельный объем влажного пара: 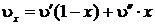
Используя [5, табл. II, с.31] определяем
р = 19 МПа = 1,9·107 Па. При этом давлении 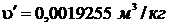
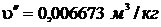
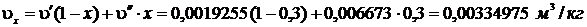
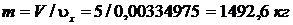
Объем, занимаемый сухим насыщенным паром: 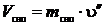
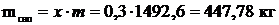
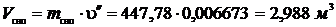
Масса воды равна: 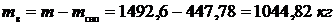
Объем, занимаемый водой:  .
.
Ответ: 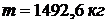 ;
; 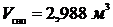 ;
; 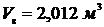 .
.
9.29 К питательной воде, вводимой в прямоточный паровой котел при р = 24 МПа и t = 350 0С в количестве D = 900·103 кг/ч, от топочных газов подводится Q = 1600 ГДж/ч теплоты. Определите температуру пара на выходе из парового котла, его энтальпию и внутреннюю энергию. Падением давления при протекании воды и пара по трубам пренебречь. Представьте процесс в Т, s – и h, s – диаграммах.
Решение. Теплота, подводимая от топочных газов 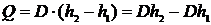 , откуда
, откуда 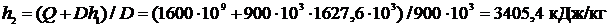
h1 определяли по [5, табл. III, с.67] при р = 24 МПа и t = 350 0С.
Значение энтальпии 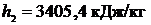 находится между значениями 3382,3 кДж/кг и 3413,2 кДж/кг [5, табл. III, с.68], что соответствует температурам 560 0С и 570 0С. Значит, искомая температура t2 находится в пределах от 560 0С до 570 0С. Проинтерполируем:
находится между значениями 3382,3 кДж/кг и 3413,2 кДж/кг [5, табл. III, с.68], что соответствует температурам 560 0С и 570 0С. Значит, искомая температура t2 находится в пределах от 560 0С до 570 0С. Проинтерполируем:
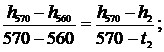
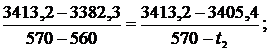 откуда t2 = 567,48 0C.
откуда t2 = 567,48 0C.
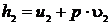 ;
; 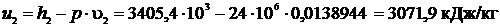
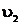 определяли по [5, табл. III, с.68] при р = 24 МПа и t2 = 567,48 0С.
определяли по [5, табл. III, с.68] при р = 24 МПа и t2 = 567,48 0С.
Ответ: 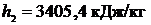 ; t2 = 567,48 0C;
; t2 = 567,48 0C; 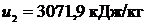 .
.
9.40Водяной пар, имеющий параметры р1 = 3,4 МПа и х1 = 98%, изоэнтропно сжимается до р2 = 9,0 МПа. Найдите температуру и энтальпию пара в конечном состоянии. Определите работу сжатия и изменение внутренней энергии 1 кг пара. Задачу решите, пользуясь таблицами. Проверьте результат по h, s – диаграмме.
Решение. 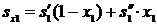 , кДж/(кг·К)
, кДж/(кг·К)
Используя [5, табл. II, с.28] определяем
р1 = 3,4 МПа = 3,4·106 Па. При этом давлении 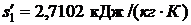
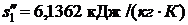
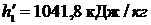
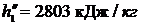
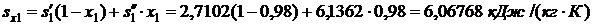 .
.
Т.к. водяной пар сжимается изоэнтропно, то 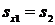
Используя [5, табл. III, с.57] определяем, что наше значение 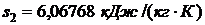 находится между значениями 6,0378 кДж/(кг·К) и 6,0940 кДж/(кг·К) [5, табл. III, с.57], что соответствует температурам 350 0С и 360 0С. Значит, искомая температура t2 находится в пределах от 350 0С до 360 0С. Проинтерполируем:
находится между значениями 6,0378 кДж/(кг·К) и 6,0940 кДж/(кг·К) [5, табл. III, с.57], что соответствует температурам 350 0С и 360 0С. Значит, искомая температура t2 находится в пределах от 350 0С до 360 0С. Проинтерполируем:
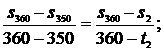
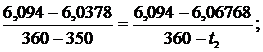 откуда t2 = 355,32 0C. Аналогично для энтальпии
откуда t2 = 355,32 0C. Аналогично для энтальпии
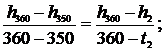
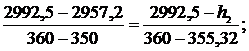 откуда h2 = 2975,98 кДж/кг
откуда h2 = 2975,98 кДж/кг
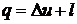 , т.к. процесс – адиабатный, т.е протекающий без теплообмена с окружающей средой, то
, т.к. процесс – адиабатный, т.е протекающий без теплообмена с окружающей средой, то 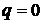 , а
, а 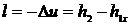
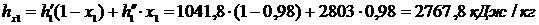
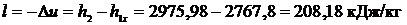 .
.
Ответ: t2 = 355,32 0C; h2 = 2975,98 кДж/кг; 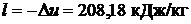 .
.
9.41 Покрытый тепловой изоляцией резервуар объемом V = 10 м3 наполовину заполнен водой при температуре насыщения и наполовину сухим насыщенным паром. Давление в резервуаре р1 = 9,0 МПа. Быстро открывая задвижку (рис. 9.9), выпускают пар в атмосферу до тех пор, пока давление в резервуаре р2 не становится равным 6,0 МПа, после чего задвижку закрывают. Сколько килограммов пара выпускается в атмосферу? Какой объем будет занимать пар, оставшийся в барабане после закрытия задвижки? Процесс изменения состояния Н2О в резервуаре считать изоэнтропным.
Решение. Т.к. резервуар объемом V = 10 м3 наполовину заполнен водой при температуре насыщения и наполовину сухим насыщенным паром, то Vснп = 5 м3 и Vж = 5 м3.
Масса сухого насыщенного пара: 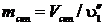 ,
,
масса жидкости: 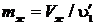 .
.
Используя [5, табл. II, с.30] определяем
р1 = 9 МПа = 9·106 Па. При этом давлении 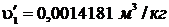 ;
;
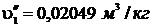 ;
;
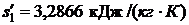 ;
;
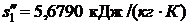 .
.
Тогда 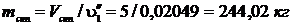 ,
,
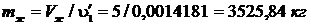 .
.
Масса влажного пара до открытия задвижки: 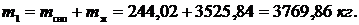
Степень сухости: 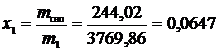 .
.
Энтропия влажного пара до открытия задвижки: 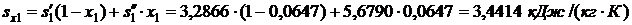 .
.
По условию задачи процесс изменения состояния Н2О в резервуаре считать изоэнтропным, то 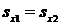 .
.
Используя [5, табл. II, с.29] определяем
р2 = 6 МПа = 6·106 Па. При этом давлении 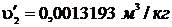 ;
;
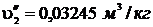 ;
;
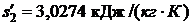 ;
;
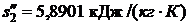 .
.
Энтропия влажного пара после закрытия задвижки: 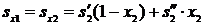 , тогда
, тогда
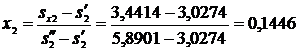 .
.
Удельный объем влажного пара после закрытия задвижки: 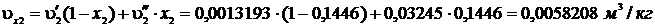 Масса влажного пара после закрытия задвижки:
Масса влажного пара после закрытия задвижки: 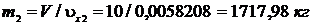 .
.
Масса пара, выпущенного в атмосферу: 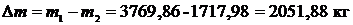 .
.
Объем, который будет занимать пар, оставшийся в барабане после закрытия задвижки: 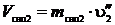
Масса сухого насыщенного пара после закрытия задвижки: 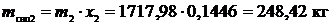
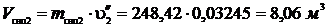
Ответ: 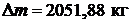 ;
; 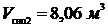 .
.
Решение.
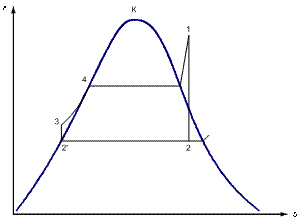
Термический КПД цикла Ренкина:
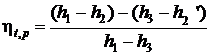 ,
,
где h1 – энтальпия пара перед турбиной;
h2 – энтальпия пара на входе в конденсатор;
h2’ – энтальпия воды на выходе из конденсатора;
h3 – энтальпия воды после насоса (энтальпия питательной воды).
Термический КПД цикла Карно:
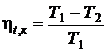 ,
,
где Т1 – температура теплоисточника;
Т2 – температура холодного источника.
Используя [5, табл. III, с.58] определяем при р1 = 10 МПа и температуре t1 = 530 0С, что h1 = 3451,7 кДж/кг, s1 = 6,6965 кДж/(кг·К).
s1 = s2
Используя [5, табл. II, с.24] определяем
р2 = 40 гПа = 4·103 Па. При этом давлении 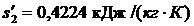 ;
;
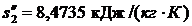 ;
;
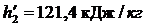 ;
;
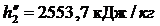 .
.
t2 = 28,96 0C.
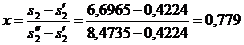
Энтальпия пара на входе в конденсатор:
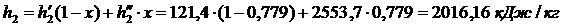
Энтальпия воды на выходе из конденсатора: 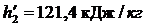 и энтропия
и энтропия 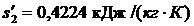 .
.
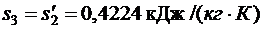
Используя [5, табл. III, с.57] при р1 = 10 МПа определяем, что наше значение 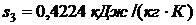 находится между значениями 0,2944 кДж/(кг·К) и 0,4337 кДж/(кг·К) [5, табл. III, с.57], что соответствует температурам 20 0С и 30 0С. Значит, искомая температура t3 находится в пределах от 20 0С до 30 0С. Проинтерполируем:
находится между значениями 0,2944 кДж/(кг·К) и 0,4337 кДж/(кг·К) [5, табл. III, с.57], что соответствует температурам 20 0С и 30 0С. Значит, искомая температура t3 находится в пределах от 20 0С до 30 0С. Проинтерполируем:
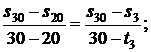
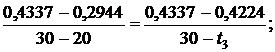 откуда t3 = 29,19 0C.
откуда t3 = 29,19 0C.
Тогда для энтальпии
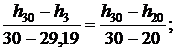
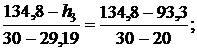 откуда h3 = 131,44 кДж/кг
откуда h3 = 131,44 кДж/кг
Термический КПД цикла Ренкина:
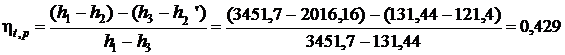 .
.
Термический КПД цикла Карно:
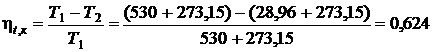 .
.
Ответ: 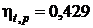 ;
; 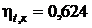 .
.
14.6 При одинаковой начальной температуре t1 = 500 0C постройте кривую зависимости 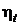 цикла паротурбинной установки от начального давления р1, приняв его равным 5,0; 10,0; 15,0 и 20,0 МПа. Давление в конденсаторе одинаково, р2 = 40 гПа. Учтите работу питательного насоса. Представьте циклы в T,s – диаграмме.
цикла паротурбинной установки от начального давления р1, приняв его равным 5,0; 10,0; 15,0 и 20,0 МПа. Давление в конденсаторе одинаково, р2 = 40 гПа. Учтите работу питательного насоса. Представьте циклы в T,s – диаграмме.
Решение.

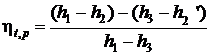
1) Используя [5, табл. III, с.54] определяем при р1 = 5 МПа и температуре t1 = 500 0С, что h1 = 3434,5 кДж/кг, s1 = 6,9778 кДж/(кг·К).
s1 = s2
Используя [5, табл. II, с.24] определяем
р2 = 40 гПа = 4·103 Па. При этом давлении 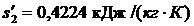 ;
;
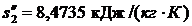 ;
;
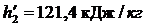 ;
;
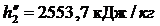 .
.
t2 = 28,96 0C.
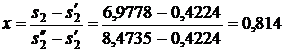
Энтальпия пара на входе в конденсатор:
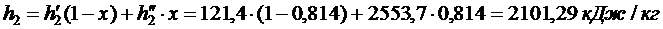 Энтальпия воды на выходе из конденсатора:
Энтальпия воды на выходе из конденсатора: 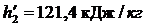 и энтропия
и энтропия 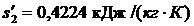 .
.
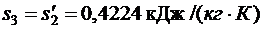
Используя [5, табл. III, с.53] при р1 = 5 МПа определяем, что наше значение 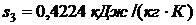 находится между значениями 0,2955 кДж/(кг·К) и 0,4353 кДж/(кг·К) [5, табл. III, с.53], что соответствует температурам 20 0С и 30 0С. Значит, искомая температура t3 находится в пределах от 20 0С до 30 0С. Проинтерполируем:
находится между значениями 0,2955 кДж/(кг·К) и 0,4353 кДж/(кг·К) [5, табл. III, с.53], что соответствует температурам 20 0С и 30 0С. Значит, искомая температура t3 находится в пределах от 20 0С до 30 0С. Проинтерполируем:
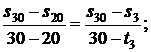
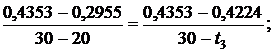 откуда t3 = 29,08 0C.
откуда t3 = 29,08 0C.
Тогда для энтальпии
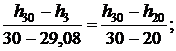
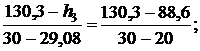 откуда h3 = 126,46 кДж/кг
откуда h3 = 126,46 кДж/кг
Термический КПД цикла Ренкина:
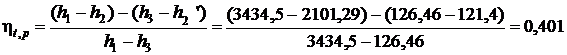
2) Используя [5, табл. III, с.58] определяем при р1 = 10 МПа и температуре t1 = 500 0С, что h1 = 3375,1 кДж/кг, s1 = 6,5993 кДж/(кг·К).
s1 = s2
Используя [5, табл. II, с.24] определяем
р2 = 40 гПа = 4·103 Па. При этом давлении 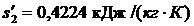 ;
;
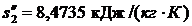 ;
;
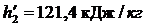 ;
;
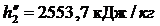 .
.
t2 = 28,96 0C.
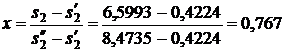
Энтальпия пара на входе в конденсатор:
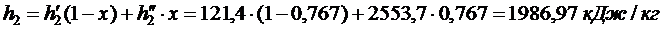 Энтальпия воды на выходе из конденсатора:
Энтальпия воды на выходе из конденсатора: 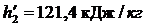 и энтропия
и энтропия 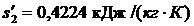 .
.
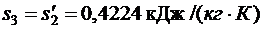
Используя [5, табл. III, с.57] при р1 = 10 МПа определяем, что наше значение 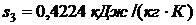 находится между значениями 0,2944 кДж/(кг·К) и 0,4337 кДж/(кг·К) [5, табл. III, с.57], что соответствует температурам 20 0С и 30 0С. Значит, искомая температура t3 находится в пределах от 20 0С до 30 0С. Проинтерполируем:
находится между значениями 0,2944 кДж/(кг·К) и 0,4337 кДж/(кг·К) [5, табл. III, с.57], что соответствует температурам 20 0С и 30 0С. Значит, искомая температура t3 находится в пределах от 20 0С до 30 0С. Проинтерполируем:
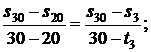
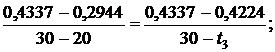 откуда t3 = 29,19 0C.
откуда t3 = 29,19 0C.
Тогда для энтальпии
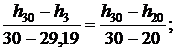
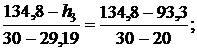 откуда h3 = 131,44 кДж/кг
откуда h3 = 131,44 кДж/кг
Термический КПД цикла Ренкина:
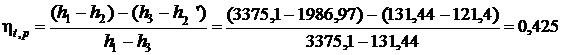
3) Используя [5, табл. III, с.64] определяем при р1 = 15 МПа и температуре t1 = 500 0С, что h1 = 3310,8 кДж/кг, s1 = 6,3479 кДж/(кг·К).
s1 = s2
Используя [5, табл. II, с.24] определяем
р2 = 40 гПа = 4·103 Па. При этом давлении 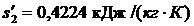 ;
;
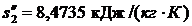 ;
;
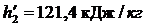 ;
;
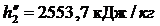 .
.
t2 = 28,96 0C.
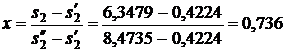
Энтальпия пара на входе в конденсатор:
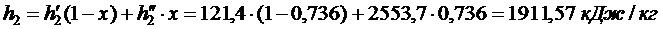 Энтальпия воды на выходе из конденсатора:
Энтальпия воды на выходе из конденсатора: 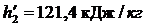 и энтропия
и энтропия 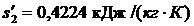 .
.
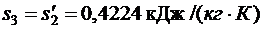
Используя [5, табл. III, с.63] при р1 = 15 МПа определяем, что наше значение 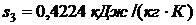 находится между значениями 0,2932 кДж/(кг·К) и 0,4322 кДж/(кг·К) [5, табл. III, с.63], что соответствует температурам 20 0С и 30 0С. Значит, искомая температура t3 находится в пределах от 20 0С до 30 0С. Проинтерполируем:
находится между значениями 0,2932 кДж/(кг·К) и 0,4322 кДж/(кг·К) [5, табл. III, с.63], что соответствует температурам 20 0С и 30 0С. Значит, искомая температура t3 находится в пределах от 20 0С до 30 0С. Проинтерполируем:
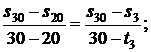
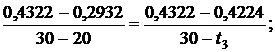 откуда t3 = 29,29 0C.
откуда t3 = 29,29 0C.
Тогда для энтальпии
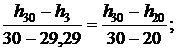
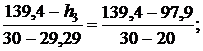 откуда h3 = 136,45 кДж/кг
откуда h3 = 136,45 кДж/кг
Термический КПД цикла Ренкина:
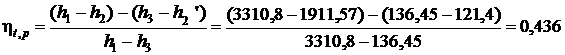
4) Используя [5, табл. III, с.66] определяем при р1 = 20 МПа и температуре t1 = 500 0С, что h1 = 3241,2 кДж/кг, s1 = 6,1445 кДж/(кг·К).
s1 = s2
Используя [5, табл. II, с.24] определяем
р2 = 40 гПа = 4·103 Па. При этом давлении 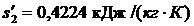 ;
;
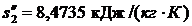 ;
;
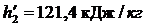 ;
;
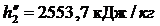 .
.
t2 = 28,96 0C.
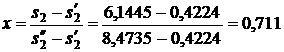
Энтальпия пара на входе в конденсатор:
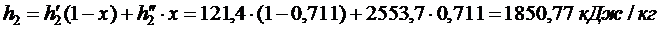 Энтальпия воды на выходе из конденсатора:
Энтальпия воды на выходе из конденсатора: 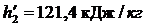 и энтропия
и энтропия 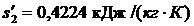 .
.
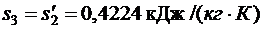
Используя [5, табл. III, с.65] при р1 = 20 МПа определяем, что наше значение 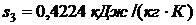 находится между значениями 0,2921 кДж/(кг·К) и 0,4306 кДж/(кг·К) [5, табл. III, с.65], что соответствует температурам 20 0С и 30 0С. Значит, искомая температура t3 находится в пределах от 20 0С до 30 0С. Проинтерполируем:
находится между значениями 0,2921 кДж/(кг·К) и 0,4306 кДж/(кг·К) [5, табл. III, с.65], что соответствует температурам 20 0С и 30 0С. Значит, искомая температура t3 находится в пределах от 20 0С до 30 0С. Проинтерполируем:
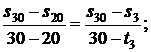
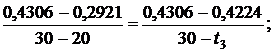 откуда t3 = 29,41 0C.
откуда t3 = 29,41 0C.
Тогда для энтальпии
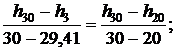
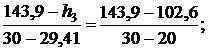 откуда h3 = 141,46 кДж/кг
откуда h3 = 141,46 кДж/кг
Термический КПД цикла Ренкина:
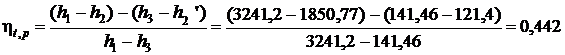
Ответ: р1, МПа 5 10 15 20
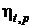 0,401 0,425 0,436 0,442
0,401 0,425 0,436 0,442
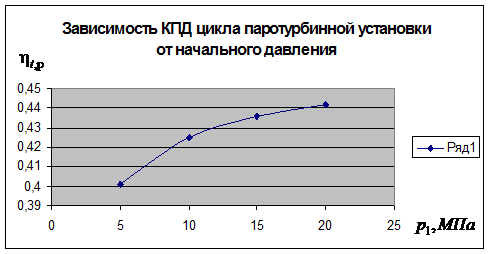
15.1 Воздушная холодильная машина должна обеспечить температуру в охлаждаемом помещении tохл = 5 0C при температуре окружающей среды tо.с. = 20 0C. Холодопроизводительность машины 840 МДж/ч. Давление воздуха на выходе из компрессора р2 = 0,5 МПа, давление в холодильной камере р1 = 0,1 МПа. Определите мощность двигателя для привода машины, расход воздуха, холодильный коэффициент и количество теплоты, передаваемое окружающей среде. Подсчитайте холодильный коэффициент машины, работающей по циклу Карно в том же интервале температур. Представьте цикл в T,s – диаграмме.
Решение. Холодильный коэффициент: 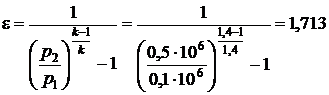 .
.
Мощность двигателя для привода машины: 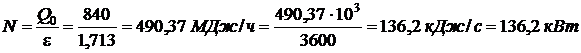
Холодильный коэффициент машины, работающей по циклу Карно: 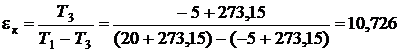
Количество теплоты, передаваемое окружающей среде: 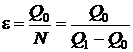 , откуда
, откуда 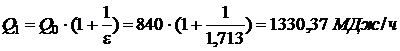 .
.
Удельная холодопроизводительность: 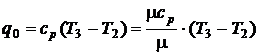
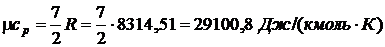 [3, с.36]
[3, с.36]
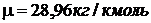
Из соотношения 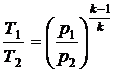 находим
находим 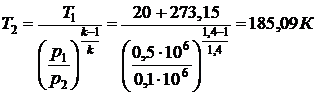 .
.
Тогда 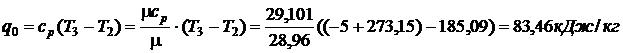
Расход воздуха: 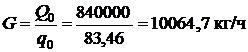
Ответ: 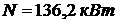 ;
;  ;
; 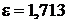 ;
; 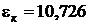 ;
; 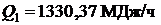 .
.
15.8 Компрессор аммиачной холодильной установки имеет теоретическую мощность 40 кВт. Из компрессора сухой насыщенный пар аммиака при температуре t2 = 25 0C направляется в конденсатор, после которого жидкость в дроссельном вентеле расширяется. Температура испарения аммиака в охлаждаемой среде t1 = -10 0C. Определите холодопроизводительность установки, используя табл. 24 приложения [3].
Решение. Холодопроизводительность установки: 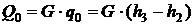
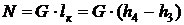 , откуда
, откуда 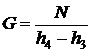 , тогда
, тогда
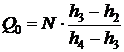
Процесс 1-2 – дросселирование ( 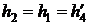 )
)
Процесс 3-4 – адиабатное сжатие ( 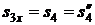 )
)
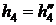 находим по таблице 24 при t = 25 0C
находим по таблице 24 при t = 25 0C 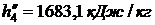
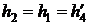 находим по таблице 24 при t = 25 0C
находим по таблице 24 при t = 25 0C 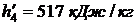
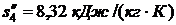 определяли по таблице 24 при t = 25 0C
определяли по таблице 24 при t = 25 0C
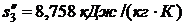 определяли по таблице 24 при t = -10 0C
определяли по таблице 24 при t = -10 0C
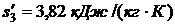 определяли по таблице 24 при t = -10 0C
определяли по таблице 24 при t = -10 0C
Степень сухости 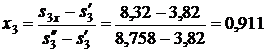
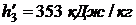 определяли по таблице 24 при t = -10 0C
определяли по таблице 24 при t = -10 0C
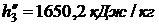 определяли по таблице 24 при t = -10 0C
определяли по таблице 24 при t = -10 0C
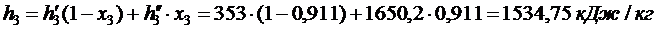
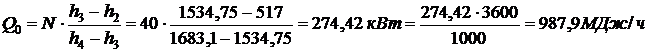 Ответ:
Ответ: 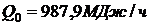
15.13 Современные электрогенераторы работают с применением водородного охлаждения. Циркулирующий в системе водород может быть использован как рабочее вещество в схеме теплового насоса (рис. 15.6). Каков отопительный коэффициент 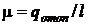 этой установки, если давление водорода в системе охлаждения генератора постоянно: р1 = р4 = 0,097 МПа, а температура в точках 1,3 и 4 указана на схеме.
этой установки, если давление водорода в системе охлаждения генератора постоянно: р1 = р4 = 0,097 МПа, а температура в точках 1,3 и 4 указана на схеме.
Каково давление водорода р2 поступающего в теплообменник. Теплоемкость ср водорода считать не зависящей от температуры.
Решение. Отопительный коэффициент 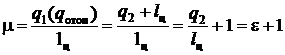 .
.
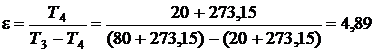 . Тогда
. Тогда 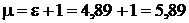 .
.
Подставив значения в формулу 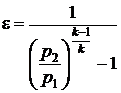 , получим
, получим 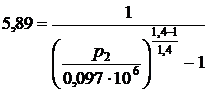 откуда р2 = 186041 Па = 0,186 МПа.
откуда р2 = 186041 Па = 0,186 МПа.
Ответ: 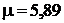 ; р2 = 0,186 МПа.
; р2 = 0,186 МПа.
б) Теплопередача [4]
Решение.
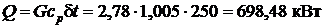
1) для цилиндрической стенки
Коэффициент теплопередачи
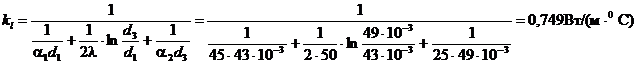
Поверхность нагрева подогревателя: 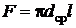 , м2 (1)
, м2 (1)
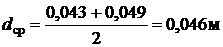
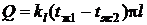 (2)
(2)
Выразив из формулы (2) 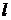 и подставив в уравнение (1), получим
и подставив в уравнение (1), получим
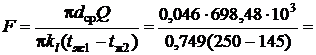
Параметры состояния. Законы и уравнения состояния идеальных газов.
1.4; 3.11; 3.15; 3.22; 3.23.
1.4 В машинном зале электростанции работают три турбины, в конденсаторах которых поддерживается абсолютное давление p1 = 2,94 кПа, р2 = 3,923 кН/м2 и р3 = 0,711 lbf/in2. Определите величины вакуумов в процентах барометрического давления. Показание барометра в машинном зале В = 753 мм рт. ст.
Решение. Давление:
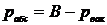 ,
,
где 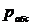 - абсолютное давление;
- абсолютное давление;
В – барометрическое (атмосферное) давление;
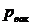 - давление разряжения (вакуум).
- давление разряжения (вакуум).
Тогда 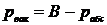 . Выражаем все в Па (таблица 5, с. 291, [3]).
. Выражаем все в Па (таблица 5, с. 291, [3]).
1) p1 = 2,94 кПа = 2940 Па; 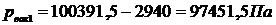 ;
; 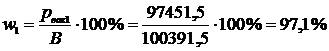 ;
;
2) р2 = 3,923 кН/м2 = 3,923 кПа = 3923 Па; 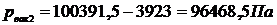 ;
; 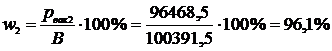
3) 10 lbf/in2 = 0,68948·105 Па
0,711 lbf/in2 = р3. р3 = 4902,2 Па. 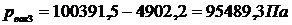 ;
; 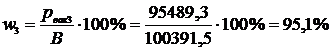
4) 103 мм рт. ст. = 1,33322·105 Па
753 мм рт. ст. = В. В = 100391,5 Па.
Ответ: 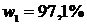 ,
, 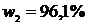 ,
, 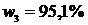 .
.
3.11 Определите массу воздуха, находящегося в комнате площадью 25 м2 и высотой 3,2 м. Принять, что температура воздуха в комнате t = 220С, а барометрическое давление В = 986,5 гПа.
Решение.Уравнение состояния идеальных газов 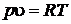 , для произвольной массы газа m, кг:
, для произвольной массы газа m, кг:
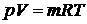 ,
,
где р – абсолютное давление, Па;
V – объем, м3;
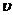 - удельный объем, м3/кг;
- удельный объем, м3/кг;
Т – температура, К;
R – удельная газовая постоянная, Дж/(кг·К).
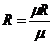 ,
,
где 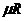 - универсальная газовая постоянная, Дж/(кмоль·К).
- универсальная газовая постоянная, Дж/(кмоль·К).
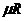 = 8314,51 Дж/(кмоль·К)
= 8314,51 Дж/(кмоль·К)
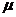 - молекулярная масса, кг/ кмоль (таблица 7, с. 292, [3])
- молекулярная масса, кг/ кмоль (таблица 7, с. 292, [3])
Газовая постоянная 1 кг газа R = 8314,51/ 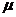 .
.
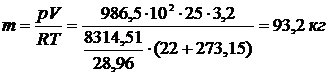
Ответ: 93,2 кг.
3.15 В комнате площадью 35 м2 и высотой 3,1 м воздух находится при t = 230C и барометрическом давлении В = 973 гПа. Какое количество воздуха проникнет с улицы в комнату, если барометрическое давление увеличится до В = 1013 гПа. Температура воздуха остается постоянной.
Решение. 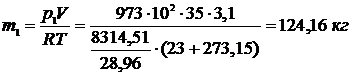
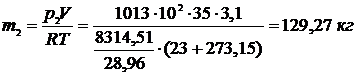
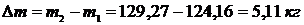 .
.
Ответ : 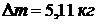
3.22 При температуре t = 8000C и давлении р = 0,1 МПа плотность газа 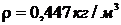 . Что это за газ?
. Что это за газ?
Решение. 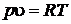 ,
, 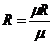 →
→ 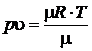 ,
, 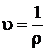 .Откуда
.Откуда 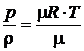 . Следовательно,
. Следовательно, 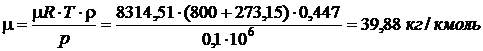
По таблице 7, с. 292 [3] определяем по молекулярной массе, что искомый газ – аргон.
Ответ:аргон.
3.23 Компрессор подает кислород в резервную емкость 3 м 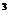 . Избыточное давление в резервуаре увеличивается при этом от 0,01 до 0,6 МПа, а температура газа – от 15 до 30 0С. Определите массу поданного компрессором кислорода. Барометрическое давление 993гПа.- гекто
. Избыточное давление в резервуаре увеличивается при этом от 0,01 до 0,6 МПа, а температура газа – от 15 до 30 0С. Определите массу поданного компрессором кислорода. Барометрическое давление 993гПа.- гекто
Решение. 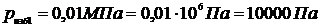
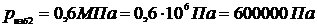
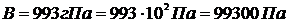
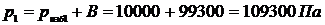 ,
, 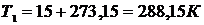
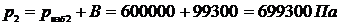 ,
, 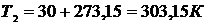
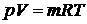
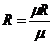 =
= 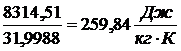
Изначальное количество кислорода, кг, в резервуаре:
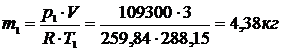
После подачи кислорода компрессором, кг:
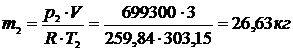
Масса поданного компрессором кислорода:
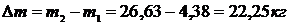
Ответ: 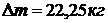 .
.
