Характеристики процессов теплообмена.
Состояние термодинамической системы с точки зрения молекулярной физики характеризуется внутренней энергией. Внутренняя энергия - это энергия движения и взаимодействия атомов и молекул, составляющих данное тело или систему тел.
Процессы обмена внутренней энергией между телами (системами) характеризуют количеством теплоты: Q - для конечного процесса, dQ - для элементарного процесса.
Теплоемкостью тела (системы тел) в процессе теплообмена называют физическую величину, численно равную
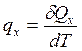 , (1)
, (1)
где:
- dT - изменение температуры;
- “х” – символ процесса (изохорический, изобарический и др.).
В ситуациях, когда qx не зависит или мало зависит от температуры
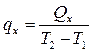 , (2)
, (2)
В этом случае теплоемкость можно определить, как количество теплоты, которое необходимо подвести к системе, чтобы ее температуру увеличить (ответы, чтоб понизить) на единицу принятой шкалы температур (1 °С = 1 К = 0,8 °R = 1,8 F).
Понятие об удельной теплоемкости, как правило, вводят для однородных систем. Тогда удельная теплоемкость в заданном процессе есть и характеристика вещества:

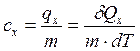 , (3)
, (3)
где m - масса вещества.
Если сх не зависит от температуры, то:
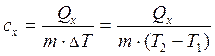 (4)
(4)
Удельная теплоемкость вещества в заданном процессе численно равна тому количеству теплоты, которое необходимо подвести к единице (отвести от единицы) массы вещества, чтобы изменить температуру ее на единицу принятой шкалы температур.
В СИ: 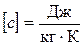 ; в практической системе единиц:
; в практической системе единиц: 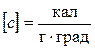 .
.
Может быть введено и использовано для расчетов понятие о молярной теплоемкости:
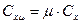 (5)
(5)
Здесь m - в первом случае символ; масса моля во втором.
У конденсированных сред удельная теплоемкость вещества мало зависит от вида процесса и остается практически постоянной в достаточно широком температурном интервале, (данные приводятся в таблицах). Тогда:
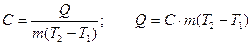 (6)
(6)
Фазовые переходы I рода (плавление, кристаллизация, кипение, конденсация) при заданных внешних условиях (p = const) не сопровождаются изменением температуры. В этом случае вещество характеризуют удельной теплотой фазового перехода
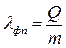 . (7)
. (7)
СИ: 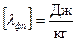 ; практическая система единиц:
; практическая система единиц: 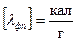 .
.
Удельная теплота фазового перехода показывает, какое количество теплоты нужно подвести к единице массы (отвести от единицы массы) вещества, чтобы его перевести из одного фазового состояния в другое при неизменной температуре.
В процессах плавления и кипения теплота подводится к веществу, при кристаллизации и конденсации это же количество теплоты выделяется веществом (должно быть отведено). Изучение физических свойств вещества предполагает умение экспериментально определять удельную теплоемкость и удельные теплоты фазовых переходов. Для определения этих характеристик можно воспользоваться калориметрическим методом, предложенным академиком Петербургской академии наук Г.В. Рихманом.
Довольно часто приходится пользоваться понятием средней удельной теплоемкости для систем, которые содержат несколько компонентов. Покажем это на примере конденсированных сред.
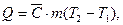 где
где
масса системы m = 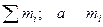 - масса i-го компонента;
- масса i-го компонента;
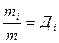 - долевое содержание “i” компонента;
- долевое содержание “i” компонента;
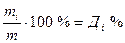 - процентная доля компонента.
- процентная доля компонента.