Аэробный метаболизм пирувата. Окислительное декарбоксилирование пировиноградной кислоты. Механизм действия пируватдегидрогеназного комплекса.
АЭРОБНЫЙ МЕТАБОЛИЗМ ПИРУВАТА
Клетки, недостаточно снабжаемые кислородом, могут частично или полностью существовать за счет энергии гликолиза. Однако большинство животных и растительных клеток в норме находится в аэробных условиях и свое органическое «топливо» окисляет полностью до СО2 и Н2О. В этих условиях пируват, образовавшийся при расщеплении глюкозы, не восстанавливается до лактата, а постепенно окисляется до СО2 и Н2О в аэробной стадии катаболизма, при этом первоначально происходит окислительное декарбоксилирование пирувата с образованием ацетил-КоА.
Окислительное декарбоксилирование
Пировиноградной кислоты
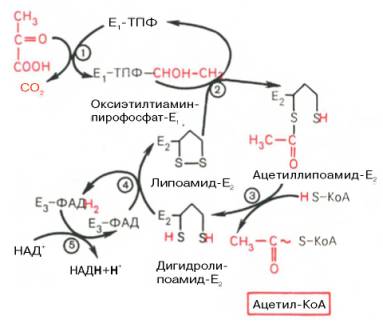
Окисление пирувата до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединенных структурно в мультиферментную систему, получившую название «пируватдегидрогеназный комплекс». На I стадии этого процесса пируват (рис. 10.8) теряет свою карбоксильную группу в результате взаимодействия с тиаминпирофосфатом (ТПФ) в составе активного центра фермента пируватдегидрогеназы (E1). На II стадии оксиэтильная группа комплекса E1–ТПФ–СНОН–СН3 окисляется
с образованием ацетильной группы, которая одновременно переносится на амид липоевой кислоты (кофермент), связанной с ферментом дигидролипоилацетилтрансферазой (Е2). Этот фермент катализирует III стадию – перенос ацетильной группы на коэнзим КоА (HS-KoA) с образованием
конечного продукта ацетил-КоА, который является высокоэнергетическим
(макроэргическим) соединением. На IV стадии регенерируется окисленная форма липоамида из вос-
становленного комплекса дигидролипоамид–Е2. При участии фермента дигидролипоилдегидрогеназы (Е3) осуществляется перенос атомов водорода от восстановленных сульфгидрильных групп дигидролипоамида на ФАД, который выполняет роль простетической группы данного фермента и прочно с ним связан. На V стадии восстановленный ФАДН2 дигидролипоилдегидрогеназы передает водород на кофермент НАД с образованием НАДН + Н+. Процесс окислительного декарбоксилирования пирувата происходит
в матриксе митохондрий. В нем принимают участие (в составе сложного мультиферментного комплекса) 3 фермента (пируватдегидрогеназа, дигидролипоилацетилтрансфераза, дигидролипоилдегидрогеназа) и 5 коферментов (ТПФ, амид липоевой кислоты, коэнзим А, ФАД и НАД), изкоторых три относительно прочно связаны с ферментами (ТПФ-E1, липоамид-Е2 и ФАД-Е3), а два – легко диссоциируют (HS-KoA и НАД).
Все эти ферменты, имеющие субъединичное строение, и коферменты организованы в единый комплекс. Поэтому промежуточные продукты способны быстро взаимодействовать друг с другом. Показано, что составляющие комплекс полипептидные цепи субъединиц дигидролипоилацетилтрансферазы составляют как бы ядро комплекса, вокруг которого расположены пируватдегидрогеназа и дигидролипоилдегидрогеназа. Принято считать, что нативный ферментный комплекс образуется путем самосборки. Суммарную реакцию, катализируемую пируватдегидрогеназным комплексом, можно представить следующим образом:
Пируват + НАД+ + HS-KoA –> Ацетил-КоА + НАДН + Н+ + СO2.
Реакция сопровождается значительным уменьшением стандартной свободной энергии и практически необратима. Образовавшийся в процессе окислительного декарбоксилирования ацетил-КоА подвергается дальнейшему окислению с образованием СО2 и Н2О. Полное окисление ацетил-КоА происходит в цикле трикарбоновых кислот (цикл Кребса). Этот процесс, так же как окислительное декарбоксилирование пирувата, происходит в митохондриях клеток.
· Наследственные нарушения обмена моносахаридов и дисахаридов : галактоземия, непереносимость дисахаридов.
Одно из патологических состояний, возникающих в результате нарушения обмена углеводов,– это рецессивно наследуемое заболевание галактоземия. При этом заболевании общее содержание моносахаридов в крови повышается главным образом за счет уровня галактозы, достигая 11,1–16,6 ммоль/л. Концентрация глюкозы в крови существенно не изменяется. Кроме галактозы, в крови накапливается также галактозо-1-фосфат. Галактоземия приводит к умственной отсталости и катаракте хрусталика. Возникновение данной болезни у новорожденных связано с недостатком фермента гексозо-1-фосфатуридилилтрансферазы. С возрастом наблюдается ослабление этого специфического нарушения обмена углеводов. Непереносимость дисахаридов -наследственная или приобретённая недостаточность активности дисахаридаз, обусловливающая нарушения расщепления и всасывание дисахаридов; вызывает непереносимость лактозы, сахарозы и/или мальтозы; проявляется расстройствами пищеварения и питания в виде хронической ферментативной диспепсии.
· Биологические функции липидов, переваривание и всасывание.
Расщепление триглицеридов в пищеварительном тракте. Слюна не содержит расщепляющих жиры ферментов. Следовательно, в полости рта жиры не подвергаются никаким изменениям. У взрослых людей жиры проходят через желудок также без особых изменений. В желудочном соке содержится
липаза, получившая название желудочной, однако роль ее в гидролизепищевых триглицеридов у взрослых людей невелика. Во-первых, в желудочном соке взрослого человеа и других млекопитающих содержание липазы крайне низкое. Во-вторых, рН желудочного сока далек от оптимума действия этого фермента. В-третьих, в желудке отсутствуют условия для эмульгирования триглицеридов, а липаза может активно действовать только на триглицериды, находящиеся в форме эмульсии. Поэтому у взрослых неэмульгированные триглицериды, составляющие основную массу пищевого жира, проходят через желудок без особых изменений. Вместе с тем расщепление триглицеридов в желудке играет важную роль в пищеварении у детей, особенно грудного возраста. Расщепление триглицеридов в желудке взрослого человека невелико, но оно в определенной степени облегчает последующее переваривание их в кишечнике. Даже незначительное по объему расщепление триглицеридов в желудке приводит к появлению свободных жирных кислот, которые, не подвергаясь всасыванию в желудке, поступают в кишечник и способствуют там эмульгированию жиров, облегчая таким образом воздействие на них липазы панкреатического сока. Считают, что только комбинация соль желчной кислоты + ненасыщенная жирная кислота + моноглицерид придает необходимую степень эмульгирования жира. Соли желчных кислот резко уменьшают поверхностное натяжение на поверхности раздела жир/вода, благодаря чему они не только
облегчают эмульгирование, но и стабилизируют уже образовавшуюся эмульсию.
Всасывание триглицеридов и продуктов их расщепления. Всасывание происходит в проксимальной части тонкой кишки. Тонкоэмульгированные жиры (величина жировых капель эмульсии не должна превышать 0,5 мкм) частично могут всасываться через стенки кишечника без предварительного гидролиза. Основная часть жира всасывается лишь после расщепления его панкреатической липазой на жирные кислоты, моноглицериды и глицерин.
Биологическая роль липидов
- Энергетическая - при сгорании 1 гр жира выделяется 39кДж, причем, это самый энергоемкий источник энергии, особенно для спортсменов, тренирующих выносливость. Кроме того, энергия, полученная при окислении жиров, используется не только во время работы, но и обеспечивает восстановительные процессы во время отдыха.
- Теплоизоляционная (у полярных животных и растений)
- Защитная (амортизационная) - жиры предохраняют внутренние органы от механических повреждений и фиксируют их.
- Строительная - жиры выполняют роль структурного компонента мембран; особенно богата ими нервная ткань.
- Гормональная - выполняют регуляторную функцию, являясь основой стероидных гормонов. Кроме того, жиры являются растворителями многих неполярных соединений.
По содержанию в организме все жиры можно разделить на две большие группы : резервный жир и протоплазматический.
Резервный жир Находится в подкожно-жировой клетчатке, брызжейке, сальнике, капсуле почек и других внутренних органов. Жировая (адипозная) ткань выполняет функцию депо, т.е. поглощает липиды из крови и высвобождает их при необходимости (при повышении энергозатрат). Клетки, содержащие жиры называются адипоциты. Они имеют сферическую форму, большую часть их заполняет липидная капля. Состав резервного жира может меняться в широких пределах в зависимости от характера питания, функционального состояния, физической активности. В норме он составляет 10-15% от веса тела, при ожирении - 30% и более.
Протоплазматический жир Входит в состав плазматических мембран, (особенно много его содержится в мембранах нервных клеток), является основой гормонов стероидной природы. Его процентное содержание и соотношение между различными липидными фракциями очень устойчиво, постоянно, жестко регулируется и не изменяется даже при голодании.
· Биосинтез нейтральных жиров
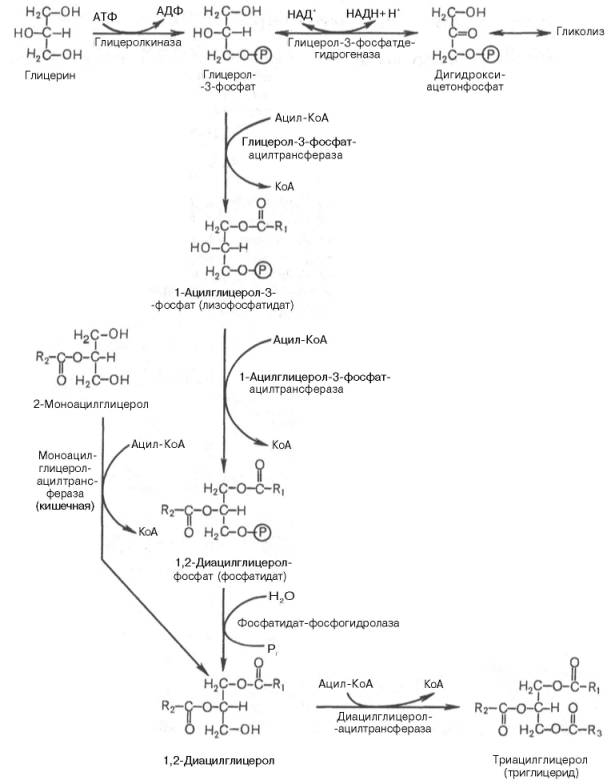
Синтез триглицеридов происходит из глицерина и жирных кислот(главным образом стеариновой, пальмитиновой и олеиновой). Путь биосинтеза триглицеридов в тканях протекает через образование α-глицерофосфата (глицерол-3-фосфата) как промежуточного соединения.
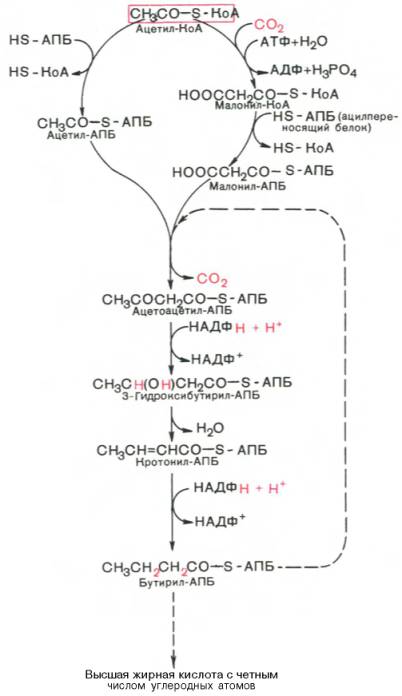
· Биосинтез жирных кислот (схема)
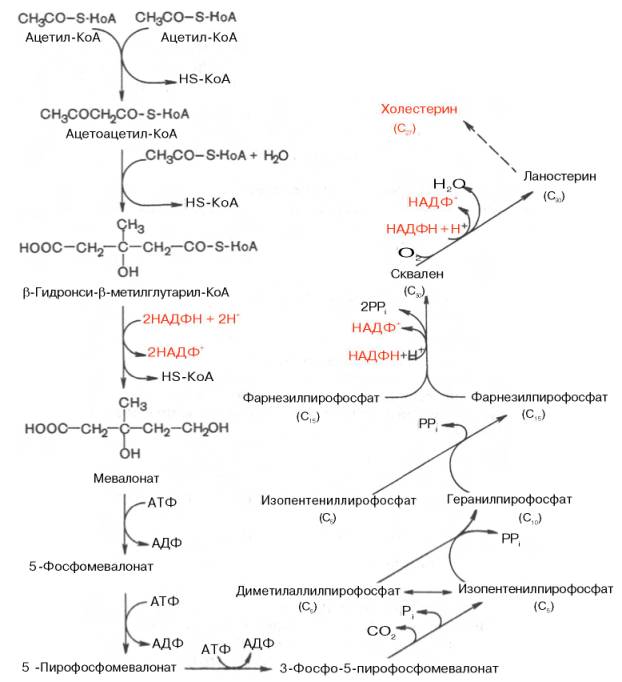
· Синтез холестерина
Холестерин в составе клеточной плазматической мембраны играет роль модификатора бислоя, придавая ему определённую жёсткость за счёт увеличения плотности «упаковки» молекул фосфолипидов. Таким образом, холестерин — стабилизатор текучести плазматической мембраны.
Холестерин открывает цепь биосинтеза стероидных половых гормонов и кортикостероидов, служит основой для образования жёлчных кислот и витаминов группы D, участвует в регулировании проницаемости клеток и предохраняет эритроциты крови от действия гемолитических ядов
· Гормоны гипофиза. Вазопрессин и окситоцин. Строение и биологическая функция этих гормонов.
Гормоны вазопрессин и окситоцин синтезируются рибосомальным путем,причем одновременно в гипоталамусе синтезируются 3 белка: нейрофизин I, II и III, функция которых заключается в нековалентном связывании окситоцина и вазопрессина и транспорте этих гормонов в нейросекреторные гранулы гипоталамуса. Далее в виде комплексов нейрофизин–гормон они мигрируют вдоль аксона и достигают задней доли гипофиза, гдеоткладываются про запас; после диссоциации комплекса свободный гормон
секретируется в кровь. Нейрофизины также выделены в чистом виде,и выяснена первичная структура двух из них (92 из 97 аминокислотных остатков соответственно); это богатые цистеином белки, содержащие по
семь дисульфидных связей. Оба гормона представляют собой нонапептиды следующего строени
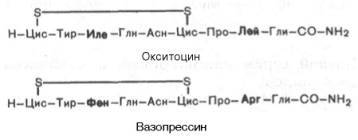
Основной биологический эффект окситоцина у млекопитающих связансо стимуляцией сокращения гладких мышц матки при родах и мышечныхволокон вокруг альвеол молочных желез, что вызывает секрецию молока.Вазопрессин стимулирует сокращение гладких мышечных волокон сосудов,оказывая сильное вазопрессорное действие, однако основная роль егов организме сводится к регуляции водного обмена, откуда его второеназвание антидиуретического гормона. В небольших концентрациях (0,2 нг на 1 кг массы тела) вазопрессин оказывает мощное антидиуретическоедействие – стимулирует обратный ток воды через мембраны почечныхканальцев. В норме он контролирует осмотическое давление плазмы кровии водный баланс организма человека. При патологии, в частности атрофиизадней доли гипофиза, развивается несахарный диабет – заболевание,характеризующееся выделением чрезвычайно больших количеств жидкости
с мочой. При этом нарушен обратный процесс всасывания воды в канальцах почек.
· Гормоны надпочечников. Гормон мозгового вещества надпочечников. Их влияние на обмен углеводов в организме человека.
Надпочечники состоят из двух индивидуальных в морфологическом и функциональном отношениях частей – мозгового и коркового вещества. Мозговое вещество относится к хромаффинной, или адреналовой, системе и вырабатывает гормоны, которые по приведенной ранее классификации считаются производными аминокислот. Корковое вещество состоит из эпителиальной ткани и секретирует гормоны стероидной природы.
Адреналин норадреналин Изопропиладреналин
предшественником гормонов мозгового вещества надпочечников является тирозин, подвергающийся в процессе обмена реакциям гидроксилирования,декарбоксилирования и метилирования с участием соответствующих ферментов.
Адреналин и норадреналин,относятся к катехоламинам, т.е. к классу органических веществ, оказывающих сильное биологическое действие. Кроме того, все они оказывают мощное сосудосуживающее действие, вызывая повышение артериального давления, и в этом отношении действие их сходно с действием симпатической нервной системы. Известно мощное регулирующее влияние этих гормонов на обмен углеводов в организме. Так, в частности, адреналин вызывает резкое повышение уровня глюкозы в крови, что обусловлено ускорением распада гликогена в печени под действием фермента фосфорилазы. Гипергликемическйй эффект норадреналина значительно ниже – примерно 5% от действия адреналина. Параллельно отмечаются накопление гексозофосфатов в тканях, в частности в мышцах, уменьшение концентрации неорганического фосфата и повышение уровня ненасыщенных жирных кислот в плазме крови. Имеются данные о торможении окисления глюкозы в тканях под влиянием адреналина.
· Гормоны поджелудочной железы. Инсулин, образование из проинсулина. Влияние инсулина на углеводный обмен.
Поджелудочная железа относится к железам со смешанной секрецией. Внешнесекреторная функция ее заключается в синтезе ряда ключевых ферментов пищеварения, в частности амилазы, липазы, трипсина, химотрипсина, карбоксипептидазы и др., поступающих в кишечник с соком поджелудочной железы.
биосинтез инсулина осуществляется в β-клетках панкреатических островков из своего предшественника проинсулина. Проинсулин представлен одной полипептидной цепью, содержащей 84 аминокислотных остатка; он лишен биологической, т.е. гормональной, активности. Местом синтеза проинсулина считается фракция микросом β-клеток панкреатических островков; превращение неактивного проинсулина в активный инсулин (наиболее существенная часть синтеза) происходит при перемещении проинсулина от рибосом к секреторным гранулам путем частичного протеолиза (отщепление с С-конца полипептидной цепи пептида, содержащего 33 аминокислотных остатка и получившего наименование соединяющего пептида, или С-пептида). Синтезированный из проинсулина инсулин может существовать в нескольких формах, различающихся по биологическим, иммунологическим и физико-химическим свойствам. Различают две формы инсулина: 1) свободную, вступающую во взаимодействие с антителами, полученными к кристаллическому инсулину, и стимулирующую усвоение глюкозы мышечной и жировой тканями; 2) связанную, не реагирующую с антителами и активную только в отношении жировой ткани.
При недостаточной секреции (точнее, недостаточном синтезе) инсулина развивается специфическое заболевание – сахарный диабет. Помимо клинически выявляемых симптомов (полиурия, полидипсия и полифагия), сахарный диабет характеризуется рядом специфических нарушений процессов обмена. Так, у больных развиваются гипергликемия (увеличение уровня глюкозы в крови) и гликозурия (выделение глюкозы с мочой,в которой в норме она отсутствует). К расстройствам обмена относят также усиленный распад гликогена в печени и мышцах, замедление биосинтеза белков и жиров, снижение скорости окисления глюкозы в тканях, развитие отрицательного азотистого баланса, увеличение содержания холестерина и других липидов в крови. При диабете усиливаются мобилизация жиров из депо, синтез углеводов из аминокислот (глюконеогенез) и избыточный синтез кетоновых тел (кетонурия). После введения больным инсулина все перечисленные нарушения, как правило, исчезают, однако действие гормона ограничено во времени, поэтому необходимо вводить его постоянно.
· Гормоны щитовидной железы. Биологическое действие гормонов щитовидной железы.
Щитовидная железа играет исключительно важную роль в обмене веществ. Об этом свидетельствуют резкое изменение основного обмена, наблюдаемое при нарушениях деятельности щитовидной железы, а также ряд косвенных данных, в частности обильное ее кровоснабжение несмотря на небольшую массу (20–30 г). Щитовидная железа состоит из множества особых полостей – фолликулов, заполненных вязким секретом – коллоидом. В состав коллоида входит особый йодсодержащий гликопротеин с высокой
мол. Массой. Этот гликопротеин получил название йодтиреоглобулина. Он представляет собой
запасную форму тироксина и трийодтиронина – основных гормонов фолликулярной части щитовидной железы. Помимо этих гормонов, в особых клетках – так называемых парафолликулярных клетках, или С-клетках щитовидной железы, синтезируется гормон пептидной природы, обеспечивающий постоянную концентрацию кальция в крови. Он получил название «кальцитонин». Биологическое действие гормонов щитовидной железы распространяется на множество физиологических функций организма. В частности, гормоны регулируют скорость основного обмена, рост и дифференцировку тканей, обмен белков, углеводов и липидов, водно-электролитный обмен, деятельность ЦНС, пищеварительного тракта, гемопоэз, функцию сердечно-сосудистой системы, потребность в витаминах, сопротивляемость организма инфекциям и др. Гипофункция щитовидной железы в раннем детском возрасте приводит к развитию болезни - кретинизм. Помимо остановки роста, специфических изменений кожи, волос, мышц, резкого
снижения скорости процессов обмена, при кретинизме отмечаются глубокие нарушения психики; специфическое гормональное лечение в этом случае не дает положительных результатов.
Недостаточная функция щитовидной железы в зрелом возрасте сопровождается развитием гипотиреоидного отека, или микседемыЭто заболевание чаще встречается у женщин и характеризуется нарушением водно-солевого, основного и жирового обмена.У больных отмечаются слизистый отек, патологическое ожирение, резкое снижение основного обмена, выпадение волос и зубов, общие мозговые нарушения и психические расстройства. Кожа становится сухой, температура тела снижается; в крови повышено содержание глюкозы. Повышенная функция щитовидной железы (гиперфункция) вызывает развитие гипертиреоза, известного в литературе под названием «зоб диффузный токсический» (болезнь Грейвса, или базедова болезнь). Резкое повышение обмена веществ сопровождается усиленным распадом тканевых белков, что приводит к развитию отрицательного азотистого баланса. Наиболее характерным проявлением болезни считается триада симптомов: резкое увеличение числа сердечных сокращений (тахикардия), пучеглазие (экзофтальм) и зоб, т.е. увеличенная в размерах щитовидная железа;
у больных отмечаются общее истощение организма, а также психические расстройства.
Биомембраны и биоэнергетика
1. Состав и строение биологических мембран. Основные функции биомембран.
Состав биологических мембран зависит от их типа и функций, однако основными составляющими являются липиды ибелки, а также углеводы (небольшая, но чрезвычайно важная часть) и вода (более 20% общего веса).
Липиды. В составе биологических мембран обнаружены липиды трех классов: фосфолипиды, гликолипиды и стероиды. В мембранах животных клеток более 50% всех липидов составляют фосфолипиды — глицерофосфолипиды (фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, фосфатидилинозит) и сфингофосфолипиды (производные церамида, сфингомиелин). Гликолипиды представлены цереброзидами, сульфатидами и ганглиозидами, а стероиды — в основном холестерином (около 30%). В липидных компонентах биологических мембран содержатся разнообразные жирные кислоты, однако в мембранах животных клеток преобладают пальмитиновая, олеиновая и стеариновая кислоты. Основную структурную роль в биологических мембранах играют фосфолипиды. Они обладают выраженной способностью формировать двухслойные структуры (бислои) при смешивании с водой, что обусловлено химической структурой фосфолипидов, молекулы которых состоят из гидрофильной части — «головки» (остаток фосфорной кислоты и присоединенная к нему полярная группа, например холин) и гидрофобной части — «хвоста» (как правило, две жирно-кислотные цепи). В водной среде фосфолипиды бислоя расположены таким образом, что жирно-кислотные остатки обращены внутрь бислоя и, следовательно, изолированы от окружающей среды, а гидрофильные «головки» —наоборот, наружу. Липидный бислои представляет собой динамичную структуру: образующие его липиды могут вращаться, двигаться в латеральном направлении и даже переходить из слоя в слой (флип-флоп переход). Такое строение липидного бислоя легло в основу современных представлений о структуре биологических мембран и определяет некоторые важные свойства биологических мембран , например способность служить барьером и не пропускать молекулы веществ, растворенных в воде (рис.). Нарушение структуры бислоя может привести к нарушению барьерной функции мембран.
Холестерин в составе биологических мембран играет роль модификатора бислоя, придавая ему определенную жесткость за счет увеличения плотности «упаковки» молекул фосфолипидов.
Гликолипиды несут разнообразные функции: отвечают за рецепцию некоторых биологически активных веществ, участвуют в дифференцировке ткани, определяют видовую специфичность.
Белки биологических мембран исключительно разнообразны. Молекулярная масса их в большинстве своем составляет 25 000 — 230 000.Белки могут взаимодействовать с липидным бислоем за счет электростатических и (или) межмолекулярных сил. Они сравнительно легко могут быть удалены из мембраны. К такому типу белков относят цитохром с (молекулярная масса около 13 000), обнаруживаемый на наружной поверхности внутренней мембраны митохондрий.Эти белки называются периферическими, или наружными. Для других белков, получивших название интегральных, или внутренних, характерно то, что одна или несколько полипептидных цепей оказываются погруженными в бислои или пересекают его, иногда не один раз (например, гликофорин, транспортные АТФ-азы, бактериородопсин). Часть белка, контактирующая с гидрофобной частью липидного бислоя, имеет спиральное строение и состоит из неполярных аминокислот, в силу чего между этими компонентами белков и липидов происходит гидрофобное взаимодействие. Полярные группы гидрофильных аминокислот непосредственно взаимодействуют с примембранными слоями, как с одной, так и с другой стороны бислоя. Молекулы белков, как и молекулы липидов, находятся в динамическом состоянии, для них также характерна вращательная, латеральная и вертикальная подвижность. Она является отражением не только их собственной структуры, но и функциональной активности. что в значительной степени определяется вязкостью липидного бислоя, которая, в свою очередь, зависит от состава липидов, относительного содержания и вида ненасыщенных жирно-кислотных цепей. Этим объясняется узкий температурный диапазон функциональной активности мембраносвязанных белков.Белки мембран выполняют три основные функции: каталитическую (ферменты), рецепторную и структурную. Однако такое разграничение достаточно условно, и в ряде случаев один и тот же белок может выполнять и репепторную и ферментную функции (например, инсулин).Число мембранных ферментов в клетке достаточно велико, однако их распределение в различных типах биологических мембран неодинаково. Некоторые ферменты (маркерные) присутствуют только в мембранах определенного типа (например, Na, К-АТФ-аза, 5-нуклеотидаза, аденилатциклаза — в плазматической мембране; цитохром Р-450, НАДФН-дегидрогеназа, цитохром в5 — в мембранах эндоплазматического ретикулума; моноаминоксидаза — в наружной мембране митохондрий, а цитохром С-оксидаза, сукцинат-дегидрогеназа — во внутренней; кислая фосфатаза — в мембране лизосом)Рецепторные белки, специфически связывая низкомолекулярные вещества (многие гормоны, медиаторы), обратимо меняют свою форму. Эти изменения запускают внутри клетки ответные химические реакции. Таким способом клетка принимает различные сигналы, поступающие из внешней среды К структурным белкам относят белки цитоскелета, прилегающие к цитоплазматической стороне клеточной мембраны. В комплексе с микротрубочками и микрофиламентами цитоскелета они обеспечивают противодействие клетки изменению ее объема и создают эластичность. В эту же группу включают ряд мембранных белков, функции которых не установлены.Углеводы в биологических мембранах находятся в соединении с белками (гликопротеины) и липидами (гликолипиды). Углеводные цепи белков представляют собой олиго- или полисахаридные структуры, в состав которых входят глюкоза, галактоза, нейраминовая кислота, фукоза и манноза. Углеводные компоненты биологических мембран открываются в основном во внеклеточную среду, образуя на поверхности клеточных мембран множество ветвистых образований, являющихся фрагментами гликолипидов или гликопротеидов. Их функции связаны с контролем за межклеточным взаимодействием, поддержанием иммунного статуса клетки, обеспечением стабильности белковых молекул в биологических мембранах . Многие рецепторные белки содержат углеводные компоненты. Примером могут служить антигенные детерминанты групп крови, представленные гликолипидами и гликопротеинами.
Функции биологических мембран. Барьерная функция. Для клеток и субклеточных частиц биологических мембран служат механическим барьером, отделяющим их от внешнего пространства. Функционирование клетки часто сопряжено с наличием значительных механических градиентов на ее поверхности преимущественно вследствие осмотического и гидростатического давления. Основную нагрузку в этом случае несет клеточная стенка, главными структурными элементами которой у высших растений являются целлюлоза, пектин и экстепин, а у бактерий — муреин (сложный полисахарид-пептид). В клетках животных необходимость в жесткой оболочке отсутствует. Некоторую жесткость этим клеткам придают особые белковые структуры цитоплазмы, примыкающие к внутренней поверхности плазматической мембраны.Перенос веществ через биологические мембраны сопряжен с такими важнейшими биологическими явлениями, как внутриклеточный гомеостаз ионов, биоэлектрические потенциалы, возбуждение и проведение нервного импульса, запасание и трансформация энергии и т.п. (). Различают пассивный и активный транспорт (перенос) нейтральных молекул, воды и ионов через биологические мембраны . Пассивный транспорт не связан с затратами энергии, он осуществляется путем диффузии по концентрационным, электрическим или гидростатическим градиентам. Активный транспорт осуществляется против градиентов, связан с затратой энергии (преимущественно энергии гидролиза АТФ) и сопряжен с работой специализированных мембранных систем (мембранных насосов). Различают несколько видов транспорта. Если вещество транспортируется через мембрану независимо от наличия и переноса других соединений, то такой вид транспорта называют юнипортом. Если перенос одного вещества сопряжен с транспортом другого, то говорят о котранспорте, причем однонаправленный перенос называется симпортом, а противоположно направленный — антипортом. В особую группу выделяют перенос веществ путем экзо- и пиноцитоза. Пассивный перенос может осуществляться путем простой диффузии через липидный бислои мембраны, а также через специализированные образования — каналы. Путем диффузии через мембрану проникают в клетку незаряженные молекулы, хорошо растворимые в липидах, в т.ч. многие яды и лекарственные средства, а также кислород и углекислый газ. Каналы представляют собой липопротеиновые структуры, пронизывающие мембраны. Они служат для переноса определенных ионов и могут находиться в открытом или закрытом состоянии. Проводимость канала зависит от мембранного потенциала, что играет важную роль в механизме генерации и проведения нервного импульса.В ряде случаев перенос вещества совпадает с направлением градиента, но существенно превосходит по скорости простую диффузию. Этот процесс называют облегченной диффузией; он происходит с участием белков-переносчиков. Процесс облегченной диффузии не нуждается в энергии. Этим способом транспортируются сахара, аминокислоты, азотистые основания. Такой процесс происходит, например, при всасывании сахаров из просвета кишечника клетками эпителия.Перенос молекул и ионов против электрохимического градиента (активный транспорт) связан со значительными затратами энергии. Часто градиенты достигают больших величин. например, концентрационный градиент водородных ионов на плазматической мембране клеток слизистой оболочки желудка составляет 106, градиент концентрации ионов кальция на мембране саркоплазматического ретикулума — 104, при этом потоки ионов против градиента значительны. В результате затраты энергии на транспортные процессы достигают, например, у человека, более 1/3 всей энергии метаболизма. В плазматических мембранах клеток различных органов обнаружены системы активного транспорта ионов натрия и калия — натриевый насос. Эта система перекачивает натрий из клетки и калий в клетку (антипорт) против их электрохимических градиентов. Перенос ионов осуществляется основным компонентом натриевого насоса — Na+, К+-зависимой АТФ-азой за счет гидролиза АТФ. На каждую гидролизующуюся молекулу АТФ транспортируется три иона натрия и два иона калия. Существуют два типа Са2+-АТФ-аз. Одна из них обеспечивает выброс ионов кальция из клетки в межклеточную среду, другая — аккумуляцию кальция из клеточного содержимого во внутриклеточное депо. Обе системы способны создавать значительный градиент иона кальция. К+, Н+-АТФ-аза обнаружена в слизистой оболочке желудка и кишечника. Она способна транспортировать Н+ через мембрану везикул слизистой оболочки при гидролизе АТФ. В микросомах слизистой оболочки желудка лягушки найдена аниончувствительная АТФ-аза, способная при гидролизе АТФ осуществлять антипорт бикарбоната и хлорида.Изложенные механизмы транспорта различных веществ через клеточные мембраны имеют место и в случае их транспорта через эпителий ряда органов (кишечника, почек, легких), который осуществляется через слой клеток (монослой в кишечнике и нефронах), а не через единичную клеточную мембрану. Такой транспорт называют трансцеллюлярным, или трансэпителиальным. Характерной особенностью клеток, например эпителиоцитов кишечника и канальцев нефронов, является то, что апикальная и базальная их мембраны различаются по проницаемости, величине мембранного потенциала и транспортной функции.Способность генерировать биоэлектрические потенциалы и проводить возбуждение. Возникновение биоэлектрических потенциалов связано с особенностями строения биологических мембран и с деятельностью их транспортных систем, создающих неравномерное распределение ионов по обе стороны мембраны). Процессы трансформации и запасания энергии протекают в специализированных биологических мембранах и занимают центральное место в энергетическом обеспечении живых систем. Два основных процесса энергообразования — фотосинтез и тканевое дыхание — локализованы в мембранах внутриклеточных органелл высших организмов, а у бактерий — в клеточной (плазматической) мембране Фотосинтезирующие мембраны преобразуют энергию света в энергию химических соединений, запасая ее в форме сахаров — основного химического источника энергии для гетеротрофных организмов. При дыхании энергия органических субстратов освобождается в процессе переноса электронов по цепи окислительно-восстановительных переносчиков и утилизируется в процессе фосфорилирования АДФ неорганическим фосфатом с образованием АТФ. Мембраны, осуществляющие фосфорилирование, сопряженное с дыханием, называют сопрягающими (внутренние мембраны митохондрий, клеточные мембраны некоторых аэробных бактерий, мембраны хроматофоров фотосинтезирующих бактерий).Метаболические функции мембран определяются двумя факторами: во-первых, связью большого числа ферментов и ферментативных систем с мембранами, во-вторых, способностью мембран физически разделять клетку на отдельные отсеки, отграничивая друг от друга метаболические процессы, протекающие в них. Метаболические системы не остаются при этом полностью изолированными. В мембранах, разделяющих клетку, имеются специальные системы, обеспечивающие избирательное поступление субстратов, выделение продуктов, а также движение соединений, обладающих регуляторным действием.Клеточная рецепция и межклеточные взаимодействия. Под этой формулировкой объединен весьма обширный и разнообразный набор важных функций клеточных мембран, определяющих взаимодействие клетки с окружающей средой и формирование многоклеточного организма как единого целого. Молекулярно-мембранные аспекты клеточной рецепции и межклеточных взаимодействий касаются прежде всего иммунных реакций, гормонального контроля роста и метаболизма, закономерностей эмбрионального развития
2. Цикл трикарбоновых кислот: схема и биологическое значение этого процесса
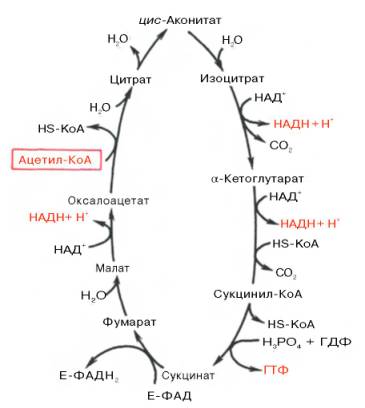
БИОЛОГИЧЕСКАЯ ЦЕННОСТЬ ЦТК
В ЦТК за период одного цикла сгорает 1 молекула ацетил-КоА. При этом образуются три молекулы НАДН2 и одна молекула ФАДН2.
Эти восстановительные эквиваленты передаются в дыхательную цепь, локализованную во внутренней митохондриальной мембране. При прохождении по дыхательной цепи НАДН2 образуются три молекулы АТФ из АДФ. За счет ФАДН2 образуются только две молекулы АТФ ( причину этого мы рассмотрим позже, когда будем разбирать работу дыхательной цепи). Еще один высокоэнергетический фосфат производится на субстратном уровне при превращении сукцинил~КоА в сукцинат. Таким образом, всего за период каждого цикла образуется12молекул АТФ.
Помимо энергетической ценности ЦТК, он является также источником некоторых очень важных метаболитов, которые дают начало новым метаболическим путям: это в первую очередь глюконеогенез, переаминирование и дезаминирование аминокислот, синтез жирных кислот, холестерина.
Жизненно важными являются такие соединения как ЩУК и альфа-кетоглутаровая кислота. Эти соединения используются в качестве предшественников таких важнейших молекул клетки, как, например, аминокислоты. Вспомним, что весь ЦТК происходит в Мх. Митохондриальная мембрана непроницаема для ЩУК и альфа-КГ, поэтому сначала из Мх в цитоплазму выводятся малат и изоцитр
