Функционирование ферментов дыхательной цепи
Окислительное фосфорилирование
ПДГ сбрасывает 2 атома Н∙ с НАД∙Н2 на І акцептор ДЦ - НАД∙Н2-дегидрогеназу. Которая в структуре своей содержит ФМН.
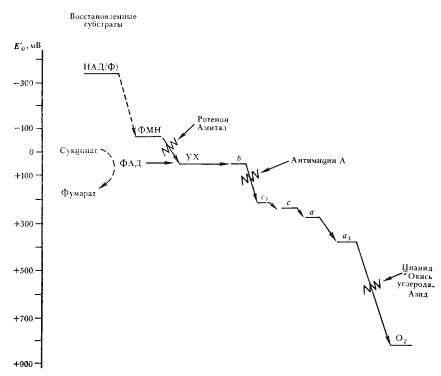 |
| Схема переноса электронов в дыхательной цепи митохондрий: ФМН — простетическая группа НАД(Ф)-H2 — дегидрогеназы; ФАД — простетическая группа сукцинатдегидрогеназы; УХ — убихинон; b, c, с1, а, a3 — цитохромы. Сплошными линиями обозначены процессы, протекающие в мембране; прерывистыми — в цитозоле клетки; зигзагообразной линией показаны места действия ингибиторов |
НАД∙Н2-дегидрогеназа переносит водород на FeS-белок. Но FeS-белок может быть восстановлен электроном, поэтому на уровне НАД∙Н2-дегидрогеназы функционирует первая водородная помпа, которая приводит к разделению водорода на 2 восстановительных эквивалента на Н+ и электрон. Н+ переносится на внешнюю сторону мембраны, а электрон восстанавливает FeS-белок. Следующими по цепочке являются хиноны, переносящиеся или восстанавливающиеся водородом, поэтому на внешней стороне мембраны происходит объединение восстановленных эквивалентов (электрона и протона – получаем атомарный водород), что и восстанавливает хинон. С хинонов восстановленный эквивалент передаётся на цитохром в, переносящий электроны, поэтому на уровне хинона функционирует вторая водородная помпа, которая приводит к выбросу Н+ на внешнюю поверхность мембраны и энергизацию мембраны. Восстановленный электроном цитохром в переносит электрона на гипотетический переносчик Z, природа которого
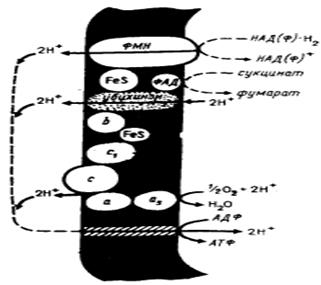 |
| Топография компонентов дыхательной цепи митохондрий: ФМН — простетическая группа НАД(Ф)-H2-дегидрогеназы; ФАД — простетическая группа сукцинатдегидрогеназы; FeS — железхеросолержащий белок; b, c1, c, a, a3 — цитохромы. |
остается неизвестной, но этот переносчик должен восстанавливать Н2 в атомарной форме, поэтому на внешней стороне мембраны происходит объединение электрона и протона и получается атомарный водород, восстанавливающий гипотетический переносчик Z. С него восстановитель передается на цитохром с, который способен переносить только электроны, поэтому на уровне цитохрома с функционирует треться водородная помпа, которая приводит к выбросу протона на внешнюю сторону мембраны. С цитохрома с электрон поступает на цитохром а, где происходит объединение протона с электроном. Атомарный водород восстанавливает кислород на внутренней части мембраны и образуется либо перекись, либо вода. Таким образом, при сбрасывании 2 водородных атомов с ПДГ в ДЦ функционирование 3 водородных помп приводит к выбросу 6Н+, которые на внешней стороне мембраны обеспечивают ей суммарный положительный заряд. Внутренняя часть мембраны несёт суммарный отрицательный заряд. Согласно теории Митчелла это приводит к генерации мембранного потенциала ∆μН. Как только значение мембранного потенциала достигает 0,2В происходит разрядка или диссипация мембраны и Н+ возвращается внутрь клетки. Возвращение 6Н+ обеспечивает синтез 3 молекул АТФ.
ФДГ (сукцинатдегидрогеназа, которая функционирует в ЦТК) согласно окислительно-восстановительному потенциалу сбрасывает водород на уровне хинона, поэтому миграция 2 атомов водорода (2 электронов) обеспечивает в ДЦ выброс 4 протонов, поскольку на участке от хинона до кислорода функционируют 2 водородных помпы, таким образом, окисление ФАД∙Н2 эквивалентно синтезу 2 молекул АТФ.
АТФазный комплекс
АТФаза является полиферментативным комплексом, который располагается в ЦПМ и является трансмембранным комплексом. Имеет сложное строение, состоит из 2 компонентов: F0 и F1.
F0 состоит из 3 белковых субъединиц а, в, с и обеспечивает трансмембранный канал. Через который возвращается протон на внутреннюю сторону мембраны. F1 – каталитический центр фермента, состоит из 5 субъединиц α, β, γ, δ, ε. Согласно первой гипотезе, энергия мембранного потенциала затрачивается на присоединение фосфата к АДФ. Согласно второй гипотезе, образование АТФ происходит без затрат энергии, а энергия мембранного потенциала расходуется на перенос АДФ и фосфата в каталитический центр F1.
АДФ3+ + РО43-+2Н+→АТФ+Н2О
АТФазный комплекс обладает двойственной функцией: наряду с АТФ-синтетазной активностью этот комплекс может работать как АТФ-гидролаза: она расщепляет АТФ с образованием АДФ, фосфата, что сопровождается распадом Н2О и 2 протона перебрасываются на внешнюю сторону мембраны.
Таким образом, АТФ-гидролаза работает в качестве 4 водородной помпы в системе ЦПМ.
Амонификаторыв качестве субстрата используют белки или аминокислоты. Белки как полимерные молекулы вне клетки расщепляются на пептиды протеолитическими ферментами, которые внутри клетки расщепляются в дальнеёшем до аминокислот. Далее превращение возможно по двум направлениям: с одной стороныв конструктивном метаболизме аминокислоты включаются в структуру белков; с другой стороны аминокислоты служат основным материалом как источник энергии. В этом случае аминокислоты подвергаются дезаминированию и азот выделяется в виде неорганического восстановителя – аммиака, при этом часть аминокислот после дезаминирования (аланин, аспаргин, глутаминовая кислота) образуют α-кетокислоты (пировиноградная, α-кетоглутаровая, ЩУК), которые включаются в соответствующие участки ЦТК, но большинство аминокислот подвергается превращениям с образованием соединений, которые включают гликолиз или альтернативные ему механизмы, либо на уровне второго этапа аэробного дыхания (образуется Ацетил-КоА). Например, распад L-лейцина приводит к образованию Ацетил-КоА – исходного субстрата ЦТК.
Амонифицирующие микроорганизмы помимо белков могут катаболизировать сахара и органические кислоты, которые они предпоситают белкам. Амонификаторов, облигатно использующих белки, немного, в основном это Г+ спороорбразующие палочки р. Bacillus.
Целлюлозные бактерии используют в качестве субстрата целлюлозу – вещество полисахаридной природы, имеют целый комплекс целлюлолитических ферментов, которые позволяют расщепить целлюлозу до глюкозы, а она включается в основной метаболизм. К разложению целлюлозы способны большая группа Прокариот – Актиномицеты. Они имеют мощный комплекс целлюлолитических ферментов.
Анаэробное дыхание
У микроорганизмов очень пластичный метаболизм. Анаэробное дыхание – это процесс, при котором конечным акцептором электроном являетсяне кислород, а другой органический или неорганический субстрат. Неполное окисление – еще один механизм – разновидность аэробного дыхания, но продукты сами по себе богаты энергией, поэтому энергетический выход неполного окисления меньше, чем при аэробном дыхании.
Анаэробное дыхание. В процессе биохимической эволюции возник такой тип метаболизма, который позволил микроорганизмам переносить электрон в дыхательной цепи в безкислородных условиях. В результате такого безкислородного процесса обеспечивался синтез АТФ по механизму окислительного фосфорилирования. Безусловно, что такое анаэробное дыхание позволяло извлекать энергии в гораздо большем объеме , чем при брожении. У анаэробно дышащих микроорганизмов существует ДЦ и ЦТК. В зависимости от природы конечного акцептора ДЦ различают следующие виды:
| Энергетический процесс | Конечный акцептор электронов | Продукты восстановления |
| Нитратное дыхание и денитрификация | NO3–, NO2– | NO2–, NO, N2O, N2 |
| Сульфатное и серное дыхание | SO42–, S0 | H2S |
| Карбонатное дыхание | CO2 | ацетат |
| Фумаратное дыхание | Фумарат | сукцинат |
К анаэробному дыханию способны не только облигатные анаэробы, но и факультативные микроорганизмы, которые в аэробной среде осуществляют аэробное дыхание, а в анаэробной среде – анаэробное. Так в анаэробной среде у таких микроорганизмов в отсутствии кислорода происходит изменение направления восстановительных эквивалентов (протона, электона и атомарного водорода) с кислородом на из перечисленных акцепторов, так например, микроорганизмы, которые осуществляют нитратное дыхание имеют разветвление дыхательной цепи на уровне цитохрома в:
НАД→ФАД+Q→цитохром в→с →а →О2
 нитроредуктаза
нитроредуктаза
NO3-
Фермент, который перебрасывает электрон (восстановительный эквивалент) на неорганический субстрат – редуктаза.
Нитратное дыхание. При нитратном дыхании 1 из продуктов – нитрит, который накапливается в культуральной жидкости, питьевой воде. Поступление нитритов в организм вызывает заболевание – цианоз. Ионы нитрита связываются с гемоглобином и препятствуют переносу кислорода.
Сульфатное дыхание. Осуществляется сульфатредуцирующими бактериями р. Desulfovibrio и Desulfotomaculum. Эти микроорганизмы – основная группа микроорганизмов, потребляющих Н2S, образуемый в природе и способствуют отложению суьфид минералов в природе. Накопление сероводорода в водоёмах отрицательно влияет на флору и фауну, приводит к их гибели.
Серное дыхание приводит к образованию сероводорода как конечного акцептора дыхательной цепи.
Карбонатное дыхание. Осуществляют архебактерии-метанообразующие. Акцептор электрона – СО2, а окисленный продукт Н2. В качестве супстрата используют навоз и получают биогаз и биоудобрения.
Железное дыхание. Осуществляют почвенные бактерии в анаэробной среде. Соли Fe3+ должны проникнуть внутрь клетки. У этих бактерий есть переносчики – сидерофоры, которые переводят железо в растворимую форму.
Фумаратное дыхание. Осуществляют хемоорганотрофные анаэробные бактурии. Фумарат восстанавливается до сукцината.
Неполное окисление
Неполное окисление – исключительно аэробный процесс, АТФ-окислительное фосфорилирование. Конечные продукты неполностью окислены, то есть сами по себе содержат достаточно большой запас энергии ( фумаровая кислота, уксусная кислота) продукты напоминают брожение. Инода процесс называют окислительное брожение. Все микроорганизмы имеют полноценную дыхательную цепь и конечным акцептором является О2
Усксусно-кислое брожение (неполное окисление). Осуществляют уксусно-кислые бактерии- Г-, неспороорбразующие палочки, подвижные за счет перетрихиально или полярно расположенных жгутиков. Есть неподвижные. Строгие (иногда факультативные) аэробы. Объединены в р.Acetomonas (Gluconobacter), Acetobacter. Все микроорганизмы нуждаются в сложных питательных средах, в определенных витаминах. В качестве исходного энергетическоо продукта используют спирты этиловый, глицерол, глюконовый). Переводят их в уксусную кислоту, глицериновую, глюконовую.
Процесс идёт в две стадии:
СН3 – СН2 – ОН + НАД+→СН3СНО+НАД∙Н2
СН3СНО+НАД+ +Н2О→СН3СООН+НАД∙Н2
Ацетомонас – 6 АТФ из 1 молекулы этилового спирта
Ацетобактер – 18 АТФ
Микроорганизмы рода ацетомонас накапливают уксусную кислоту в культуральной жидкости до тех пор, пока в среде есть спирт, который они окисляют. Как только спирт утилизируется полностью из среды, микроорганизмы используют уксусную кислоту как энергетический субстрат , включая ее в ЦТК, который у этих микроорганизмов функционирует полноценно. Процесс утилизации уксусной кислоты до СО2 и Н2О проходит по типу аэробного дыхания.
