Регуляция цикла Кребса
осуществляется путем влияния на ключевые ферменты: цитратсинтазу (начинает процесс), изоцитратдегидрогеназу (лимитирующий фермент), 2-ок-соглутаратдегидрогеназу (фермент, стоящий на развилке).
Цитратсинтазу активируют оксалоацетат и ацетил-КоА, ингибируют АТФ, НАДН, длинноцепочные ацилы-КоА, сукцинил-КоА.
Изоцитратдегидрогеназа является аллостерическим ферментом. Ее активируют АДФ, Са2+, цАМФ. Ингибируют изоцитратдегидрогеназу АТФ, НАДН, НАДФН.
2-оксоглутаратдегидрогеназуактивируют Са2+ и цАМФ, ингибирует сукцинил-КоА.
Цикл Кребса активируется под влиянием катехоламинов, глюкагона и йодтиронинов.
Значение цикла Кребса:
- катаболическое и энергетическое (цикл Кребса является общим конечным путем распада для метаболитов всех классов соединений; в нем образуется АТФ в результате субстратного фосфорилирования; он является главным поставщиком водорода для дыхательной цепи);
- анаболическое или биосинтетическое Промежуточные метаболиты цикла Кребса используются на синтез других соединений. Например, из оксалоацетата, 2-оксоглутарата и сукцината образуются аминокислоты; из оксалоацетата - глюкоза и другие углеводы; сукцинил-КоА используется на синтез гема;
- регуляторное. Метаболиты - цитрат и АТФ являются регуляторами других процессов. Они активируют синтез жирных кислот и ингибируют гликолиз.
Дыхательная цепь
Дыхательная цепь (цепь переноса электронов) - это цепь сопряженных окислительно-восстановительных реакций, в ходе которых водород, отщепленный от субстратов, переносится на кислород с образованием воды и выделением энергии. Назначение дыхательной цепи - генерирование энергии.
Компоненты дыхательной цепи называются дыхательными переносчиками. Большинство из них (кроме убихинона) являются сложными белками.
Схема дыхательной цепи
Субстраты НАД-зав. Субстраты ФАД-зав.
дегидрогеназ дегидрогеназ
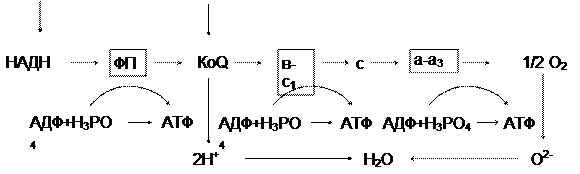
Характеристика дыхательных переносчиков:
НАДН-дегидрогеназа(НАДН-ДГ) (в схеме - ФП) - это флавинзависимый фермент, небелковой частью которого является ФМН и железо-серные центры. НАДН-ДГ встроена во внутреннюю мембрану митохондрий. Она осуществляет перенос водорода с НАДН вначале на ФМН с образованием ФМНН2, затем переносит водород с ФМНН2 на железо-серные центры и только потом на КоQ, при этом последний восстанавливается до КоQН2.
Таким образом, НАДН-ДГ катализирует реакцию:
|
 НАДН2 + КоQ НАД+ + КоQН2
НАДН2 + КоQ НАД+ + КоQН2
КоQ (убихинон)- это небелковый переносчик, растворимый в липидах. Восстановленная форма убихинона (КоQН2) называется убихинол. Убихинон может перемещаться в липидной фазе внутренней мембраны митохондрий, представляя, таким образом, лабильный субстрат для ферментов встроенных в мембрану.
Цитохромы (b, c1, c, a, а3) - это сложные белки, небелковой частью которых является гем, содержащий Fe3+. Принимая электрон, железо трехвалентное переходит в железо двухвалентное, отдавая электрон - переходит опять в трехвалентное.
 Fe3+ + e- Fe2+
Fe3+ + e- Fe2+
 Fe2+ - e- Fe3+
Fe2+ - e- Fe3+
Комплекс цитохромов b-c1 является ферментом (КоQН2 -дегидро-геназой). Он переносит электроны с КоQН2 на цитохром c, при этом железо цитохрома восстанавливается до двухвалентного. Протоны атомов водорода выбрасываются в межмембранное пространство..
Таким образом, осуществляется реакция:
|
 КоQН2 + 2c(Fe3+) KoQ +2Н+ + 2c(Fe2+)
КоQН2 + 2c(Fe3+) KoQ +2Н+ + 2c(Fe2+)
Комплекс цитохромов a-a3 является оксидазой. Он переносит электроны с цитохрома c на кислород, превращая последний в ион (О2-). Цитохромоксидаза катализирует реакцию:
|
 2c(Fe2+) + 1/2 О2 2c(Fe3+) + О2-
2c(Fe2+) + 1/2 О2 2c(Fe3+) + О2-
Ионы кислорода и протоны водорода взаимодействуют с образованием воды.
Перенос электронов по дыхательной цепи происходит по градиенту окислительно-восстановительного потенциала (Ео). Окислительно-восстановительный потенциал характеризует способность сопряженной окислительно-восстановительной пары обратимо отдавать электроны. Чем более отрицательна величина Ео, тем выше способность данной пары отдавать электроны, чем более положительна - тем выше способность принимать электроны. Величина Ео у пары НАДН/НАД+ -0,32в, Ео у пары Н2О/О2- +0,82в, при этом разность между этими величинами составляет 0,82-(-0,32)=1,14в. Этому соответствует разность свободной энергии - 220 кдж на пару переносимых электронов. Этого количества энергии достаточно для синтеза 4 молекул АТФ. Однако в дыхательной цепи синтезируется только 3 АТФ. Синтез АТФ происходит в тех участках дыхательной цепи, где наибольший перепад окислительно-восстановительного потенциала. В этих участках энергии выделяется столько, что ее достаточно для проведения реакции фосфорилирования АДФ.
 АДФ + Н3РО4 АТФ
АДФ + Н3РО4 АТФ
Таким образом, в дыхательной цепи синтез АТФ (фосфорилирование) энергетически сопряжен с переносом электронов, то есть окислением дыхательных переносчиков.
Синтез АТФ, сопряженный с переносом электронов по дыхательной цепи, называется окислительным фосфорилированием.
Участки дыхательной цепи, где есть такой синтез, называют пунктами сопряжения окисления с фосфорилированием.
Пункты сопряжения: между НАДН и КоQ, на участке цитохромов b - c1, и a - a3.
Таким образом, окисление 1 молекулы НАДН приводит к синтезу 3 молекул АТФ, окисление 1 молекулы ФАДН2 - к образованию 2 молекул АТФ.
Для работы цикла Кребса и дыхательной цепи требуются следующие витамины: В1, В2, РР, Q, пантотеновая и липоевая кислоты.
Механизм окислительного фосфорилирования
Компоненты электрон-транспортной цепи (дыхательной цепи) находятся во внутренней мембране митохондрий (непроницаемой для протонов водорода). Они расположены таким образом, что, передавая электроны по цепи, одновременно выталкивают протоны водорода на наружную сторону мембраны в межмембранное пространство. В результате, на наружной стороне мембраны создается избыток протонов водорода (положительный заряд), а с внутренней стороны – недостаток (отрицательный заряд). Это проявляется в возникновении мембранного электрохимического потенциала DmН+, который складывается из разности зарядов на мембране (Dj) и разности рН (снаружи более кислое, внутри – более щелочное). Протоны водорода могут возвращаться в матрикс по протонным каналам, с которыми связана специфическая Н+-АТФаза (АТФ-синтетаза). Обратный ток протонов по каналам в матрикс активирует этот фермент, и он катализирует синтез АТФ из АДФ и Н3РО4. Таким образом, энергия мембранного поценциала преобразуется в энергию макроэргической связи АТФ. АТФ с помощью фермента транслоказы переносится из митохондрий в цитозоль, где и используется.
Сопряжение и разобщение в дыхательной цепи
Сопряжение в дыхательной цепи - это такое состояние, когда окисление (перенос электронов) сопровождается фосфорилированием, то есть синтезом АТФ.
Разобщение - это такое состояние дыхательной цепи, когда окисление идет, а фосфорилирование не происходит, то есть пункты фосфорилирования выключены полностью или частично. В этом случае вся или какая-то часть образующейся энергии выделяется в виде тепла. Сопряженность дыхательной цепи можно оценить по коэффициенту Р/О. Коэффициент Р/О равен числу молей АТФ, образующихся из АДФ и Н3РО4 , на 1 грамм-атом поглощенного кислорода.
Разобщение в дыхательной цепи могут вызывать липофильные вещества, которые способны переносить протоны водорода с внешней стороны внутренней мембраны митохондрий на внутреннюю, минуя АТФ-синтетазу. В результате вся энергия мембранного потенциала будет рассеиваться в виде тепла.
Разобщение вызывают: 2,4-ДНФ (динитрофенол), многие яды промышленных производств, бактериальные токсины, набухание митохондрий, жирные кислоты, ионофоры (вещества, переносящие ионы через мембрану).
Разобщители повышают скорость переноса электронов по дыхательной цепи и выводят ее из под контроля АТФ.
Регуляция дыхательной цепи
1. АДФ стимулирует работу дыхательной цепи. Это явление называется дыхательным контролем.
2. АТФ тормозит работу дыхательной цепи и потребление кислорода.
3. Адреналин и глюкагон активируют работу дыхательной цепи.
Блокаторы дыхательной цепи
1. Ротенон блокирует дыхательную цепь на участке НАДН – КоQ.
2. Амитал, антимицин - на участке между цитохромами b и c1.
3. Цианиды и окись углерода блокируют цитохромоксидазу, при этом вся дыхательная цепь не работает.
Нефосфорилирующее (свободное) окисление
Это окисление без образования АТФ.
Ферменты свободного окисления:оксидазы, оксигеназы, некоторые дегидрогеназы.
Значение свободного окисления:
- терморегуляция;
- Образование биологически важных соединений (катехоламинов, глюкокортикостероидов, коллагена, активация витамина Д и т.д);
- обезвреживание ксенобиотиков (ядов, токсинов, лекарств, веществ бытовой химии).
Тканевые и возрастные особенности окислительных процессов
Анаэробные ткани могут получать энергию без кислорода. Такими тканями являются: скелетные мышцы, эритроциты, периферические нервы, мозговое вещество почек, кость, хрящ, соединительная ткань.
Аэробные ткани получают энергию с использованием кислорода и полностью зависят от кровотока. К таким тканям относятся: головной мозг, сетчатка глаза, сердце, кора почек, печень, слизистая тонкого кишечника.
Потребление кислорода, а значит, и интенсивность окислительных процессов с возрастом падают.
