Остаток фосфорной кислоты
Химический состав живых организмов
Элементный состав
Химический состав живых организмов можно выразить в двух видах — атомном и молекулярном. Атомный (элементный) состав характеризует соотношение атомов элементов, входящих в живые организмы. Молекулярный (вещественный) состав отражает соотношение молекул веществ.
По относительному содержанию элементы, входящие в состав живых организмов, принято делить на три группы:
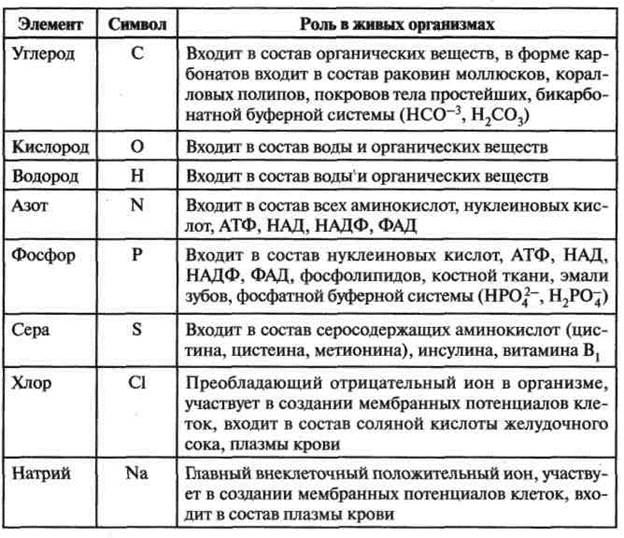
/. Макроэлементы — О, С, Н, N (в сумме около 98—99 %, их еще называют основные); Са, К, Si, Mg, P, S, Na, CI, Fe (в сумме
около 1—2%). Макроэлементы составляют основную массу процентного состава живых организмов.
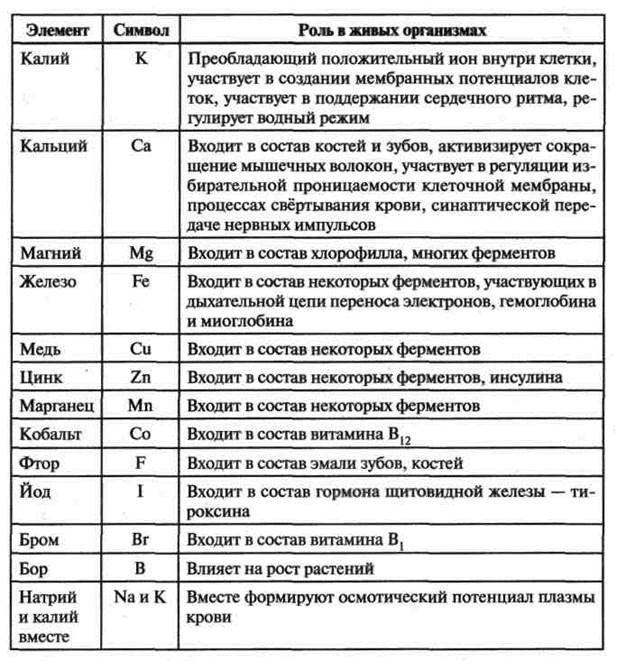
2. Микроэлементы — Mn, Co, Zn, Си, В, I, F и др. Их суммарное содержание в клетке составляет порядка 0,1%.
3. Ультрамикроэлементы — Se, U, Hg, Ra, Au, Ag и др. Их содержание в клетке очень незначительно (менее 0,01 %), а физиологическая роль большинства из них не раскрыта.
Химические элементы, которые входят в состав живых организмов и при этом выполняют биологические функции, называются биогенными. Даже те из них, которые содержатся в клетках в ничтожно малых количествах, ничем не могут быть заменены и совершенно необходимы для жизни
Молекулярный состав
Химические элементы входят в состав клеток в виде ионов и молекул неорганических и органических веществ. Важнейшие неорганические вещества в клетке — вода и минеральные соли, важнейшие органические вещества — углеводы, липиды, белки и нуклеиновые кислоты.
Вода
Вода— преобладающий компонент всех живых организмов. Она обладает уникальными свойствами благодаря особенностям строения: молекулы воды имеют форму диполя и между ними образуются водородные связи. Среднее содержание воды в клетках большинства живых организмов составляет около 70 %. Вода в клетке присутствует в двух формах: свободной (95 % всей воды клетки) и связанной (4—5 % связаны с белками).
Функции воды:
1. Вода — растворитель.
2. Вода — реагент.
3. Транспортная функция.
4. Вода — термостабилизатор и терморегулятор.
5. Структурная функция.

УглеводыУглеводы — органические соединения, состоящие из одной или многих молекул простых Сахаров. Содержание углеводов в животных клетках составляет 1—5 %, а в некоторых клетках растений достигает 70%. Выделяют три группы углеводов: моносахариды (или простые сахара), олигосахариды (состоят из 2—10 молекул простых Сахаров), полисахариды (состоят более чем из 10 молекул сахаров).
Моносахариды: рибоза, дезоксирибоза, глюкоза, фруктоза. Олигосахариды: мальтоза, лактоза, сахароза. Полисахариды: целлюлоза, крахмал, гликоген, хитин.
Функции углеводов:
1. Энергетическая (глюкоза).
2. Запасающая (крахмал и гликоген).
3. Строительная, или структурная (целлюлоза, хитин).
4. Рецепторная (гликопротеины).
Липиды
Липиды — жиры и жироподобные органические соединения, практически нерастворимые в воде. Их содержание в разных клетках сильно варьирует: от 2—3 до 50—90 % в клетках семян растений и жировой ткани животных. В химическом отношении липиды, как правило, сложные эфиры жирных кислот и ряда спиртов. Они делятся на несколько классов. Наиболее распространены в живой природе нейтральные жиры, воски, фосфолипиды, стероиды. В состав большинства липидов входят жирные кислоты, молекулы которых содержат гидрофобный длинноцепочечный углеводородный «хвост» и гидрофильную карбоксильную группу.
Функции липидов:
1. Строительная, или структурная (фосфолипиды, холестерин).
2. Гормональная, или регуляторная (тестостерон, прогестерон, кортизон).
3. Энергетическая.
4. Запасающая.
5. Защитная.
6. Участие в метаболизме (витамин D).
Белки
Белки — это биологические гетерополимеры, мономерами которых являются аминокислоты. В образовании белков участвуют только 20 аминокислот. Они называются фундаментальными, или основными. Некоторые из аминокислот не синтезируются в организмах животных и человека и должны поступать с растительной пищей (они называются незаменимыми). Аминокислоты, соединяясь друг с другом ковалентными пептидными связями, образуют различной длины пептиды.
Выделяют 4 уровня организации белков:
Первичная структура— последовательность аминокислот в полипептидной цепи. Она образуется за счет ковалентных пептидных связей между аминокислотными остатками.
Вторичная структураобразуется укладкой полипептидных цепей в α-спираль или
β-структуру. Она поддерживается за счет водородных связей между атомами водорода групп NH- и атомами кислорода групп СО—, α-спиральформируется в результате скручивания полипептидной цепи в спираль с одинаковыми расстояниями между витками. Она характерна для глобулярных белков, имеющих сферическую форму глобулы, β-структура представляет собой продольную укладку трех полипептидных цепей. Она характерна для фибриллярных белков, имеющих вытянутую форму фибриллы. Третичная и четвертичная структуры имеют только глобулярные белки.
Третичная структураобразуется при сворачивании спирали в клубок (глобулу, домен). Домены — глобулоподобные образования с гидрофобной сердцевиной и гидрофильным наружным слоем. Третичная структура формируется за счет связей, образующихся между радикалами R-аминокислот, за счет ионных, гидрофобных и дисперсионных взаимодействий, а также за счет образования дисульфидных (S—S) связей между радикалами цистеина.
Четвертичная структурахарактерна для сложных белков, состоящих из двух и более полипептидных цепей, не связанных ковалент-ными связями, а также для белков, содержащих небелковые компоненты (ионы металлов, коферменты). Четвертичная структура поддерживается такими же химическими связями, как итретичная.
Утрата белковой молекулой своей структурной организации называется денатурацией.
По химическому составу различают простые и сложные белки. Простые белки состоят только из аминокислот. Сложные белки содержат белковую часть и небелковую — простетические группы.
Функции белков:
1. Каталитическая, или ферментативная (все ферменты).
2. Строительная, или структурная (кератины, коллаген, эластин).
3. Транспортная (гемоглобин).
4. Гормональная, или регуляторная (инсулин).
5. Защитная (иммуноглобулины).
6. Сократительная, или двигательная (актин и миозин).
7. Рецепторная (сигнальная).
8. Энергетическая.
Нуклеиновые кислоты
Существуют два типа нуклеиновых кислот: ДНК и РНК. Нуклеиновые кислоты — полимеры, мономерами которых служат нуклеотиды. Нуклеотиды ДНК и РНК состоят из следующих компонентов:
1. Азотистое основание(в ДНК: аденин, гуанин, цитозин и тимин; в РНК: аденин, гуанин, цитозин и урацил).
2. Сахар-пентоза (в ДНК — дезоксирибоза, в РНК — рибоза).
Остаток фосфорной кислоты.
ДНК (дезоксирибонуклеиновые кислоты)— длинноцепочечный не-разветвленный полимер, состоящий из четырех типов мономеров — нуклеотидов А, Т, Г и Ц — связанных друг с другом ковалентной связью через остатки фосфорной кислоты.
Молекула ДНК состоит из двух спирально закрученных цепей (двойная спираль). При этом аденин образует 2 водородные связи с тимином, а гуанин — 3 связи с цитозином. Эти пары азотистых оснований называют комплементарными.
Связываясь с белками, молекула ДНК образует хромосому. Хромосома — комплекс одной молекулы ДНК с белками. Молекулы ДНК эукариотических организмов (грибов, растений и животных) линейны, незамкнуты, связаны с белками, образуя хромосомы. У прокариот (бактерий) ДНК замкнута в кольцо, не связана с белками, не образует линейную хромосому.
Функция ДНК:хранение, передача и воспроизведение в ряду поколений генетической информации. ДНК определяет, какие белки и в каких количествах необходимо синтезировать.
РНК (рибонуклеиновые кислоты)вместо дезоксирибозы содержат рибозу, а вместо тимина — урацил. РНК, как правило, имеют лишь одну цепь, более короткую, чем цепи ДНК. Двуцепочечные РНК встречаются у некоторых вирусов.
Виды РНК:
Информационная (матричная) РНК — иРНК (или мРНК).
Транспортная РНК — тРНК.
Рибосомная РНК — рРНК.
Функции РНК:участие в биосинтезе белков.
Молекулы ДНК обладают способностью, неприсущей ни одной другой молекуле, — способностью к удвоению. Процесс удвоения молекул ДНК называется репликацией. Воснове репликации лежит принцип комплементарности — образование водородных связей между нуклеотидами А и Т, Г и Ц.
