Механизм реакций нуклеофильного замещения
В 30-х годах ХХ столетия на основе фундаментальных исследований кинетики и стереохимии реакций было предложено два граничных механизма нуклеофильного замещения:
– бимолекулярное нуклеофильное замещение SN2;
- мономолекулярное нуклеофильное замещение SN1.
Бимолекулярное нуклеофильное замещение.
Реакциябимолекулярного нуклеофильного замещения,протекающая по механизму SN2, является одностадийным синхронным процессом.
1. Нуклеофил атакует субстрат со стороны, противоположной нуклеофугу (такое направление реакции называют «атакой с тыла»).
2. Образование связи с нуклеофилом протекает одновременно с разрывом связимежду атомом углерода и уходящим галогенид-ионом.
3. При переходном состоянии нуклеофил и нуклеофуг связаны с центральным атомом углерода посредством 2р-орбитали атома углерода и свободных пар электронов нуклеофила и уходящего иона:
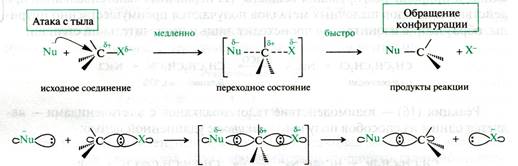
Рис. 18.3. Схема реакции бимолекулярного нуклеофильного замещения
Энергетическая характеристика реакции нуклеофильного замещения.
1. Достижение переходного состояния определяет скорость реакции в целом.
2. Переходное состояние соответствует максимуму на энергетическом профиле пути реакции:
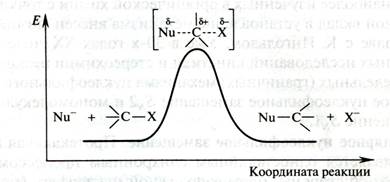
Рис. 18.4. Энергетическая диаграмма реакции бимолекулярного нуклеофильного замещения
Стереохимия реакции нуклеофильного замещения.
1. Наличие большого числа алкильных групп, связанных с электрофильным атомом углерода, приводит к стерическим затруднениям для атаки нуклеофилом.
2. В переходном состоянии атом углерода становится пентакоординированным (см. рис. 18.4).
3. Заместители большого объема создают пространственные трудности в переходном состоянии. Это увеличивает энергию переходного состояния, и реакция протекает медленнее.
Влияние алкильных групп в бромсодержащих субстратах на скорость реакции с иодид-ионом (в ацетоне) иллюстрируется нижеприведенным рядом соединений:
Рис. 18.6.
1. В переходном состоянии
- три связи атома углерода располагаются в одной плоскости (как спицы в колесе);
- возникающая связь с нуклеофилом и разрывающаяся связь с нуклеофугом направлены перпендикулярно к плоскости (как ось в колесе).
2. По мере отрыва галогенид-иона происходит возврат в тетраэдрическое состояние реагирующего атома углерода с иной конфигурацией заместителей относительно реакционного центра. Такой процесс сравнивают с выворачиванием зонтика от сильного ветра.
3. Поскольку реакция приводит к получению соединения, конфигурация которого противоположна исходному, это означает, что реакция, протекающая по механизму SN2, происходит с обращение конфигурации. Это обстоятельство особенно важно, когда реакционным центром в субстрате служи асимметрический атом углерода. Так, в результате гидролиза (S)-2-бромооктана образуется (R)-октанол-2:
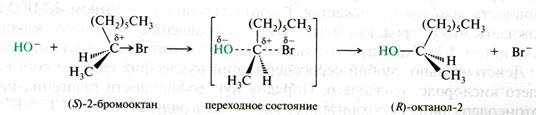
Рис. 18.5. Стереохимия реакции бимолекулярного нуклеофильного замещения в галогенводородах
Примером реакции, протекающей по механизму бимолекулярного нуклеофильного замещения, является гидролиз бромметана в водном растворе щелочи:
CH3Br + NaOH → CH3OH +NaBr
