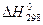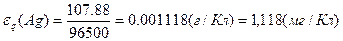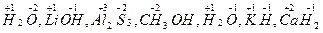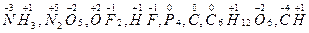| № п/п | Назва | Формула | Позначення | Одиниці вимірювання |
| | | | | |
| | Маса речовини | ___ | m | кг(г)* |
| | Об’єм | ___ | V | 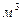 (л, мл) (л, мл) |
| | Густина речовини | 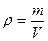 | 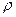 - густина речовини або розчину - густина речовини або розчину | 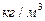 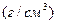 |
| | Атомна одиниця маси | а.о.м.= 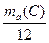 | а.о.м. 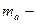 маса атома, С - Карбон маса атома, С - Карбон | кг (г) |
| | Відносна атомна маса | 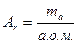 | 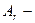 відно-сна атомна маса відно-сна атомна маса | __ |
| | Відносна молекулярна маса | 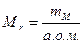 або або 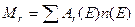 | 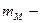 маса молекули n(Е)-число атомів елемента маса молекули n(Е)-число атомів елемента | ___ |
| Визначення та приклад розрахунку або запису |
| |
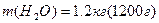 |
 |
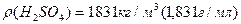 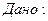 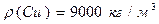 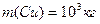 V-? V-? 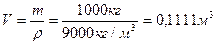 |
1/12 маса атома нукліда Карбону 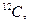 що дорівнює що дорівнює 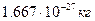 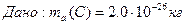 а.о.м. - ? а.о.м а.о.м. - ? а.о.м 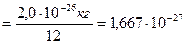 кг кг |
Величина, що дорівнює відношенню середньої маси атома до 1/12 маси атома Карбону 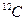 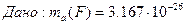 кг кг 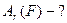 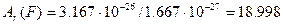 |
Дано: хімічна формула води Н2О 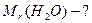 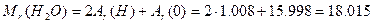 |
| | | | | |
| | Молярна маса | 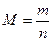 | n-кількість речовини (моль) або 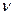 | кг/моль (г/моль) |
| | Моль | 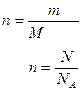 | N-число молекул атомів чи інших структур-них одиниць | моль |
| | Число Авогадро (стала Авогадро) | 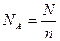 | N 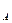 -число Авогадро -число Авогадро | 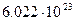 1/моль 1/моль |
| | Молярний об’єм газу | 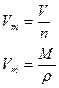 | V 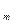 -молярний об’єм газу -молярний об’єм газу | 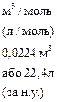 |
| | Відносна густина газу | 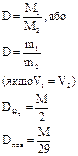 | D-відносна густина газу | __ |
| |
Маса одного моля речовини, виражена в кілограмах або грамах 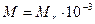 (кг/моль) або (кг/моль) або 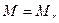 (г/моль) (г/моль) 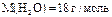 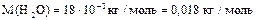  |
Кількість речовини, що містить стільки структурних одиниць (атомів, молекул, йонів, електронів, тощо), скільки атомів містить в 0,012 кг нукліда Карбону 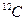 Дано: m(H Дано: m(H 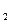 O)=90 г n-? O)=90 г n-? 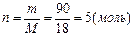 , або , або 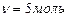 |
Число структурних одиниць, що міститься в 1 моль речовини Обчислити абсолютну масу молекули азоту. 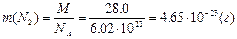 |
Відношення об’єму речовини до кількість цієї речовини Дано: 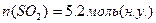 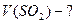 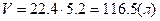 Визначити густину повітря за н.у. Визначити густину повітря за н.у. 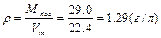 |
Визначити густину азоту за воднем. 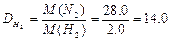 Дано: Дано: 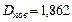 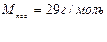 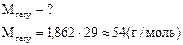 |
| | | | | |
| | Масова частка (елемента в речовині ) | 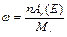 | 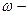 масова частка масова частка 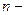 число атомів елемента число атомів елемента | ___ |
| | Об’ємна частка речовини | 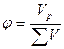 | 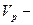 об’єм речовини; об’єм речовини; 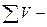 загальний об’єм загальний об’єм | ___ |
| | Температура | ___ | t | К (кельвін) 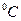 (гра-дус Цельсія) (гра-дус Цельсія) |
| | Тиск | ___ | P | Па (паскаль) (атм) |
| | Кількість теплоти | 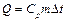 | 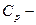 теплоємність теплоємність 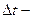 зміна температури зміна температури | Дж, кДж (кал) |
| | Час | ___ | 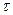 | с (хв) |
| | Валентність | 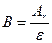 | В-валентність, позначається римським цифрами І, ІІ, ІІІ… | |
| | Хімічний еквівалент (елемента) | 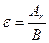 | 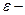 еквівалент еквівалент | |
| |
Дано: Дифосфатну кислоту Н 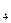 Р Р 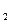 О О 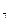 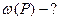 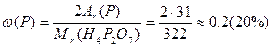 |
Дано: суміш, що складається з 2 л О 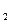 і 3 л N і 3 л N 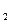 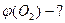 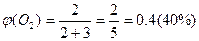 |
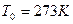 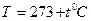 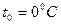 |
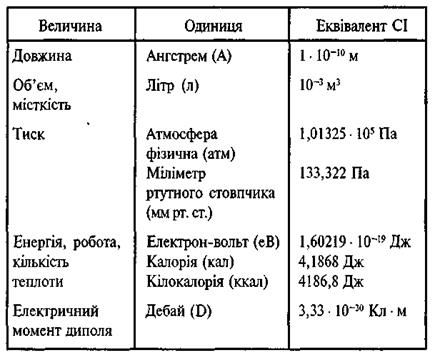
1атм=1,013 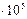 Па=760 мм.рт. ст. Па=760 мм.рт. ст. |
| 1 кал=4,18 Дж |
| 1 хв=60 c |
Здатність атома хімічного елемента сполучатися з певним числом атомів інших елементів або приєднувати число спільних електронних пар, які зв’язують атоми Н:Н або Н-Н, Н-О-Н В(Н)=І Н-О-О-Н В(0)=ІІ :N 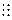 N: або N N: або N 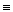 N B(N)=III NH N B(N)=III NH 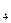 Cl B(N)=IV Cl B(N)=IV |
Кількість елемента, що сполучається з одним молем атомів Гідрогену або заміщує таку саму кількість атомів водню в інших реакціях 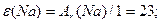 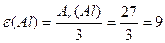 |
| | | | | |
| | Молярна маса еквіва-лента | 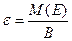 | М(Е)- молярна маса атомів елемента | кг/моль (г/моль) |
| | Еквівалент оксидів | 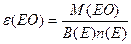 або або 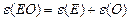 | В(Е)- валент-ність n(E)-число атомів елемента | |
| | Кислот | 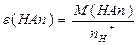 або або 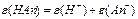 | n-число йонів Н 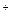 (основність) (основність) 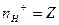 | |
| | Основ | 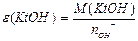 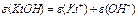 | n-число групи ОН 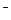 (кислот-ність) (кислот-ність) 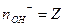 | |
| | Солей | 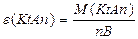 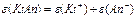 | В-валент-ність металу; n-число катіонів Z=n B | |
| |
Маса одного еквівалента елемента називається молярною масою еквівалента Визначити молярні маси еквівалентів елементів у сполуках: 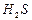 та та 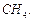 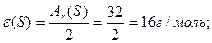 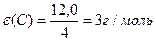 |
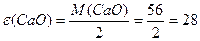 ; ; 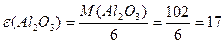 або або 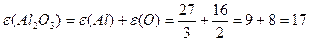 |
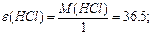 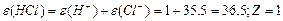 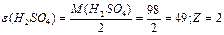 або або 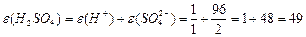 |
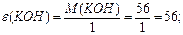 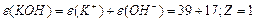 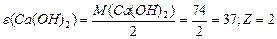 або або 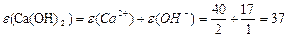 |
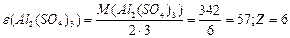 , або , або 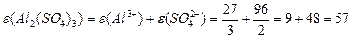 |
| | | | | |
| | Еквівалент електро-хімічний | 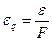 | 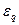 -електро-хімічний еквівалент F- число Фарадея -електро-хімічний еквівалент F- число Фарадея | (г/Кл, мг/Кл) |
| | Ступінь окиснення | ___ | с.о. познача-ється арабськи-ми цифрами із знаком “+” або “-” | ___ |
| | Електродний потенціал (стандартний) | | Е, е 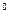 | В (мВ) |
| | Окисно-відновний потенціал (стандартний) | | Е, е 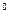 | В (мВ) |
| | Ентальпія (теплота) утворення речовини Стандартна ентальпія утворення | 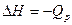 | 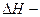 змі-на ентальпії або змі-на ентальпії або 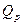 - тепловий ефект за сталого тиску Р=соnst - тепловий ефект за сталого тиску Р=соnst 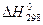 | кДж/моль (ккал/моль) |
| | | | | | | | | | | | |
| |
Маса речовини, що окислюється або відновлюється на електродах внаслідок проходження крізь електроліт 1Кл електрики 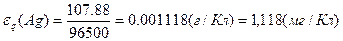 |
Умовний заряд атома в сполуці, обчислений виходячи з припущення, що дана сполука складається тільки з йонів 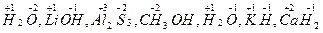 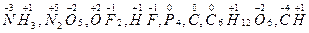 |
| Потенціал, що виникає на межі поділу метал-розчин в разі занурення металевої пластинки в розчин її солі (стандартний - в разі концентрації йонів в солі 1 моль/л, Т=298 К відносно стандартного водневого електрода) |
| Кількість теплоти, яка виділяється або поглинається внаслідок утворення одного моля речовини з простих речовин Ентальпія, виміряна за стандартних умов, називається стандартною ентальпією (Т=298 К, Р=101,3 кПа) |
Співвідношення між деякими позасистемними одиницями та одиницями CI
Наши рекомендации
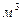 (л, мл)
(л, мл) 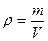
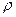 - густина речовини або розчину
- густина речовини або розчину 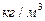
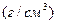
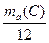
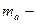 маса атома, С - Карбон
маса атома, С - Карбон 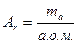
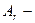 відно-сна атомна маса
відно-сна атомна маса 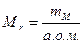 або
або 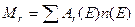
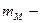 маса молекули n(Е)-число атомів елемента
маса молекули n(Е)-число атомів елемента 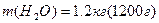

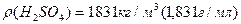
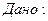
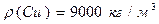
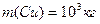 V-?
V-? 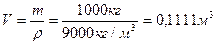
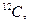 що дорівнює
що дорівнює 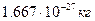
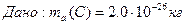 а.о.м. - ? а.о.м
а.о.м. - ? а.о.м 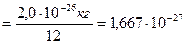 кг
кг 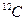
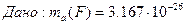 кг
кг 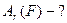
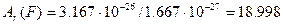
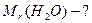
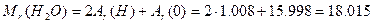
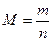
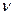
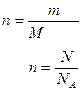
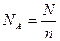
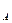 -число Авогадро
-число Авогадро 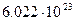 1/моль
1/моль 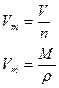
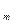 -молярний об’єм газу
-молярний об’єм газу 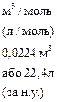
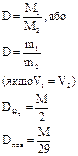
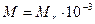 (кг/моль) або
(кг/моль) або 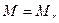 (г/моль)
(г/моль) 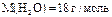
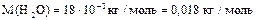

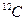 Дано: m(H
Дано: m(H 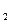 O)=90 г n-?
O)=90 г n-? 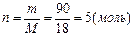 , або
, або 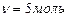
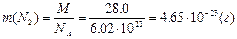
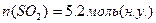
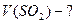
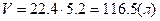 Визначити густину повітря за н.у.
Визначити густину повітря за н.у. 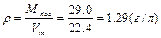
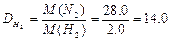 Дано:
Дано: 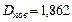
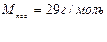
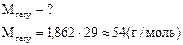
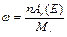
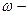 масова частка
масова частка 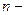 число атомів елемента
число атомів елемента 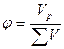
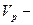 об’єм речовини;
об’єм речовини; 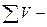 загальний об’єм
загальний об’єм 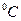 (гра-дус Цельсія)
(гра-дус Цельсія) 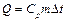
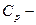 теплоємність
теплоємність 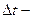 зміна температури
зміна температури 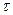
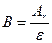
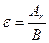
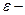 еквівалент
еквівалент 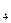 Р
Р 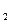 О
О 
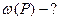
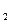 і 3 л N
і 3 л N 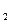
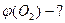
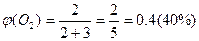
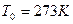
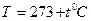
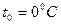
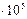 Па=760 мм.рт. ст.
Па=760 мм.рт. ст. 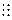 N: або N
N: або N 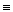 N B(N)=III NH
N B(N)=III NH 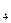 Cl B(N)=IV
Cl B(N)=IV 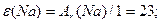
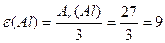
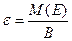
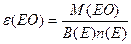 або
або 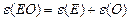
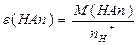 або
або 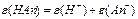
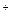 (основність)
(основність) 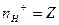
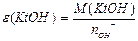
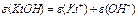
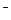 (кислот-ність)
(кислот-ність) 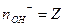
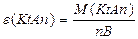
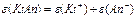
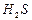 та
та 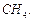
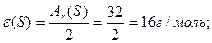
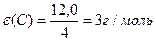
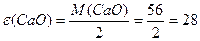 ;
; 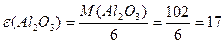 або
або 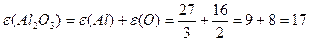
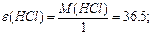
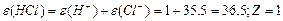
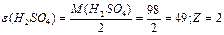 або
або 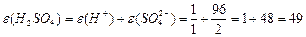
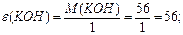
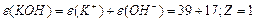
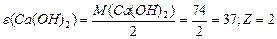 або
або 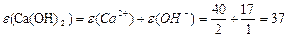
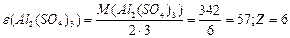 , або
, або 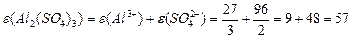
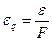
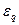 -електро-хімічний еквівалент F- число Фарадея
-електро-хімічний еквівалент F- число Фарадея 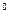
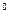
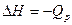
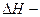 змі-на ентальпії або
змі-на ентальпії або 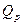 - тепловий ефект за сталого тиску Р=соnst
- тепловий ефект за сталого тиску Р=соnst