Физико-химические основы дисперсных систем и поверхностных явлений
ЗАНЯТИЕ 6
ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ ДИСПЕРСНЫХ СИСТЕМ И ПОВЕРХНОСТНЫХ ЯВЛЕНИЙ
Адсорбция газов на неподвижных границах раздела фаз. Уравнение Ленгмюра. Адсорбция из растворов на твердых адсорбентах. Зависимость величины адсорбции от различных факторов. Ионобменная адсорбция. Адсорбция на подвижной поверхности раздела фаз. Физическая адсорбция и хемосорбция.
Адсорбция происходит на границе раздела следующих фаз:
· твёрдое тело – газ;
· твёрдое тело – раствор;
· раствор – газ.
Адсорбция на границе раздела твердое тело – газ
Адсорбцию газов углем открыли К. Шееле в 1773 г. и Ф. Фонтана в 1777 г. В 1915 г. Н.Д. Зелинский разработал способ получения активированного угля, который был использован в противогазах. Адсорбция газов поверхностью твердого тела растет с увеличением парциального давления газа и с уменьшением температуры. Адсорбция, отнесенная к единице массы, возрастает с увеличением площади поверхности адсорбента.
Адсорбция зависит от природы адсорбента и адсорбата. Наиболее распространенные адсорбенты - активированные угли: хорошо адсорбируют малополярные газы (О2, SO2, NH3, углеводороды), но не адсорбируют высокополярные пары (H2O) и газы с низкой температурой конденсации (Н2, N2, CO). Гидрофильный адсорбент силикагель (пористое тело на основе кремневой кислоты) хорошо сорбирует пары воды и другие полярные газы. Другие адсорбенты − цеолиты, алюмосиликатные пористые вещества − обладают избирательной адсорбционной способностью (молекулярные сита).
По адсорбируемости на металлах газы можно расположить в ряд:
О2 >C2H4 > CO > H2 > CO2 > N2
Наибольшей адсорбционной способностью обладают d-элементы IV−VIII групп, а наименьшей способностью − тяжелые р-металлы и d-металлы с заполненными d-подуровнями.
Адсорбция на границе раздела твердое тело – жидкость
При адсорбции на границе раздела твердое тело − жидкость величина избытка адсорбируемого вещества становится функцией молярной концентрации раствора (рисунок 2).

Рисунок 2 − Изотерма адсорбции из растворов
Адсорбция из растворов имеет существенные отличия от газовой адсорбции. Это вызвано следующими причинами:
· на адсорбенте может адсорбироваться не только растворенное вещество, но и сам растворитель. Чем лучше протекает адсорбция растворителя, тем труднее будет адсорбироваться растворенное вещество;
· растворитель может растворять адсорбент. Чем лучше растворитель растворяет адсорбент, тем труднее протекает на нём адсорбция;
· скорость адсорбции из раствора зависит от скорости диффузии. В результате обеднения извлекаемым веществом слоев воды, прилежащих к адсорбенту, дальнейшая адсорбция определяется скоростью диффузии поглощаемого вещества к адсорбенту. Как известно, диффузия в жидкостях достаточно медленный процесс, поэтому для ускорения адсорбции прибегают к перемешиванию раствора.
Правило выравнивания полярностей (М.А. Ребиндер): на полярных адсорбентах лучше всего адсорбируются полярные адсорбаты из неполярных растворителей, а на неполярных – неполярные адсорбаты из полярных растворителей.
Поглощение растворенного вещества из раствора зависит от его строения.
Адсорбция на подвижной поверхности раздела фаз - адсорбция ПАВ.
Поверхностно-активные (ПАВ) и поверхностно-неактивные вещества. Изменение поверхностной активности в гомологических рядах (правило Траубе).
Вещества, добавление которых к растворителю уменьшает поверхностное натяжение, называют поверхностно-активными(ПАВ). Вещества, добавление которых увеличивает или не изменяет поверхностное натяжение, называют поверхностно-инактивными.
Рассмотрим поверхностно-активные, или дифильные (двояколюбящие), вещества. Поверхностно-активные вещества состоят из двух частей (рисунок 5):
· полярной;
· неполярной.

Рисунок 5 − Строение поверхностно-активных веществ
ПАВ являются следующие классы веществ:
· спирты R-OH;
· альдегиды R-COH;
· карбоновые кислотыR-COOH.
Углеводородные радикалы (CH3-; C2H5-; C17H35- и т.д) представляют собой неполярную часть поверхностно-активного вещества, которая может быть как угодно длинной.
Функциональные группы – COH, COOH представляют полярную часть поверхностно-активного вещества (ПАВ). Примеры ПАВ: олеиновая кислота (С17H33COOH), натриевая соль стеариновой кислоты (C17H35COONa, мыло).
Молекулы ПАВ менее полярны, чем молекулы воды. Благодаря этому взаимодействие молекул воды между собой сильнее, чем молекул воды с молекулами ПАВ. В результате молекулы ПАВ будут вытесняться из раствора в поверхностный слой. Повышение концентрации третьего вещества в поверхностном слое, в частности, молекул ПАВ, приводит к понижению поверхностного натяжения (рисунок 6).
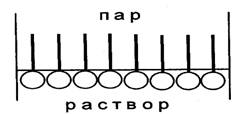
Рисунок 6 – Предельная ориентация молекул поверхностно-активных веществ в поверхностном слое
Исследуя поверхностное натяжение водных растворов органических веществ, Траубе и Дюкло установили для гомологических рядов поверхностно-активных веществ следующее эмпирическое правило:
В любом гомологическом ряду при малых концетрациях удлинение углеродной цепи на одну группу СН2 увеличивает поверхностную активность в 3−3,5 раза.
Изменение поверхностного натяжения под действием ПАВ влияет на смачиваемость твердых тел жидкостью. Например, для очистки тканей (стирка, чистка) или металлов от жировых загрязнений применяют ПАВ. ПАВ позволяет разделить пустую породу и руду при флотации руд.
Ионные ПАВ применяются в хирургии в качестве антисептиков. Механизм молекулярной адсорбции лежит в основе гемосорбции – очищении крови от токсических веществ с помощью различных адсорбентов.
4. Дисперсные системы и их классификация по: степени дисперсности; агрегатному состоянию фаз; силе межмолекулярного взаимодействия между дисперсной фазой и дисперсионной средой.
Дисперсные системы, рассматриваемые в коллоидной химии, гетерогенны, поэтому состоят как минимум из двух фаз. Одна из них является сплошной и называется дисперсионной средой. Другая фаза раздроблена и распределена в первой; её называют дисперсной фазой.
Наиболее общая классификация дисперсных систем основана на определении агрегатного состояния дисперсной фазы и дисперсионной среды. Сочетания трёх агрегатных состояний (твёрдое, жидкое и газообразное) позволяют выделить девять типов дисперсных систем (табл.1). Для краткости их условно обозначают дробью, числитель которой указывает на агрегатное состояние дисперсной фазы, а знаменатель – дисперсионной среды, например обозначение Т/Ж показывает, что система состоит из твёрдой дисперсной фазы и жидкой дисперсионной среды (твёрдое в жидкости).
Таблица 1. Классификация дисперсных систем по агрегатному состоянию фаз
| Дисперсионная среда | Дисперсная фаза | Условное обозначение системы | Название системы и примеры |
| Твёрдая | Твёрдая | Т/Т | Твёрдые гетерогенные системы: минералы, сплавы, бетон, композиционные материалы |
| Жидкая | Ж/Т | Капиллярные системы: жидкость в пористых телах, адсорбентах; влажные почвы, грунты | |
| Газообразная | Г/Т | Пористые тела: адсорбенты и катализаторы | |
| Жидкая | Твёрдая | Т/Ж | Суспензии и золи: промышленные суспензии, пульпы, взвеси, пасты, илы |
| Жидкая | Ж/Ж | Эмульсии: природная нефть, кремы, молоко | |
| Газообразная | Г/Ж | Газовые эмульсии и пены | |
| Газообразная | Твёрдая | Т/Г | Аэрозоли: пыли, дымы. Порошки |
| Жидкая | Ж/Г | Аэрозоли: туманы, в том числе промышленные облака | |
| Газообразная | Г/Г | Коллоидная система не образуется |
Одно из девяти сочетаний Г/Г не может соответствовать коллоидной системе, так как газы в обычных условиях при любых концентрациях дают истинные растворы (при очень высоких давлениях некоторые газовые системы образуют гетерогенные системы). Однако газовые смеси могут проявлять отдельные свойства гетерогенно-дисперсных систем благодаря непрерывным флуктуациям плотности и концентрации, вызывающим неоднородности в системе. Рассматривая жидкие растворы с молекулярной степенью дисперсности, к гетерогенно-дисперсным системам можно отнести растворы полимеров. Размеры макромолекул могут превышать размеры обычных коллоидных частиц. Эти системы обладают многими свойствами, характерными для типичных гетерогенно-дисперсных систем. Они как бы связывают в единое целое все дисперсные системы и указывают на непрерывность перехода от истинных молекулярных растворов к гетерогенным дисперсным системам.
Все дисперсные системы также можно разделить на два класса по кинетическим свойствам дисперсной фазы: свободнодисперсные системы, в которых дисперсная фаза подвижна, и связнодисперсные системы – системы с твердообразной дисперсионной средой, в которой частицы дисперсной фазы не могут свободно перемещаться.
И еще эти системы классифицируют по степени дисперсности. Свободнодисперсные системы подразделяют на ультрамикрогетерогенные, размер частиц которых лежит в пределах от 10-9 до 10-7 м (от 1 до 100 нм), микрогетерогенные с размером частиц от 10-7 до 10-5 м (от 0,1 до 10 мкм) и грубодисперсные с частицами, размеры которых превышают 10-5 м.
Ультрамикрогетерогенные системы часто называют истинно коллоидными или просто коллоидными, так как раньше только такие системы считались объектом коллоидной химии. Такие частицы обладают определенным агрегатным состоянием.
С ростом числа молекул в частице она постепенно приобретает все свойства фазы. В современной литературе малоконцентрированные свободнодисперсные ультрамикрогетерогенные системы чаще называют золями (нем. Sole от лат. solutio – раствор). Среди них различают аэрозоли – золи с газообразной дисперсионной средой; лиозоли – золи с жидкой дисперсионной средой (греч. lios – жидкость). В зависимости от природы среды лиозоли называют гидрозолями (вода), органозолями (органическая среда) или, более конкретно, алкозолями (спирты) и т. д.
Cвязнодисперсные (структурированные) системы с жидкой дисперсионной средой называют гелями.
К микрогетерогенным системам относят суспензии (Т/Ж), эмульсии (Ж/Ж), пены (Г/Ж), порошки (Т/Г). Эти системы имеют большое значение в промышленности. Из грубодисперсных систем наиболее распространены системы Т/Г (песок, щебень и др.).
Схема строения мицеллы.
Пример: золь иодида серебра, полученного по реакции взаимодействия АgNO3 и KI при избытке KI.
АgNO3 + KI → АgI¯ + К NO3

1 – агрегат; 2 – потенциалопределяющие ионы; 3 – ядро; 4 – противоины адсорбционного слоя; 5 – противоионы диффузного слоя; 6 – гранула.
6. Свойства лиофобных коллоидных растворов: молекулярно-кинетические, оптические, диализ, электродиализ.
Основные свойства лиофобных золей связаны с их ультрамик-рогетерогенностью, т. е. мельчайшими размерами частиц дисперсной фазы, и огромной суммарной поверхностью раздела между дисперсной фазой и дисперсионной средой.
Молекулярно-кинетические свойства (МКС).К ним относятся свойства, связанные с тепловым движением частиц: броуновское движение, диффузия, осмос. Эти свойства зависят от размеров и массы частиц дисперсной фазы (броуновское движение и диффузия), а также от числа частиц в единице объема системы (осмотическое давление). Так как размеры коллоидных частиц значительно больше размеров отдельных ионов и молекул, то, при одинаковой массовой концентрации, число коллоидных частиц в единице объема коллоидного раствора будет гораздо меньше, чем число молекул или ионов в единице объема истинных растворов низкомолекулярных веществ. Этим объясняется тот факт, что МКС в коллоидных растворах выражены менее интенсивно, чем в истинных: скорость диффузии коллоидных частиц очень мала, осмотическое давление коллоидных растворов низкое. Так, осмотическое давление 1% истинного раствора сахара составляет 79,5 кПа, а 1% коллоидного раствора сульфида мышьяка(3) AS2S3 - всего 3,4 × 10-3кПа.
Оптические свойства.Специфическим свойством коллоидных растворов является их способность рассеивать свет. Это обусловлено гетерогенностью коллоидных систем и размерами коллоидных частиц.
Грубодисперсные системы, размеры частиц в которых (r > > 10-6 м) значительно превышают длины волн видимого света (𝝀 = (3,6-7,6) ×10-7 м), отражают свет и поэтому выглядят мутными. В истинных растворах низкомолекулярных веществ молекулы и ионы имеют размеры 10-10-10-9 м, что значительно меньше длин волн видимого света, поэтому они пропускают свет и являются прозрачными.
Если размеры коллоидных частиц (r = 10-7-10-6 м) соизмеримы с длинами волн видимого света, то такие коллоидные растворы рассеивают свет вследствие явления дифракции. Рассеяние света можно наблюдать при боковом освещении коллоидного раствора: в случае точечного источника света - в виде светящегося конуса (эффект Тиндаля), а при обычном боковом освещении - в виде голубоватой опалесценции раствора. Согласно закону Рэлея интенсивность рассеянного света I зависит от интенсивности I0и длины волны 𝝀падающего света, объема частиц V и их концентрации с:
I = IoK 
где К - константа, зависящая от соотношения коэффициентов преломления дисперсионной среды и дисперсной фазы.
Из этого выражения следует, что чем меньше длина волны падающего излучения, тем больше будет рассеяние. Этим объясняется голубоватая опалесценция при боковом освещении коллоидных растворов. Красный свет имеет наибольшую длину волны (620-760 нм) в видимой части спектра и рассеивается в меньшей степени. Поэтому запрещающие сигналы имеют красный цвет. Рассеянный солнечный свет, который образуется из-за аэрозольных частиц в атмосфере, имеет голубую окраску и создает голубой цвет неба. На способности золей рассеивать свет основаны такие методы анализа, как нефелометрия и ультрамикроскопия, которые используются для определения концентрации частиц и их размеров в гетерогенных биологических средах.
Диализ.Биологические жидкости, как правило, содержат одновременно вещества в коллоидном состоянии и в виде отдельных молекул и ионов. Очистка коллоидных растворов от истинно растворенных веществ основывается на том, что относительно крупные коллоидные частицы, в отличие от молекул и ионов, не проникают сквозь поры животных и растительных мембран. На практике в качестве мембраны используется пленка из коллодия или целлофана (производные целлюлозы), а также кишечная ткань.
Диализ- процесс очистки коллоидных растворов от ионов и молекул низкомолекулярных примесей в результате их диффузии в чистый растворитель сквозь полупроницаемую мембрану.
Простейший способ диализа заключается в том, что коллоидный раствор помещают во внутренний сосуд, дно или стенки которого представляют собой мембрану с избирательной проницаемостью, погруженный во внешний сосуд с чистым растворителем (обычно вода). В результате диффузии молекулы и ионы, способные проникать сквозь поры мембраны, переходят в наружный сосуд. В обычных условиях диализ протекает очень медленно. Для ускорения процесса необходимо увеличить градиент концентраций растворенных веществ по обе стороны мембраны. Это легко осуществить периодической или непрерывной сменой растворителя в наружном сосуде (рис. 7 а).
Для ускорения очистки коллоидных растворов от ионов растворенных электролитов используют также метод электродиализа. В этом случае во внешний сосуд помещают электроды и подают постоянный электрический ток (рис. 7 б).
Электродиализ- это диализ в условиях наложения постоянного электрического поля, под действием которого катионы и анионы приобретают направленное движение к электродам.
 |
Электродиализ особенно эффективен при малых концентрациях удаляемого электролита, когда градиент концентраций невелик.
Рис. 7.Схемы диализатора (а) и электродиализатора (б):
1 - диализуемый коллоидный раствор; 2 - мембрана; 3 - подача растворителя; 4 - мешалка; 5 - электроды
В биологических жидкостях количественное определение низкомолекулярных веществ часто проводят методом компенсационного диализа, или вивидиализа. В этом случае биологическая жидкость в диализаторе омывается не чистым растворителем, а растворами с различными концентрациями определяемого вещества. Так, содержание сахара в сыворотке крови определяется путем диализа сыворотки по сравнению с изотоническим раствором, к которому добавляют различные количества сахара. Концентрация сахара во внешнем растворе не изменяется лишь в том случае, когда она равна концентрации сахара в анализируемой сыворотке. Таким образом было выявлено наличие глюкозы и мочевины в крови.
По принципу диализа работает аппарат «искусственная почка» (АИП), применяемый при острой почечной недостаточности, которая может наступить в результате отравления сулемой, сульфаниламидными препаратами, при уремии после переливания крови, при тяжелых ожогах и т. п. АИП подключается к системе кровообращения больного, и кровь протекает через систему, снабженную мембранами с избирательной проницаемостью, которые снаружи омываются физиологическим раствором. При этом кровь в процессе диализа очищается от вредных примесей, после чего поступает обратно в организм.
7. Устойчивость коллоидных растворов: седиментационная, агрегативная. Факторы, влияющие на устойчивость лиозолей.
Устойчивость коллоидных растворов.Биологические жидкости живого организма, такие как кровь, плазма, лимфа, спинномозговая жидкость, моча, представляют собой коллоидные системы. О состоянии организма можно судить по многим показателям этих жидкостей, и прежде всего крови. Наличие патологических процессов сопровождается изменением количества форменных элементов крови (эритроцитов, лейкоцитов и др.), скорости оседания эритроцитов (СОЭ), свертываемости крови и др. Все эти свойства связаны с устойчивостью биологических жидкостей, поэтому изучение устойчивости коллоидных растворов и факторов, влияющих на нее, очень важно для медиков и биологов.
Устойчивость дисперсных системхарактеризует способность дисперсной фазы сохранять состояние равномерного распределения частиц дисперсной фазы во всем объеме дисперсионной среды.
В дисперсных системах различают седиментационную и агрегативную устойчивость.
Седиментационная устойчивостьхарактеризует способность частиц дисперсной фазы находиться во взвешенном состоянии и не оседать под действием сил тяжести.
Агрегативная устойчивостьхарактеризует способность частиц дисперсной фазы противодействовать их слипанию между собой и тем самым сохранять неизменными cвои размеры.
Грубодисперсные системы гетерогенны и неустойчивы. Они самопроизвольно расслаиваются на дисперсную фазу и дисперсионную среду, так как относительно крупные частицы дисперсной фазы под действием сил тяжести оседают (седиментируют).
Истинные растворы гомогенны и неограниченно устойчивы, поскольку в них не происходит самопроизвольное выделение растворенного вещества из системы.
Коллоидные растворы относятся к ультрамикрогетерогенным системам и по устойчивости занимают промежуточное положение между грубодисперсными системами и истинными растворами. Коллоидные растворы обычно представляют собой седиментационно устойчивые системы, что обусловлено малыми размерами частиц и их интенсивным броуновским движением.
Агрегативная устойчивость коллоидных растворов с ионным стабилизатором обусловлена наличием на поверхности частиц «рыхлой» ионной атмосферы из гидратированных противоионов, которая увеличивает сродство коллоидных частиц к дисперсной среде и препятствует их слипанию (коагуляции). Ее можно рассматривать как результат взаимодействия двух противоположно направленных сил, которые одновременно действуют на сближающиеся коллоидные частицы: вандерваальсовых сил межмолекулярного притяжения и электростатических сил отталкивания, которые возникают между одноименно заряженными частицами. При сближении коллоидных частиц на расстояние 10-9-10-6 м в области перекрывания их ионных атмосфер, в тонких жидких пленках, разделяющих две твердые поверхности (поверхности ядер), возникает так называемое расклинивающее давление. Оно складывается из трех основных составляющих:
- электростатическое отталкивание одноименно заряженных частиц за счет большого скопления противоионов в области контакта ионных атмосфер;
-
 |
расклинивание за счет упругих свойств гидратных оболочек, окружающих противоионы и состоящих из ориентированных (упорядоченных) диполей воды;
Рис. 8.Схема агрегативной устойчивостимицелл коллоидных растворов
- расклинивание за счет осмотического всасывания молекул растворителя в область контакта ионных атмосфер, т. е. в область большого скопления противоионов.
В коллоидных растворах с ионным стабилизатором главной составляющей расклинивающего давления является электростатическое отталкивание одноименно заряженных частиц. Величина расклинивающего давления зависит от заряда твердой фазы, т. е. от значения межфазного потенциала Фмф, а также от толщины ионной атмосферы, главным образом ее диффузного слоя, т. е. от значения ζ-потенциала (рис. 8). Чем выше заряд твердой фазы, чем больше толщина диффузного слоя и больше значение ζ-потенциала, тем больше расклинивающее давление между частицами и выше агрегативная устойчивость коллоидного раствора. Когда диффузный слой мицеллы тонкий и ζ-потенциал меньше 30 мВ, упругие свойства диффузного слоя невелики, и поэтому при столкновении мицелл происходит перекрывание этих слоев, что приводит к преобладанию сил притяжения и потере агрегативной устойчивости. Таким образом, коллоидные растворы с ионным стабилизатором агрегативно неустойчивы, если их мицеллы имеют ζ<30 мВ относительно устойчивы, если 30 < ζ < 50 мВ и устойчивы, если ζ > 50т мВ.
Рис. 11. Схема электроосмоса
1 - дисперсная система; 2 - перегородка
При электрофорезе происходит движение частиц дисперсной фазы в направлении силовых линий электрического поля. Электрофорез используют для получения новых материалов, нанесения покрытий, очистки веществ от примесей и выделения продуктов. В медицине электрофорез применяют для введения лекарственных веществ. На кожу пациента накладывают тампон, смоченный раствором лекарственного препарата, а сверху - электроды, к которым приложен низкий, безопасный для организма потенциал. В ходе этой процедуры частички лекарственного препарата под действием электрического поля переходят в ткани организма человека.
Электроосмосом называют перемещение дисперсионной среды под действием внешнего электрического поля (рис. 11). Движение дисперсионной среды обусловлено притяжением разноименных зарядов. Оно происходит зачастую в капиллярах и в каналах пористых тел. Когда ζ-потенциал отрицательный, то положительно заряженные противоионы диффузного слоя притягиваются к отрицательному электроду. Противоионы увлекают за собой жидкость, составляющую дисперсионную среду. В результате этого происходит движение жидкости, причем перемещение жидкой дисперсионной среды относительно частиц дисперсной фазы, как и в случае электрофореза, происходит по границе скольжения.
Электроосмос используют, например, для обезвоживания древесины и других пористых материалов: строительных, грунта, продуктов питания, сырья для пищевой промышленности и др. Влажную массу помещают между электродами, а вода в зависимости от структуры ДЭС движется к одному из них и собирается в специальной емкости.
Для осуществления электрофореза или электроосмоса необходимо внешнее электрическое поле, т.е. движение частиц при электрофорезе или среды при электроосмосе является следствием воздействия этого поля.
Следует отметить, что явление электрофореза характерно главным образом для коллоидных растворов (золей), т.е. для систем, у которых размеры частиц дисперсной фазы не превышают 0,1 мкм. Электроосмос может наблюдаться не только в отношении коллоидных растворов, которые являются высокодисперсными системами, но и в отношении средне- и грубодисперсных систем.
ЗАНЯТИЕ 6
ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ ДИСПЕРСНЫХ СИСТЕМ И ПОВЕРХНОСТНЫХ ЯВЛЕНИЙ
