В связи с высокой изменчивостью вируса гриппа, длительность иммунитета, вызываемого как заболеванием, так и вакцинацией составляет около 1 года.
Эффективность же самой вакцины и ее приемлемость в качестве рутинной профилактической меры определяется тремя ключевыми факторами:
- Совпадение антигенов - сходство циркулирующего вируса гриппа с вирусом, использованным для изготовления вакцины;
- Иммуногенность - степень реакции антител на вакцинацию (четырехкратная сероконверсия, которая проверяется на 28 день после вакцинации). Индуцированные введением вакцины антитела на уровнях выше критического титра (1:40) обеспечивают защиту от серьезных и смертельных осложнений гриппа;
- Реактогенность - связанные с вакциной побочные эффекты, вызванные действием белков вируса и примесей невирусного происхождения.
В целом, эффективность вакцинации у детей и лиц моложе 60 лет составляет 70-100%.
У конкретного вакцинируемого эффективность вакцинации будет зависеть также от следующих факторов:
- Был ли у вакцинируемого контакт с вирусом гриппа в предыдущие года - в этом случае степень защиты будет больше (эффект бустерной реакции);
- Возраст вакцинируемого. Известно, что вакцинация лиц пожилого возраста вызывает у них более низкий иммунный ответ, что связано с "возрастом" иммунной системы, специфическим уменьшением Т-клеток и снижением их функций. Однако именно эта группа населения наиболее подвержена осложнениям после гриппа, и поэтому вакцинация рекомендуется им в первую очередь. Вакцинация позволяет резко снизить количество осложнений (на 50-60%) и смертельных случаев от гриппа (на 80%) у этой категории населения
Главным индикатором эффективности вакцинации является продукция специфических антител. Ниже указаны протективный уровень антител для взрослых моложе 60 лет и пожилых лиц старше 60-летнего возраста. У пожилых лиц отмечается более низкий иммунный ответ, чем у молодых. Но оба результата соответствуют требованиям ЕС.
Таблица. Серологические защитные уровни при использовании вакцины Инфлювак.
| | Защитный уровень |
| | Компонент вакцины | |
| | A-H3N2 | A-H1N1 | B |
| Возраст | |
| <60 лет | 86.0% | 82.9% | 71.1% |
| старше 60 лет | 68.6% | 60.5% | 60.6% |
Схема производства субъединичной вакцины - После того, как ВОЗ определит эпидемический штамм вируса гриппа в следующем сезоне, она распространяет прототипы вируса ("первичное семя") по производителям вакцин.
- В лабораториях каждый штамм вируса размножается на куриных эмбрионах, что служит основой для "вторичного" потомства, используемого в качестве ресурсов для индустриального производства.
- Так как вирус типа А не очень хорошо изначально реплицируется используются методы генной инженерии. Из вируса выделаются гены, кодирующие гемагглютинин и нейраминидазу и встраиваются в генотип вируса, который хорошо размножается на куриных эмбрионах. Таким образом, рекомбинантный вирус имеет антигенные свойства, требуемые ВОЗ и превосходные репликационные свойства. Для вируса типа В такая процедура также возможна, но обычно в ней нет необходимости.
Схема получения рекомбинантного вируса 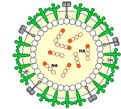 Новый штамм вируса гриппа, рекомендованный ВОЗ + Новый штамм вируса гриппа, рекомендованный ВОЗ + 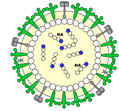 Штамм вируса гриппа PR8, хорошо реплицирующий на куриных эмбрионах Штамм вируса гриппа PR8, хорошо реплицирующий на куриных эмбрионах 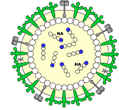 Рекомбинантный вирус Рекомбинантный вирус - Каждый тип вируса получают отдельно, на разных куриных эмбрионах. Данную процедуру проводят для каждого вирусного штамма (всего их 3). После заражения яйцо инкубируется в течение 2-3 дней при температуре 33-35 градусов. Происходит размножение вируса.
- Сто тысяч куриных эмбрионов в возрасте 10-11 дней автоматически инокулируются небольшим количеством "вторичного" вирусного потомства. Для предотвращения контаминации с бактериями происходит обработка дезинфектантами. Яйца инкубируют от 2 до3 дней при оптимальной температуре 33-35 С.
 - Затем происходит сбор материала, ультрацентрифугирование, позволяющее добиться высокой степени очистки от примесей.
- Вирус инактивируют с помощью формальдегида.
- Детергент Триметил-Цетил-Аммониум Бромид (TCAD) позволяет выделять гемагглютинин и нейраминидазу в самостоятельные субъединичные участки.
- Поверхностные белки выделяются с помощью очередного ультрацентрифугирования.
- Белки очищаются от детергента и внутренних составляющих вирусной частицы при помощи диализа.
- Гемагглютинин и нейраминидаза спонтанно соединяются в розетки и помещаются в буферный раствор, содержащий соли калия, натрия, кальция и магния и очень незначительные количества консерванта для полной уверенности в предупреждении бактериальной контаминации.
- Такая процедура применяется для каждого из трех вакцинных компонента - двух подтипов вируса А и подтипа вируса В. Эти компоненты комбинируются в одном шприце, содержащим 0.5 мл раствора.
Каждый год вакцина проходит жесткий контроль качества. В настоящее время существует центральная регистрационная процедура для всех новых вакцин в странах ЕС. Для обеспечения своевременного распространения вакцин, и производители, и органы регистрации находятся под жестким временным давлением. Как только появляется первый образец новой вакцины, сразу проводятся два клинических исследования этой вакцины у молодых лиц и пациентов преклонного возраста для оценки эффективности и переносимости. | |
Вакцины будущего.
 Новый штамм вируса гриппа, рекомендованный ВОЗ +
Новый штамм вируса гриппа, рекомендованный ВОЗ +  Штамм вируса гриппа PR8, хорошо реплицирующий на куриных эмбрионах
Штамм вируса гриппа PR8, хорошо реплицирующий на куриных эмбрионах  Рекомбинантный вирус
Рекомбинантный вирус 
