Осмоляльность/осмолярность
Осмоляльность означает осмотическое число на 1 кг растворителя, осмол яркость — на 1 л раствора.
Осмотическое давление раствора зависит от числа осмотически активных частиц (ионов и недиссоциированных молекул), которые находятся в определенном объеме.
Единица осмотического давления — осмоль или мосммоль (миллиосммоль). Если 1 моль глюкозы (относительная молекулярная масса 180,2; 1 моль= 180,2 г) находится в 1 кг воды, то этот раствор имеет «идеальную» осмоляльность, равную 1 осммоль. Если же внести в 1 кг воды 1 моль поваренной соли (относительная молекулярная масса = 58,4; 1 моль = 58,4 г), то образуется «идеальная» осмоляльность в 2 осммоль, так как поваренная соль распадается на ионы натрия и хлора, вследствие чего в растворе появляется удвоенное число частиц в отличие от глюкозы. В растворах, содержащих полностью диссоциирующие соли, осмотическое Давление упрощенно можно определить по числу катионов и анионов (так называемая идеальная осмоляльность). При этом, конечно, пренебрегают межионным взаимодействием, которое влияет на осмоляльность и ведет к «реальной» осмоляльности.
Осмотические соотношения ответственны за распределение воды ,в различные жидкостные пространства в ортанизме (рис. 5, см. также 1.4.3).
Осмотическое давление определяют измерением снижения точки замерзания (осмометрия).
Осмоляльность плазмы
Осмоляльность плазмы составляет 290 мосммоль (кг воды 38°С), (Geigy).
Плазма состоит в основном из диссоциирующих электролитов, при этом натрий по приближенному расчету определяет половину осмоляльности плазмы. Влияние неэлектролитов в нормальном состоянии незначительно: Глюкоза: 100 мг/дл = 5,5 мосммоль/л плазмы (Geigy) Мочевина: 100 мг/дл=17,2 мосммоль/л плазмы (Geigy) На основе этих представлений можно рассчитать осмоляльность плазмы, если известно количество натрия, мочевины и глюкозы (Mansberger et al.):
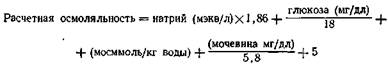
Различия между расчетной и измеренной осмоляльностью доказывают присутствие неизвестных растворенных веществ (токсины?) и служат показаниями для гемодиализа (Mans-berger и соавт.).
Низкая осмоляльность наблюдается только при гипона-триемии; гиперосмоляльное состояние, наоборот, многозначно (Mansberger et al.: гипернатриемия; гиперглюкоземия; уремия; неизвестные вещества; комбинация многих факторов).
Для практических целей из приведенных рассуждений можно сделать вывод, что концентрация натрия в плазме определяет ее осмоляльность. Отклонения наблюдаются особенно часто при диабете, уремии и в присутствии неизвестных растворенных веществ. В связи с этим точное измерение осмоляльности необходимо в каждом отдельном случае.
Эффективное осмотическое давление
Для определения отклонений в осмотическом давлении используют полупроницаемые мембраны. Вещества, частично проходящие через клеточные мембраны, например мочевина, вызывают отклонения осмотического давления только в тех количествах, которые препятствуют проницаемости клеточных мембран. Таким образом, эффективное осмотическое давление создается только истинными ионами.
Тоничность
Нормальная осмоляльность плазмы (290 мосммоль/кг воды) является отправной точкой для тоничности.
Изотоническими растворами являются (приближенно):
—1/6 молярные растворы солей, молекулы которых полностью диссоциируют на 2 иона, например 1/6 молярный раствор поваренной соли;
— 1/3 молярные растворы, если растворяемое вещество не диссоциирует, например 1/3 молярный раствор глюкозы.
Растворы, которые обнаруживают меньшую по сравнению c плазмой осмоляльность, яляются гипотоническими; растворы, обладающие более высокой осмоляльностью, являются гипертоническими.
Осмоляльность клетки соответствует таковой плазмы [Black, Moore, Burck, 1962]. При этом нужно учитывать, что часть электролитов в клетке остается недиссоциированной. На осмотическое давление в клетке постоянно влияет обмен веществ: при распаде больших молекулярных соединений на определенное количество более мелких осмоляльность повышается, при синтезе она снижается.
Коллоидно-осмотическое давление
Коллоидно-осмотическое давление соответствует степени участия белков в осмоляльности.
Так как белковые молекулы очень большие, число частиц на единицу маосы значительно меньше, чем в случае электролитов. Коллоидно-осмотическое давление плазменных белков составляет только 1,6 мосммоль/кг воды (25 мм рт. ст.). Это составляет 0,55% общей осмоляльности плазмы. Наибольший вклад вносит альбумин (85%, Geigy). Несмотря на малую величину осмоляльности плазмы, коллоидно-осмотическое давление имеет большое значение, потому что белки могут выходить из кровеносного русла только медленно. Из этого становится ясным влияние коллоидно-осмотического давления на распределение воды между плазмой и межтканевой жидкостью (см. 1.4.З.). Падение концентрации альбумина в плазме, например, снижает ее способность Удерживать воду (гипопротеинемический отек; восстановление объема циркулирующей крови).
